
12. 某研究性学习小组为了证明NaOH溶液能使酚酞试液变红是OH-的性质,设计了如下方案,其中不可行的是
A.取KOH、Ca(OH)2溶液分别与酚酞试液作用,观察溶液颜色
B.取NaCl、Na2SO4溶液分别与酚酞试液作用,观察溶液颜色
C.向滴有酚酞的20.0 mL 0.10 mol·L-1NaOH溶液中,逐滴加入25.0mL0.10 mol·L-1 的盐酸,观察溶液颜色变化
D.向滴有酚酞的25.0mL 0.10 mol·L-1盐酸中,逐滴加入20.0mL 0.10 mol·L-1的NaOH溶液,观察溶液颜色变化
11. X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.X与W可以形成W2X、W2X2两种化合物
B.Y元素最高价氧化物对应水化物的化学式为H2YO4
C.原子序数由小到大的顺序为W<X<Y<Z
D.Y、Z两元素的简单离子的半径Y>Z
10.下列离子方程式正确的是
A.F2与NaOH 稀溶液反应: F2 +4OH- → 2F- + O2 +2H2O
B.用小苏打治疗胃酸过多:HCO3- +H+ →CO2 ↑+ H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2 +2H++2Cl- →Cl2↑+Mn2+ +H2O
D.向NaOH溶液中滴加同浓度过量的Ca(HCO3)2溶液:
Ca2+ + 2HCO3- +2OH- → CaCO3 ↓+ CO32-+ 2H2O
9. 在一体积不变的密闭容器中充入H2和I2(g),发生反应:H2(g)+I2(g) 2HI(g)+Q,Q>0。当达到平衡后,改变反应的某一条件(不再充任何气体)造成容器内压强增大。下列说法正确的是
2HI(g)+Q,Q>0。当达到平衡后,改变反应的某一条件(不再充任何气体)造成容器内压强增大。下列说法正确的是
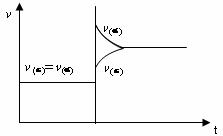
A.容器内气体颜色变深,平均相对分子质量增大
B.平衡不移动,混合气体密度不变
C.平衡向右移动,HI浓度增大
D.反应速率变化如上图所示
8. 下列各溶液中,各离子可能大量共存的有
A.含有大量Ba2+的溶液中:HCO3-、Fe3+、Ag+、SO42-、SCN-
B.滴加无色酚酞试液后仍无色的溶液中:Na+、CO32-、K+、ClO-、AlO2-
C.由水电离的c(OH-)=10-14mol·L-1 的溶液中:CH3COO-、C6H5O-、Na+、K+
D.加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、Cl-、HS-
7.设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.100g 98%的浓硫酸中含氧原子个数为4NA
B.1mol 苯分子中含有碳碳双键数约为3×6.02×1023
C.标准状况下,22.4LCH4和CO2的混合物所含有的分子数目为NA
D. 60g SiO2晶体中含SiO2分子数约为6.02×1023
6.下列各组物质或粒子的分类正确的是
A.同位素:1H、2H+、3H-
B.非电解质:SO2、NH3、C2H5OH
C.非极性分子:C60、CO2、CH2Cl2
D.同系物:  -OH、CH3-
-OH、CH3- -OH、CH3-
-OH、CH3- -CH2OH
-CH2OH
5.反应E+F→G在温度T1下进行,反应M+N→K在温度T2下进行,已知T1>T2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者的反应速率
A. 前者大 B. 后者大 C. 一样大 D. 无法判断 二、选择题(本题共36分),每小题3分,只有一个正确选项。
4. 常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到
750℃时,硫蒸汽主要以S2形式存在(占92%)。下列说法正确的是
A.S8转化为S6、S4、S2属于物理变化 B.不论哪种硫分子,完全燃烧都生成SO2
C.常温条件下单质硫为原子晶体 D.把硫单质在空气中加热到750℃即得S2
3. 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1mol N-N吸收167kJ热量,生成1molN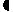 N放出942kJ热量。根据以上信息和数据,下列说法正确的是
N放出942kJ热量。根据以上信息和数据,下列说法正确的是

A.N4属于一种新型的化合物 B.N4沸点比P4(白磷)高
C.N4分子存在非极性键 D.1molN4气体转变为N2将吸收882kJ热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com