
3.以下化学用语及名称正确的是
A.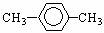 的名称是对二甲苯
的名称是对二甲苯
B.甘油的分子式 C3H8O3
C.乙醛的结构简式 CH3COH
D.葡萄糖的最简式 C6H12O6
2.下列说法正确的是
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
B.凡含有食品添加剂的食物对人体健康均有害,不宜食用
C.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源
D.钢铁在海水中比在河水中更易腐蚀,主要原因是海水中含有游离态氧
1.在探索地球上生命的起源活动中,科学家们做了一个著名的实验,他们模拟原始大气的成份将甲烷、氨、氢和水蒸气混合,放入真空的玻璃仪器中进行实验。一个星期后,他们惊奇地发现仪器中果然有数种氨基酸生成。你从该实验中能得出的结论是
A.一定发生了化学变化 B.没有发生化学变化
C.无法判断是否发生了化学变化 D.一定没有发生物理变化
22.(9分)在四川的抗震救灾中,大量的化学试剂和药品发挥了很好的保障生活、防疫治病的作用。
(1)人的生活和生命都离不开食盐。将下列关于氯化钠的描述进行分类:
①氯化钠是由钠元素和氯元素组成的
②氯化钠在维持人体内的电解质平衡中起重要作用
③氯化钠是常用的调味品
④氯化钠中钠离子和氯离子的个数相等
可将上述四项分成两类,则分类的依据分别是________________、_______________。
(2)救灾首先要保证人畜的饮用水清洁无菌。高铁酸钾(K2FeO4)是一种比Cl2、O3化学性质更强、用途更广、无二次污染的多功能绿色水处理剂,其制备反应:
2Fe(OH)3+3ClO-+4OH-===2FeO42-+3Cl-+5H2O。
其消毒净水的反应原理为:FeO42- Fe3+ Fe(OH)3。请回答:
①每生成1 mol K2FeO4转移电子 。
②K2FeO4能消毒是由于其具有 。
③K2FeO4能净水是由于产物能形成 ,吸附悬浮物,其净水过程_________
a.只有物理过程 b.只是化学过程 c.是物理和化学过程
(3)AlCl3也是常用的净水剂,其净水原理用离子方程式表示为: 。
21.(8分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为
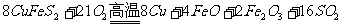
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是___________(填元素符号)。
(2)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、AI2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是____________ __。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为_____________。
c.证明炉渣中含有FeO的实验现象为 。
20.(5分)食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、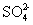 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
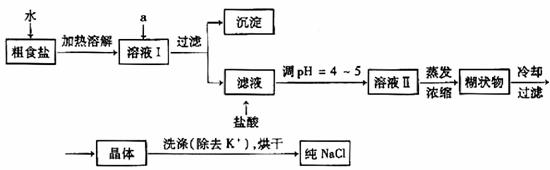
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、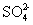 离子,选出a所代表的试剂,按滴加顺序依次为________ _ (只填化学式)。
离子,选出a所代表的试剂,按滴加顺序依次为________ _ (只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_________。
19.(12分)下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500mL的操作,请按要求填空:
(1)所需浓H2SO4的体积为 。
(2)如果实验室有10mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。
(3)如果先用100mL水来稀释浓H2SO4请写出具体操作 。
(4)将 的上述溶液沿 注入 中,并用50mL蒸馏水洗涤烧杯2-3次,洗涤液要 中,并摇匀。
(5)加水至距刻度 处,改用 加水,使溶液的凹液面正好跟刻度相平。
18.(6分)下列有关物质分离提纯的方法正确的是 (填序号)。
①由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来;
②水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精;
③由于胶粒的直径比离子大,所以淀粉溶液中混有的碘化钾可用渗析法分离;
④由于氯化钠的溶解度随温度变化改变较小,所以可用冷却法从热的含有少量硝酸钾的氯化钠浓溶液中分离得到纯净的氯化钠晶体;
⑤由于高级脂肪酸钠盐在水中的分散质微粒直径在1nm-100nm之间,所以可用食盐使高级脂肪酸纳从皂化反应后的混合物中析出;
⑥氯化氢气体极易溶于水,且饱和食盐水中的氯离子能促进反应
C12+H2O HC1+HC1O向逆方向进行,所以用盛有饱和食盐水的洗气瓶,既可除去氯气中混有的少量氯化氢气体;
HC1+HC1O向逆方向进行,所以用盛有饱和食盐水的洗气瓶,既可除去氯气中混有的少量氯化氢气体;
⑦由于粗铜中混有Zn、Fe等比Cu活泼的金属,电解时也会溶解,所以不可用电解法提炼高纯高的铜;
⑧除去FeC13溶液中有的少量FeC12:加入足量铁屑,充分反应后,过滤。
17.(8分)某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外的反应物与生成物分别填入以下空格内。

(2)反应中,被还原的元素是 ,还原剂是 。
(3)将氧化剂与还原剂填入下列空格中,并用单线桥法标出电子转移的方向和数目。

(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂的物质的量之比为 。
16.(7分)用下列仪器的编号回答问题
①容量瓶 ②蒸馏烧瓶 ③酸式滴定管 ④量筒 ⑤烧杯 ⑥托盘天平 ⑦分液漏斗
⑴加热时必须垫石棉网的有 ,
⑵使用时必须检查是否漏水的有 ,
⑶标有零刻度的有 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com