
4.下列有机物的关系说法正确的是( )
A.丙酸和油酸互为同系物
B.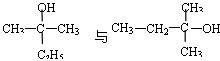 互为同分异构体
互为同分异构体
C.A代表芳香烃、B代表芳香族化合物、C代表苯的同系物
D.乙醇和乙醚是同分异构体
3.正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A.脂肪不是酯、甘油不是油、油酸不是酸B.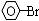 的官能团:
的官能团: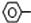
C.醛基的电子式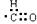 D.石油的馏分不是纯净物
D.石油的馏分不是纯净物
2.下列说法不正确的是( )
A.乙二醇是一种无色、黏稠、有甜味的液体,它的水溶液凝固点高,可用作内燃机的抗冻剂
B.有机物沸点按由高到低的顺序排列是:正戊烷>异戊烷>新戊烷>正丁烷>异丁烷
C.诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”指“蛋白质”,“泪”指“烃”
D.乙醛又名蚁醛,是一种无色、有刺激性气味的气体,易溶解于水
1. 生活是化学的源泉,下列有关生活中的化学叙述不正确的是( )
A.2008年 6月1日起,在全国范围内将禁止生产、销售、使用厚度小于0.025毫米的塑料。“限塑令” 从一定程度上控制了环境的“白色污染”蔓延
B.纤维素和羊毛水解的最终产物均为葡萄糖
C.在采煤工业上,把干冰与炸药放在一起,既能增强爆炸威力,又能防止火灾
D.玻璃钢是一种复合材料,它具有强度高、耐高温、耐腐蚀的优良性能
22.(9分)已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子效是内层电子数的2倍。E元素与D元素同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)画出E的阴离子的结构示意图: 。
(2)由A、C、D可以形成一种盐,此盐中A、C、D元素的原子个数比为4︰2︰3,该盐的化学式是 ,其含有的化学键类型有 。
(3)在通常情况下,化合物CD2与C2D4能相互转化。现将装有CD2的烧瓶放入热水中,观察到的现象为 。
(4)将9gB单质在足量D单质中燃烧,所得气体通入1L lmol L-1的NaOH溶液中,完全吸收后,所得产物的物质的量浓度分别为 。
21.(14分)某研究性学习小组设计下图装置制取氯气并以氯气为原料进行实验。
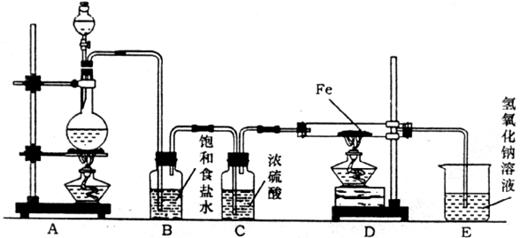
(1)装置A烧瓶中发生反应的化学方程式为 。
(2)装置B中饱和食盐水的作用是 ,装置C中浓硫酸的作用是 。
(3)实验时,先点燃 处的酒精灯,再点燃 处酒精灯,写出D中反应的化学方程式 。写出E中反应的离子方程式 。
(4)若实验中用12mol·L-1浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是① ,② 。欲使反应生成Cl2的物质的量最大程度的接近0.03mol,则在装置气密性良好的前提下实验中应采取的措施是 。
20.(8分)当前,国际石油价格持续上涨,每桶原油期货价格达到了130美元左右,为了减少石油价格带来的影响,很多汽车开发商开始投资研制以各种电池为动力的汽车。
(1)在银锌原电池中,以硫酸铜为电解质溶液,锌为 极,银电极上的电极反应式是 ;当烧杯中的溶液质量变化1g时,电路中有 mol电子通过。
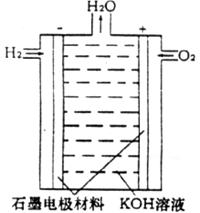
(2)氢氧燃料电池是目前最成熟的燃料电池。下图为一种氢氧燃料电池结构示意图,电解质溶液为氢氧化钾溶液,电极材料为石墨,氢气和氧气(或空气)源源不断地通到电极上。该燃料电池负极的电极反应式为 ,电池反应为 。
19.(10分)某课外实验小组利用稀硫酸与金属铁反应探究影响化学反应速率的因素,得到如下实验数据:
|
实验序号 |
铁的质量/g |
铁的形态 |
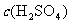 / / |
V(H2SO4)/mL |
溶液温度/℃ |
金属消失的时间/s |
|
|||
|
反应前 |
反应后 |
|
||||||||
|
1 |
0.10 |
铁片 |
0.7 |
50 |
20 |
36 |
250 |
|
||
|
2 |
0.10 |
铁片 |
0.8 |
50 |
20 |
35 |
200 |
|
||
|
3 |
0.10 |
铁粉 |
0.8 |
50 |
20 |
36 |
25 |
|
||
|
4 |
0.10 |
铁片 |
1.0 |
50 |
20 |
35 |
125 |
||
|
5 |
0.10 |
铁片 |
1.0 |
50 |
35 |
50 |
50 |
|
||
分析上述数据,回答下列问题:
(1)实验2和3表明, 对反应速率有影响,影响规律是 。
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号)。
(3)本实验中影响反应速率的其他因素还有 ,能体现该影响因素的实验序号是 。
(4)在实验4中滴入几滴硫酸铜溶液,金属消失的时间小于125s,原因是 。
(5)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,试从反应过程能量的变化角度推测其原因 。
18.(11分)有机物种类繁多,应用广泛。根据所学有机物的知识,回答下列问题:
(1)2008年6月1日开始实施的“限塑令”是解决“白色污染”的重要措施。有机物A是合成食品包装塑料袋的原料,它的产量可作为衡量一个国家石油化工发展水平的标志。在一定条件下,A发生加聚反应生成塑料袋材料的化学方程式为 。A可跟水发生加成反应生成B,将一根光洁的铜丝绕成螺旋状,放在酒精灯外焰上加热,然后伸入盛有B的试管中,铜丝变化的现象为 ,B中发生反应的化学方程式为 。
(2)有机物C的化学式为C2H4O2,它是一种常用的调味品,它能使紫色石蕊试液变红,C与B在一定条件下能反应生成一种具有水果香味的物质,该反应的化学方程式为 ,其反应类型为 。
(3)北京“祥云”火炬用的燃料是丙烷,某有机物E跟丙烷同类,其化学式是C4H10,写出E的所有同分异构体的结构简式 。
17.(8分)根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有 种,失电子能力最强的元素是 (填元素符号)。
(2)形成化合物种类最多的两种元素是 (填元素符号)。
(3)第三周期中,原子半径最大的元素的单质(稀有气体除外)与氧气反应生成的所有化合物的化学式为 。
(4)推测P、O元素最简单气态氢化物的稳定性较强的是 (填化学式)。
(5)第ⅢA族某元素最高价氧化物对应水化物呈两性,该水化物与烧碱溶液反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com