
9.某炼金厂的废水因连降暴雨而溢出,导致河水严重污染。炼金废水中所含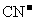 有剧毒,其性质与卤素离子相似,还原性介于
有剧毒,其性质与卤素离子相似,还原性介于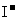 与
与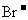 之间,HCN为弱酸。下列说法不正确的是
之间,HCN为弱酸。下列说法不正确的是
A.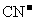 可以和稀硫酸反应生成HCN B.
可以和稀硫酸反应生成HCN B.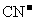 可被Cl2氧化成(CN)2
可被Cl2氧化成(CN)2
C.在水溶液中(CN)2可被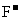 还原 D.HCN的电子式为
还原 D.HCN的电子式为
8.家用消毒液发生器是化学知识在日常生活中的“创新”应用,该发生器利用常见的精盐和自来水为反应物。通电时,器内电解槽的极板上产生大量气泡,切断电源后所得消毒液具有强烈的杀菌能力,且对人体无害。与该反应器直接有关的反应是
①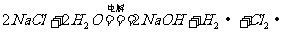
②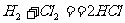
③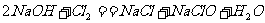
④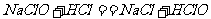
A.只有① B.①③ C.①③④ D.①②③④
7.某同学从一种未知的无色溶液中检验出含有Ba2+和Ag+,同时测得溶液的pH=1,他还准备继续检验溶液中是否还含有下列离子: 、
、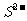 、
、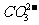 、
、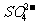 、
、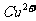 、
、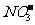 、
、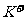 、
、 、
、 、
、 ,你认为其中不必检验的离子有
,你认为其中不必检验的离子有
A.4种 B.5种 C.6种 D.7种
6.用NA表示阿伏加德罗常数的值,下列说法中不正确的是
A.23g Na和O2恰好完全反应,一定失去NA个电子
B.1mol的KClO3与足量的浓盐酸反应,得到的电子数为5NA
C.含有2NA个阴离子的Na2O2固体,投入足量水中,能产生约22.4L(标准状况)的氧气
D.标准状况下,2.24L氧单质所含原子数一定为0.2N
5.下列有关工业生产的说法中,错误的是
A.氯碱工业中隔离两电极的材料是阳极交换膜,因此该生产方法又称“阳离子交换膜法”
B.生产普通玻璃的主要原料及设备是:石灰石、石英、纯碱及玻璃熔炉
C.常压下SO2转化为SO3的转化率已经较高,所以SO2转化为SO3时不需高压条件
D.合成氨的反应是放热反应,因此工业合成氨时常采用低温条件
4.镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素。镓的原子序数为31,属ⅢA族。镓的熔点为29.78℃,沸点高达2403℃。镓有过冷现象(即冷至熔点下不凝固),它可过冷到-120℃。由此判断下列有关镓的性质及其用途的叙述不正确的是
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸和强碱
C.镓与锌、锡、铟等金属制成的合金,可用在自动救火的水龙头中
D.近年来镓成为电子工业的新宠,其主要用途是制造半导体材料
3.目前一些汽车制造商开始生产环保汽车,以氢气作燃料,因为氢气燃烧的唯一生成物是水蒸气,所以不会对环境造成污染。但这种环保也是有一定限度的,氢气在空气中燃烧过程中也会产生有害物质,这些物质是
A.二氧化碳 B.二氧化硫
C.二氧化氮和一氧化氮 D.一氧化碳
2.下列说法错误的是
A.铅笔芯的主要原料是石墨,儿童在使用时不会引起中毒
B.CO有毒,生有煤炉的居室可放置数盆清水,这样可有效地吸收CO,防止煤气中毒
C.“汽水”浇灌植物有一定的道理,其中二氧化碳的缓释,有利于作物的光合作用
D.硅的提纯与应用,促进了半导体元件与集成芯片业的发展,可以说“硅是信息技术革命的催化剂”
1.飘尘是物质燃烧时产生的粒状飘浮物,颗粒很小,不易沉降。它与空气中的SO2、O2接触时,SO2会部分转化为SO3,使空气的酸度增加。飘尘所起的作用可能是
A.氧化剂 B.还原剂 C.催化剂 D.吸附剂
29.(15分)某校化学研究性学习小组的同学在学习了金属的知识后,为了解Cu的常见化合物性质,运用类比学习的思想提出如下的问题,进行探究。请你协助该小组的同学完成下列研究。
[提出问题]
①Cu的金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
[实验方案]
(1)解决问题①需用到的药品有CuSO4溶液、 (填试剂),同时进行相关实验。
(2)解决问题②的实验步骤和现象如下:取98gCu(OH)2固体,加热至80℃-100℃C时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A。冷却后称量,A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。据此可推得,A的化学式为 。
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):
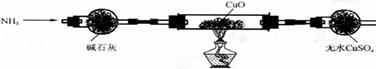
实验中观察到Cu0变为红色物质,无水CuS04变蓝色。同时生成一种无污染的气体。
[实验结论]
(1)Cu(OH)2具有两性。证明Cu(OH)2具有两性的实验现象是 。
(2)根据“实验方案(2)”,得出的+1价Cu和+2价Cu稳定性大小的结论是 。
(3)CuO能被NH3还原。该反应的化学方程式为 。
[问题讨论]
有同学认为NH3与CuO反应中生成的红色物质是Cu,也有同学认为NH3与CuO反应中生成的红色物质是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com