
3.设NA为阿伏伽德罗常数的值,下列叙述中正确的是
A.电解饱和食盐水时,阳极上生成22.4L气体时转移的电子数为2NA
B.常温、常压下,32g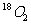 中所含的中子数为20NA
中所含的中子数为20NA
C.工业上铜的电解精炼时,电解池中每转移1mol电子,阳极上溶解的铜等于0.5 NA
D.1mol NaCl晶体中含有图所示的结构单元的数目为0.25NA

2.下列叙述不正确的是
A.硅是人类将太阳能转换为电能的常用材料
B.硅胶可用于某些气体和袋装品的干燥剂
C.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
D.电流通过胶体时,胶体就会发生丁达尔现象
1.背景材料:①2006年5月信息时报报道:世界卫生组织建议每天钠的摄取量少于2000mg,长期过量摄入钠可能引起高血压、肾病、胃病;②2006年初夏,四川大部分地区进行人工降雨;③空气是人类生存所必需的重要资源。改善空气质量称为“蓝天工程”;④2008年夏季奥运会将在我国举行,这次奥运会要突出“绿色奥运、科技奥运、人文奥运”的理念。下列相应说法不正确的是
A.钠是活泼金属,常常保存在煤油中,人们每天可以摄取少于2000mg的金属钠
B.AgI和干冰都可用于人工降雨
C.加大石油、煤炭的开采速度,增加化石燃料的供应量不利于“蓝天工程”的建设
D.把环境保护作为奥运设施规划和建设的首要条件之一
26.(6分)以石墨为电极,在烧杯中电解含等物质的最的NaCl和AlCl3的混合溶液足够长时间(不考虑气体在溶液中的溶解,最终溶质不含NaCl)。
(1)电解过程中可看到的现象: 。
(2)若在阳极收集到8.96L纯净气体(已折算成标准状况下),且最终溶液的体积为200mL,则该溶液中溶质的物质的量浓度为 mol/L。
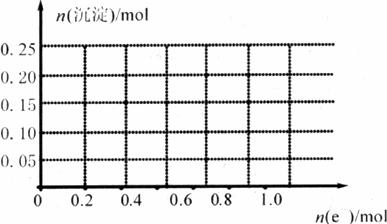
(3)在图3-6中画出(2)中电极上通过电子的物质的量与溶液中沉淀的物质的量的关系图。
25.(10分)某同学设计了图3-5所示装置进行探究。(夹持装置已略去)
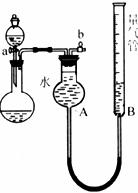
(1)进行“铜和稀硝酸反应制取NO”的实验。
①制取NO的化学方程式: 。
②收集气体前必须先 ,然后才开始收集气体。
(2)利用该装置制取并收集少量其他气体,请完成下表:
|
制取气体 |
药品 |
|
O2 |
_________、_________ |
|
H2 |
_________溶液、Al |
(3)利用该装置进行实验,并根据产生氢气的量来确定某酸的结构:
①反应前,先对量气管进行第一次读数。读数时,应注意的操作是 ,并使视线凹液面最低处相平;反应后,待 时,再对量气管进行第二次读数。
②实验数据记录如下:(表中读数已折合成标准状况下的数值)
|
编号 |
酸的质量 |
金属锌的质量 |
量气管第一次读数 |
量气管第二次读数 |
|
1 |
1.459 |
10.09(足量) |
40ml。 |
264mL |
|
2 |
1.459 |
10.09(足量) |
30mi。 |
228mL |
|
3 |
1.459 |
10.09(足量) |
20mL |
243mL |
已知该酸的相对分子质量为145。根据上述数据可确定该酸是 元酸;
③如果第二次对量气管读数时仰视,则所测得的气体体积会 (填“偏大”、“偏小”或“不能确定”)
24.(10分)有机物参加的反应往往比较复杂,常有副反应发生;如图乙烯跟溴水反应既可生成A,同时又可生成B和C2H5Br。
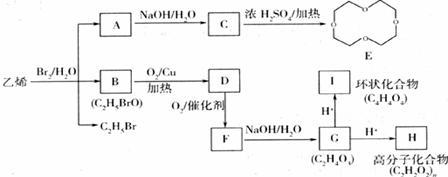
回答下列问题:
(1)环氧乙烷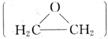 的结构可简写为
的结构可简写为 , .则E的分子式是
。
, .则E的分子式是
。
(2)B的结构简式是 ;I的结构简式是 。
(3)写出G转化为H的化学方程式: 。
(4)化合物A-I中,易发生加成反应的物质是 (填字母)。
23.(10分)研究表明,火灾中绝大多数人的第一死因并非高温烘烤或火烧,而是慌乱奔跑时吸入烟雾中毒,且起火的建筑装修越豪华,这一点越明显。聚氯乙烯是制作装修材料的最常用原料,失火时聚氯乙烯在不同的温度下,发生一系列复杂的化学变化,产生大量有害气体,其过程大体如下:
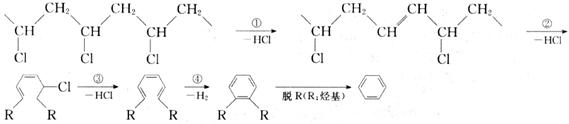
请回答下列问题:
(1)火灾中由聚氯乙烯产生的有害气体,其化学成分主要是 ,你认为其中含量最大的为 ,在火灾现场,为防止气体中毒的防护措施是 ;
(2)工业上用乙烯和氯气为原料经下列各步合成PVC: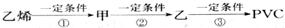 ,乙是PVC的单体,其结构简式为 ,反应①、③的化学方程式分别为 、 。
,乙是PVC的单体,其结构简式为 ,反应①、③的化学方程式分别为 、 。
(3)聚氯乙烯可以制成保鲜膜,化学工作者十分关注聚氯乙烯(PVC)保鲜膜的安全问题。PVC保鲜膜的安全隐患主要来自于塑料中残留的PVC单体以及不符合国家标准的增塑剂DEHA。邻苯二甲酸辛酯(DOP)是国家标准中允许使用的增塑剂之一,邻苯二甲酸酐(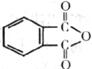 )是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酸酯,写出制取DMP的反应方程式: 。
)是制造DOP的原料,它跟过量的甲醇反应能得到另一种增塑剂DMP(分子式为C10H10O4),DMP属于芳香酸酯,写出制取DMP的反应方程式: 。
22.(10分)A、B、C是三种常见的短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素原子最外层电子数比B多一个。甲、乙、丙是三种最高价含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙的水溶液均有较强的碱性,乙的水溶液pH小于7。丁为一种气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如图3-3:(图中略去了物质转化时的部分生成物)
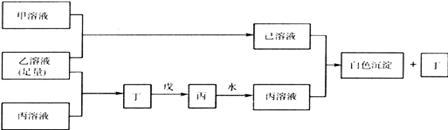
回答下列问题:
(1)写出A、B、C三种元素的元素符号 、 、 。
(2)写出戊的电子式 。
(3)若乙溶液不足量,乙溶液分别和甲、丙溶液也能发生化学反应,但生成物不是己和丁。写出不足量的乙溶液分别和甲溶液、丙溶液反应时的离子反应方程式:
乙+甲: ;
乙+丙: 。
(4)写出己溶液和丙溶液反应的离子方程式: 。
21.(6分)“碘钟”实验中,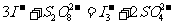 的反应速率可以用
的反应速率可以用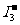 与加入的淀粉溶液显蓝色的时间
与加入的淀粉溶液显蓝色的时间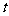 来度量,
来度量,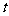 越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
|
试验编号 |
① |
② |
③ |
④ |
⑤ |
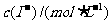 |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
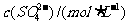 |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
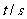 |
88.0 |
44.0 |
22.0 |
44.0 |
 |
回答下列问题:
(1)该实验的目的是 。
(2)显色时间 = 。
= 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间 的范围为 (填字母)
的范围为 (填字母)
A.<22.0s B.22.0-44.0s C.>44.0s D.数据不足,无法判断
20.(9分)微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体,将有机物的化学能转化为电能。以葡萄糖溶液为例,其工作原理如图所示。已知石墨电极上反应为: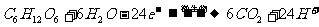 。
。
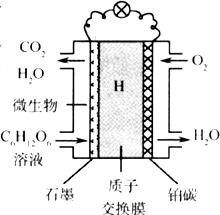
(1)电池中的质子交换膜只允许质子和水分子通过。电池工作时,质移向电源的 极,铂碳上所发生的电极反应式为 。
(2)葡萄糖的燃烧热为2800kJ/mol,写出葡萄糖燃烧的热化学方程式: ___ 。
(3)化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果ll。废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是 (填序号)。
|
序号 |
A |
B |
C |
D |
E |
|
污水类型 |
生活污水 |
印染 |
电镀 |
造纸 |
硫酸工业废水 |
|
COD值/(mg/L) |
520 |
870 |
20 |
960 |
120 |
(4)在化学工作者的眼中,“垃圾是放错了位置的资源”。写出硫酸工业“废气”处理利用的化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com