
6.下列物质中,既有离子键又有共价键的是( )
A.CaCl2 B.KOH C.H2O D.H2SO4
5.下列各物质性质的比较中,正确的是( )
A.稳定性:NH3>H2O>HF B.稳定性HF> HCl> HBr >HI
C.碱性:Al(OH)3>Mg(OH)2>NaOH D.酸性:H2SiO3>H3PO4>H2SO4
4.下列电子式书写正确的是( )
A.Cl
H+﹝: :﹞-
B.HClO H:
:﹞-
B.HClO H: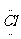 :
: :
:
C.H2O2 ﹝H: :﹞2
D.Na2O2 Na+﹝:
:﹞2
D.Na2O2 Na+﹝: :
:  :﹞2- Na+
:﹞2- Na+
3.某粒子含有6个质子,7个中子,电荷为0,则它的化学符号是 ( )
A. 13Al B.13 Al C.13 C D. 13 C
2.根据右图微粒结构示意图的共同特征,可以把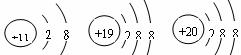
三种微粒归为一类。下列微粒中也可以归为这一类的是 ( )
A.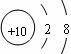 B.
B. C.
C. D.
D.
1.1992年我国取得的重大科技成果之一是发现了三种元素的所有同位素,其中之一是  ,它的中子数为( )
,它的中子数为( )
A.80 B.128 C.208 D.288
26.(6分)取50.00 g纯净Na2SO3·7H2O晶体,经600℃以上加热至恒重,计算表明,恒重后样品质量相当于无水Na2SO3的质量,但将它溶于水后,却发现溶液的碱性大大高于期望值,经过仔细思考,这位同学解释这种反常现象,并设计了一组实验,验证了自己的解释是正确的。
(1)他对反常现象的解释是 。
(2)他设计的验证实验是 。
25.(7分)为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计出了如下图所示的4种实验装置,请回答下列问题:

(1)选择任意一种实验装置,简述出现的实验现象,解释产生该实验现象的原因:
选择的实验装置是 ,实验现象为 。产生该实验现象的原因是 。
(2)某同学质疑上述实验设计,该同学质疑的依据是 。
(3)在原实验基础上,请你设计实验证明CO2和NaOH肯定发生了化学反应。
24.(6分)甲、乙、丙三位同学在实验室分别用金属单质A和非金属B做实验,可以生成化合物AB,化学方程式为A+B→AB。充分反应时各自所用A、B的质量不相同,但总质量相等,均为9.00g,有关实验的数据记录如下表:
|
|
A的溶液 |
B的用量 |
AB的产量 |
|
甲 |
7.00g |
2.00g |
6.00 g |
|
乙 |
4.00g |
5.00g |
6.00 g |
|
丙 |
 g g |
 g g |
4.44 g |
试求:
(1)A+B→AB的反应中,A、B、AB三者质量比;
(2)丙同学在实验中, 和
和 的值分别为多少。
的值分别为多少。
23.(10分)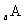 、
、 、
、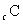 、
、 、
、 是五种短周期元素,它们都是生命体不可缺少的重要元素。已知它们的原子序数有如下关系:
是五种短周期元素,它们都是生命体不可缺少的重要元素。已知它们的原子序数有如下关系: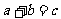 ,
, ,
,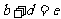 ,B、D、E都有多种同素异形体。B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但有一点是肯定的,那就是没有第三种元素形成化合物的种数会超出它们。根据以上信息回答下列有关问题:
,B、D、E都有多种同素异形体。B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但有一点是肯定的,那就是没有第三种元素形成化合物的种数会超出它们。根据以上信息回答下列有关问题:
(1)请参照NH3沸点较高的特点,比较B2A4、C2A4、E2A4三种化合物的沸点,由高到低的顺序是 。
(2)从给定的元素中选出若干种组成化合物,写出相对分子质量最小的离子化合物的化学式。
(3)从题中元素为选择对象,写出不少于三种炸药的化学式或名称: 、 、 。
(4)有人设想某种分子式为C4N4O8的物质(该物质中同种原子的化学环境完全相同)是一种威力极强的炸药,请推测它的结构简式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com