
6.下列事实与氢键有关的是( )
①NH3易液化;②氧族元素的氢化物中,H2O的沸点最高;③卤族元素的氢化物中,HF的稳定性最强;④冰的密度比水小;⑤H2S的还原性强于H2O
A.①②③ B.①②④ C.①②③④ D.全部
5.下列叙述正确的是( )
A.原子晶体都是单质,晶体中只含有共价键
B.离子晶体都是化合物,晶体中只含有离子键,不含有共价键
C.分子晶体既有单质又有化合物,晶体中只存在分子间作用力,不含有其他化学键
D.金属晶体都是单质,晶体中含有阳离子,但不含有阴离子
4.下列各组物质中,化学键类型相同,晶体类型也相同的是( )
A.C(金刚石)和CO2 B.NaBr和HBr
C.CH4和H2O D.Na2O2和H2O2
3.下列高分子材料与其用途对应关系不正确的是( )
|
|
材料 |
用途 |
|
A |
聚乙烯 |
食品袋、包装袋 |
|
B |
合成橡胶 |
橡皮管、轮胎 |
|
C |
硅聚合物.聚氨酯 |
人工心脏等人造器官 |
|
D |
玻璃钢 |
高强度导电材料 |
2.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷。已知丙烷的燃烧热为 2221.5 KJ/mol,下列有关说法不正确的是( )
A.丙烷的沸点比正丁烷低
B.奥运火炬燃烧主要是将化学能转变为热能和光能
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)===3CO2(g)+4H2O(1);
 2 221.5 kJ/mol
2 221.5 kJ/mol
1.下列叙述,从化学角度分析正确的是( ).
A.木材、棉花、羊毛、尼龙都属于天然纤维,而锦纶、碳纤维、光导纤维则属于合成纤维
B.煤气化技术的使用,虽然能达到减少二氧化硫和烟尘排放的目的,但不能提高煤的燃烧效率
C.食用植物油的主要成分是高级饱和脂肪酸甘油酯,是人体的营养物质
D.改进塑料的配方和生产工艺,研究开发易分解的新型塑料,如淀粉塑料、水溶塑料、光解塑料等是治理“白色污染”的发展方向
27、碘盐是日常生活中必不可少的调味品,我国强制推广食用加碘盐。根据GB5461--
《国家食用盐标准》,碘元素含量为20-50mg/kg为合格。质量监督部门为检测某品牌加碘
盐是否合格,进行了如下实验:称取250g 某品牌加碘盐样品,在酸性条件下用足量KI溶
液将其中IO3-全部转化成I2,生成的I2再用0.010mol/L的硫代硫酸钠溶液滴定,滴定到终
点时用去12mL。
有关反应如下:①IO3-+5I-+6 H+ 3I2+3H2O
3I2+3H2O
②I2+2S2O32- 2I-+S4O62-
2I-+S4O62-
(1)用硫代硫酸钠溶液滴定I2时,应用_____作指示剂,滴定到终点的现象是________;
(2)试通过计算说明该加碘食盐是否为合格产品(写出具体的计算过程)。
26.现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
单质能与水剧烈反应,所得溶液呈弱酸性 |
|
X |
L层p电子数比s电子数多2个 |
|
Y |
第三周期元素的简单离子中半径最小 |
|
Z |
L层有三个未成对电子 |
(1)写出元素X的原子基态时的电子排布式 。写出元素Z的气态氢化物的电子式__________(用元素符号表示)
(2)写出Y元素最高价氧化物水化物的电离方程式________________________________。
(3)元素T与氯元素相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是_____。
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液不能置换出氯气
c.氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之-。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是 ,理由 。
25.(12分)布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:

请回答下列问题:
⑴A长期暴露在空气中会变质,其原因是 。
⑵有A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是 。(填字母)
a. b.
b. c.
c. d.
d.
⑶在E的下列同分异构体中,含有手性碳原子的分子是 。(填字母)
a. b.
b.
c. d.
d.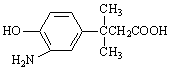
⑷F的结构简式 。
⑸D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是 。高聚物L由H通过肽键连接而成,L的结构简式是 。
24.下列是A、B、C、D、E、F、G、H及丙二酸(HOOCCH2COOH)间转化反应的关系图。A是一种链状羧酸,分子式为C3H4O2;F中含有由七个原子构成的环;H是一种高分子化合物。请填写下列空白: (1)写出结构简式:A ;C ;F 。
(2)写出下列反应的反应类型:A→B: ;
D+E→F: ;E→G: 。

(3)写出下列反应的化学方程式:
①A→H: 。
②B→D: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com