
5.下列各组物质中,按熔点由低到高排列正确的是 ( )
A.SiO2、NaCl、CO2 B.HF、HCl、HBr
C.NaCl、KCl、RbCl D.Na、Mg、Al
4.最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如上图所示,则该晶体的化学式为 ( )
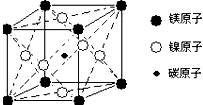
A.Mg2CNi3 B.MgC2Ni C.MgCNi2 D.MgCNi3
3.下图是一种新型无机材料的结构示意图,它含有B和N两种元素,具有与石墨类似的片层结构。有关该无机材料用途的叙述,正确的是 ( )
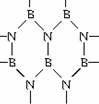
A.是一种坚硬耐磨的材料 B.是高温润滑材料、导电材料
C.是生产化学纤维的原料 D.不能确定
2.碘的熔沸点低,其原因是 ( )
A.碘的非金属性较弱 B.I-I键的键能较小
C.碘晶体属于分子晶体 D.I-I共价键的键长较长
1.下列物质中,其水溶液能导电、溶于水时化学键被破坏,且该物质属于非电解质的是( )
A.I2 B.BaCO3 C.CO2 D.C6H12O6(葡萄糖)
32.向8克二价金属的氧化物固体中加入稀硫酸,使其恰好完全溶解,已知所消耗的硫酸体积为100毫升,在所得溶液插入铂电极进行电解,通电一定时间后,在一个电极上收集到224毫升(标准状况)氧气,在另一个电极上得到1.28克该金属。
|
(2)计算通电后硫酸溶液的物质量浓度(溶液体积按100毫升计算)。
31.某温度下将一定量密度为1.15克/毫升的氯化钠溶液用惰性电极电解,设氯化钠恰好完全电解且无其它反应发生时,得到的溶液中氧元素的质量分数为80%,试计算:
(1)电解后溶液中溶质与溶剂的物质的量之比。
(2)原氯化钠溶液的物质的量浓度。
30.常温下将0.01molCH3COONa和0.001molHCl溶于水,配制0.5L混合溶液。判断:
(1)溶液中共有 种微粒;
(2)溶液中有两种微粒的物质的量之和一定等于0.01mol,它们是 和 ;
(3)溶液中n(CH3COO-)+n(OH-)-n(H+)= mol。
29.从H+、Na+、Cu2+、Ba2+、Cl-、SO42-离子中,选出恰当的离子组成一种电解质,将电解质溶液按下列要求进行电解(均是惰性电极):
(1)电解时电解质含量减小,水量不变,则所采用的电解质是 ;
(2)电解时电解质的质量保持不变,水量减小,则所采用的电解质是 ;
(3)电解时电解质和水的质量都发生变化,则所采用的电解质是 ;
28.以铁为阳极,铜为阴极对足量的NaOH溶液电解,一段时间后,得到了2mol Fe(OH)3固体,那么此间共消耗了水 ( )
A.3mol B.4mol C.5mol D.6mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com