
1.下列关于胶体的说法中正确的是 ( )
A.胶体外观不均匀 B.胶粒不能通过滤纸
C.胶粒做不停的、无秩序的运动 D.氢氧化铁胶体带正电
10.A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B,D分别是同一主族元素,B、D元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体。请回答:
(1)C、D组成的常见化合物,其水溶液呈碱性,原因是 ,
(用离子方程式表示)。写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式 。
(2)D的单质能跟C的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式 。
(3)A、B、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 。
(4)4.0 g D单质在足量的B单质中完全燃烧,放出37 kJ热量,写出其热化学方程式:
。
(5)用A元素的单质与B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特制的防止透过的隔膜,在A极通入A的单质,B极通入B的单质,则A极是该电池的 极;B极的电极反应式是
。
9.已知一种c(H+)=1×10-3mol·L-1的酸和一种c(OH-)=1×10-3mol·L-1的碱溶液等体积混合
后溶液呈酸性,其原因可能是 ( )
A.较浓的强酸和稀的强碱溶液反应 B.较浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应 D.生成了一种强酸的碱盐
8.下列说法中正确的是 ( )
A.水是极弱的电解质,它能微弱电离生成相同物质的量的H+和OH-
B.稀溶液中c(H+)•c(OH-)=KW,任何条件下KW都保持不变
C.无论在什么条件下,中性溶液的c(H+)一定等于1×10-7 mol·L-1
D.H2O H++OH-是一吸热过程,所以温度升高,KW也随之增大
H++OH-是一吸热过程,所以温度升高,KW也随之增大
7.用水稀释0.1 mol·L-1氨水时,溶液中随着水量的增加而减小的是 ( )
A.c(OH-)/c(NH3·H2O) B.c(NH3·H2O)/(OH-)
C.c(H+)和c(OH-)的乘积 D.OH-的物质的量
6.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,这两种溶液的体积和pH都相等;再向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法正确的是( )
A.甲烧杯中放入的锌粒质量比乙烧杯中放入锌的质量大
B.甲烧杯中的酸过量
C.两烧杯中参加反应的锌等量
D.反应开始后乙烧杯中的C(H+)始终比甲烧杯中的C(H+)小
5.在容积不变的密闭容器中进行如下反应:H2O(g)+C(s) H2(g)+CO(g) △H>0达到平衡后,改变下列反应条件,相关叙述正确的是 ( )
H2(g)+CO(g) △H>0达到平衡后,改变下列反应条件,相关叙述正确的是 ( )
A.加入H2,平衡向逆反应方向移动,体系压强减小
B.加入少量C,正反应速率增大
C.降低温度,平衡向正反应方向移动
D.加入CO,混合气体的密度增大
4.关于如图装置的说法错误的是 ( )
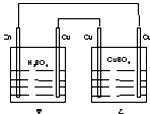
A.甲是原电池,乙是电解池
B.甲池的pH将增大
C.乙池中c(Cu2+)保持不变
D.甲池中Zn溶解的物质的量小于乙池中阳极Cu溶解的物质的量。
3.已知:H2(g)+I2(g)
= 2HI(g)的平衡常数为K1 ; 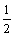 H2(g)+
H2(g)+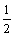 I2(g) = HI(g)的平衡常数为K2,则K1和K2的关系为 ( )
I2(g) = HI(g)的平衡常数为K2,则K1和K2的关系为 ( )
A.K1= 2K2 B.K1= K22 C.K1 = K2 D.K1=1/ K2
2.反应:A(g)+3B(g) 2C(g) △H<0。达平衡后,将气体混和物的温度降低,下列叙述中正确的是 ( )
2C(g) △H<0。达平衡后,将气体混和物的温度降低,下列叙述中正确的是 ( )
A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动
B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动
C.正反应速率和逆反应速率变小,平衡向正反应方向移动
D.正反应速率和逆反应速率变小,平衡向逆反应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com