
22.食盐是日常生活的必需品,也是重要的化工原料。
(l)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl
的流程如下:
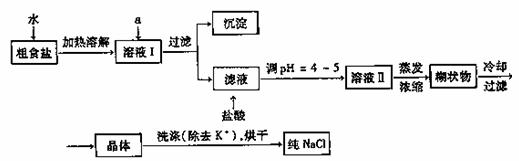
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
① 欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42- 离子,选出a所代表的试剂,按滴加顺序依次为 (只填化学式)。
② 洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为 。
(2)用提纯的NaCl配制500mL4.00mol·L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有
(填仪器名称)。
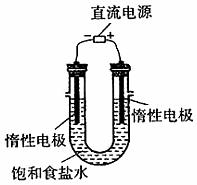
(3)电解饱和食盐水的装置如图所示,若收集的H2 为2L,则同样条件下收集的Cl2 (填“>”、“=”或“<”=2L,原因是 。
装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为
。
(4)实验室制备H2和Cl2通常采用下列反应:Zn+H2SO4 ZnSO4+H2↑
ZnSO4+H2↑
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置 (填代号)和制备并收集干燥、纯净Cl2的装置 (填代号)。
可选用制备气体的装置: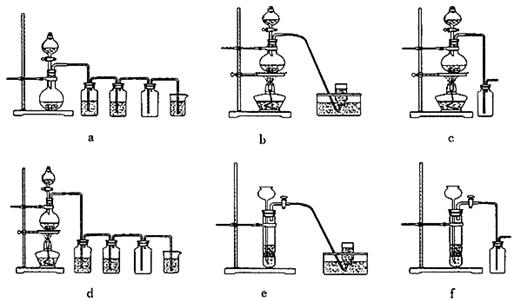
21.由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用下图所法实验装置可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
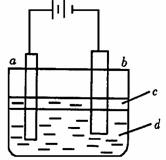
① a电极材料为_______,其电极反应式为_____。
② 电解液d可以是_______,则白色沉淀在电极上生成;也可以是_____,则白色沉淀在两极之间的溶液中生成。
A.纯水 B.NaCl 溶液
C.NaOH溶液 D.CuCl2溶液
③ 液体c为苯,其作用是________,在加入苯之前,对d溶液进行加热处理的目的是____________________。
④ 为了在短时间内看到白色沉淀,可以采取的措施是___。
A.改用稀硫酸做电解液 B.适当增大电源电压
C.适当缩小两电极间距离 D.适当降低电解液温度
⑤若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为_____。
20.采用惰性电极从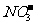 -、SO42-、
-、SO42-、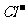 、Cu2+、Ba2+、H+中选出适当的离子组成电解质,并对其溶液进行电解(少写多写均扣分)。
、Cu2+、Ba2+、H+中选出适当的离子组成电解质,并对其溶液进行电解(少写多写均扣分)。
(1)若两极分别放出H2和O2,则电解质的化学式为 ;
(2)若阴极析出金属,阳极放出O2,则电解质的化学式为 ;
(3)若两极分别放出气体,且体积比为1:1,则电解质的化学式为 。
19.正确书写电极反应和化学方程式:
(1)铁在潮湿的空气中转变为铁锈
负极: 正极:
总反应: 氧化反应:
分解反应:
(2)向FeBr2 溶液中加入少量Cl2
向FeBr2 溶液中加入足量Cl2
18.下列实验可行的是 ( )
A.用澄清石灰水检验CO中含有的CO2
B.用BaCl2除去NaOH溶液中混有的少量Na2SO4
C.用KSCN溶液检验溶液中含有的Fe2+
D.用溶解、过滤的方法分离CaCl2和NaCl固体混合物
17.下列说法正确的是 ( )
A.不用其它试剂便无法区别NaCl、Na2CO3、NaHSO4、AlCl3四种溶液
B.实验室常用带玻璃塞的试剂瓶保存NaOH溶液
C.用导线将电解池和电池连接,电子从电池的负极流向电解池的阳极
D.用以下反应制取硫酸铜:2Cu+O2==2CuO、CuO+H2SO4=CuSO4+H2O符合绿色化学的理念
16.电解100mL含c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是 ( )
A.0.10mol/LAg+ B.0.02mol/L Zn2+ C.0.20mol/L Cu2+ D.0.20mol/L Pb2+
15.自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,会产生明显的试剂变质问题的是: ( )B
A.NaNO3 B.FeCl2 C.Na2SO4 D.AlCl3
14.下列关于铜-锌-稀硫酸构成的原电池中有关叙述中错误的是 ( )
A.铜为正极,铜不易失去电子而受到保护
B.负极发生还原反应,正极发生氧化反应
C.锌为负极,锌发生氧化反应
D.外电路中电子流入的一极为正极,电子流出的一极为负极
13.下列说法错误的是 ( )
①测定CuSO4·XH2O晶体中结晶水的含量需用蒸发皿加热;
②银镜反应实验后,粘有银的试管可用稀氨水洗涤
③向盛有少量苯酚稀溶液的试管里,滴入过量浓溴水有白色沉淀产生
④向氯化铁溶液里滴入氢氧化钠溶液可以制取氢氧化铁胶体
⑤向含有乙酸杂质的乙酸乙酯中加入氢氧化钠溶液后分液,提纯乙酸乙酯;
⑥SO2气体通入溴水,溴水褪色,说明SO2有漂白性。
A.①②④⑤ B.①②③ C.①②④⑤⑥ D.全部
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com