
32£®Čē¹ū¼ÓČČ0.04mol KMnO4¹ĢĢåŅ»¶ĪŹ±¼äŗóŹÕ¼Æµ½amolµ„ÖŹĘųĢ壬“ĖŹ±KMnO4µÄ·Ö½āĀŹĪŖx£¬ŌŚ·“Ó¦ŗóµÄ²ŠĮō¹ĢĢåÖŠ¼ÓČė¹żĮæµÄÅØHCl²¢¼ÓČČ£¬³ä·Ö·“Ó¦ŗóÓÖŹÕ¼Æµ½bmolµ„ÖŹĘųĢ壬ĒŅMnŌŖĖŲČ«²æŅŌMn2+µÄŠĪŹ½“ęŌŚÓŚ·“Ó¦ŗóµÄČÜŅŗÖŠ”£
(1)a+b=____________(ÓĆx±ķŹ¾)”£
(2)µ±x=___________Ź±£¬(a+b)µÄÖµ×īŠ”£¬ĒŅ×īŠ”ÖµĪŖ______________”£
(3)µ±a+b=0.09Ź±£¬0.04mol KMnO4¼ÓČČŗóĖłµĆ²ŠĮō¹ĢĢåµÄÖŹĮæĪŖ_________g”£
31£®Ä³Ń§ÉśĪŖĮĖ²ā¶Ø²æ·Ö±äÖŹµÄNa2SO3ѳʷµÄ“æ¶Č£¬Éč¼ĘĮĖČēĻĀŹµŃé£ŗ
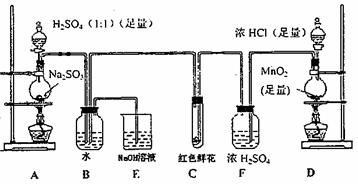
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Š“³öA×°ÖĆÖŠ²£Į§ŅĒĘ÷µÄĆū³Ę£ŗ¾Ę¾«µĘ”¢_____________”¢_____________”£
(2)ŹµŃéæŖŹ¼ŗ󣬊“³öBÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½______________________________________”£
(3)CÖŠµÄĻÖĻóŹĒ____________________£¬E×°ÖƵÄ×÷ÓĆŹĒ____________________________”£
(4)°“ĻĀĶ¼ĖłŹ¾³ĘČ”Ņ»¶ØĮæµÄNa2SO3ѳʷ·ÅČėA×°ÖƵÄÉÕĘæÖŠ£¬µĪČė×ćĮæµÄH2SO4ĶźČ«·“Ó¦”£Č»ŗó½«BÖŠĶźČ«·“Ó¦ŗóµÄČÜŅŗÓė×ćĮæµÄBaCl2ČÜŅŗ·“Ó¦£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ£¬µĆ°×É«³Įµķ23.3g£¬ŌņŌѳʷ֊Na2SO3µÄ“æ¶ČĪŖ________(¾«Č·µ½0.1%)”£
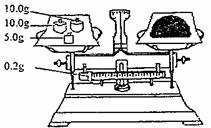
(5)ŌŚ¹żĀĖ³ĮµķŹ±Čō¹żĀĖŅŗ³öĻÖ»ė×Ē£¬Ōņ±ŲŠėŅŖÖŲø“²Ł×÷£¬ČōøĆѧɜƻӊÖŲø“¹żĀĖ£¬Ōņ²ā¶ØµÄ½į¹ū½«_______(Ģī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°ĪŽÓ°Ļģ”±)
(6)ŅŖŹ¹²ā¶Ø½į¹ū×¼Č·£¬µŚŅ»£¬×°ÖĆĘųĆÜŠŌ±ŲŠėĮ¼ŗĆ£»µŚ¶ž£¬Ó¦ĻȵćČ¼______“¦¾Ę¾«µĘ(Ģī×°ÖĆ×ÖÄø)£»µŚČż£¬_________________________________________________________”£
30£®(8·Ö)·Ņ±ŲµĆŹĒŅ»ÖÖøߊ§µÄĻūŃ×Ņ©Īļ£¬ĘäÖ÷ŅŖ³É·ÖĪŖ²¼Āå·Ņ£¬ĖüÓŠ¶ąÖÖŗĻ³ÉĀ·Ļߣ¬ĻĀĆęŹĒŅ»ÖÖŗĻ³É·½·Ø”£
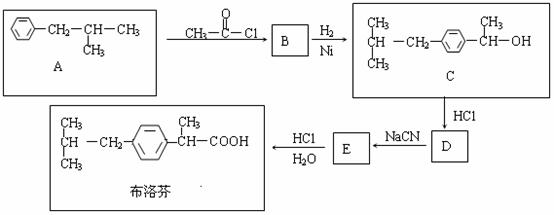
ŅŃÖŖ£ŗĀ±“śĢžÓŠČēĻĀ·“Ó¦£ŗR£Cl+NaCN ”ś R£C N+
N+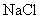 »Ų“šĻĀĮŠĪŹĢā£¬
»Ų“šĻĀĮŠĪŹĢā£¬
(1)Š“³öÓŠ»śĪļBµÄ½į¹¹¼ņŹ½£ŗ ________________________”£
(2)Š“³ö·“Ó¦A”śBŗĶB”śCµÄ·“Ó¦ĄąŠĶ_______________”¢________________(æɹ©Ń”ŌńµÄ·“Ó¦ĄąŠĶÓŠ£ŗČ”“ś£¬¼Ó³É£¬ĻūČ„£¬¼Ó¾Ū£¬Ėõ¾Ū)”£
(3)ÓŠ»śĪļCŗĶ±½·ÓµÄ¹ŲĻµŹĒ___________(Ń”Ģī×ÖÄø)
A£®»„ĪŖĶ¬·ÖŅģ¹¹Ģå”””” B£®»„ĪŖĶ¬ĻµĪļ””
C£®¾łŹōÓŚ·¼Ļć“¼Ąą”””” D£®¾łŹōÓŚ·¼Ļć×å»ÆŗĻĪļ
(4)ÓėA¾ßÓŠĻąĶ¬µÄ·Ö×ÓŹ½£¬ĒŅ±½»·ÉĻÖ»ÓŠŅ»øöČ”“ś»łµÄÓŠ»śĪļ¹²ÓŠĖÄÖÖ£¬Š“³ö³żAĶāµÄĘäӹȿÖֵĽį¹¹¼ņŹ½£ŗ_______________£»_____________________£»_____________________”£
(5)Š“³öE”ś²¼Āå·Ņ·“Ó¦µÄ»Æѧ·½³ĢŹ½(ŅŖĒóÅäĘ½£¬ÓŠ»śĪļŅŖÓĆ½į¹¹¼ņŹ½±ķŹ¾)£ŗ
________________________________________________________________________ӣ
29.(8·Ö)ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ĻņŅ»øöČŻ»ż²»±äµÄČŻĘ÷ÖŠĶØČė2molµŖĘųŗĶ8molĒāĘų¼°¹ĢĢå“߻ƼĮ£¬Ź¹Ö®·“Ó¦”£ŅŃÖŖ£ŗN2+3H2(g)
 2NH3(g);”” ”÷H=-92.2KJ/molĘ½ŗāŹ±ČŻĘ÷ÄŚĘųĢåµÄŃ¹ĒæĪŖĘšŹ¼Ź±µÄ80%”£
2NH3(g);”” ”÷H=-92.2KJ/molĘ½ŗāŹ±ČŻĘ÷ÄŚĘųĢåµÄŃ¹ĒæĪŖĘšŹ¼Ź±µÄ80%”£
(1)Ę½ŗāŹ±ČŻĘ÷ÄŚ°±ĘųµÄĢå»ż·ÖŹż¦Õ=_____________”£
(2)¼ÓČė2molµŖĘųŗĶ8molĒāĘų£¬·“Ó¦“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæĪŖ_________(ĢīŠņŗÅ)”£
A£®Š”ÓŚ92.2kJ”””””””””””” B£®µČÓŚ92.2kJ
C£®“óÓŚ92.2kJ”””””””””””” D£®æÉÄÜ“óÓŚ»ņŠ”ÓŚ»ņµČÓŚ92.2kJ
(3)ŌŚĻąĶ¬ČŻĘ÷ÖŠ£¬½µµĶĪĀ¶Č£¬ĶØČė2mol°±ĘųŗĶ1molĒāĘų¼°¹ĢĢå“߻ƼĮ£¬·“Ó¦“ļµ½Ę½ŗāŹ±°±ĘųµÄĢå»ż·ÖŹż£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ_________(ĢīŠņŗÅ)”£
A£®Ņ»¶ØµČÓŚ¦Õ”””””””””””” B£®Ņ»¶Ø“óÓŚ¦Õ””””
C£®Ņ»¶ØŠ”ÓŚ¦Õ”””””””””””” D£®æÉÄÜ“óÓŚ»ņŠ”ÓŚ»ņµČÓŚ¦Õ
(4)±£³ÖĶ¬Ņ»ĪĀ¶Č£¬ŌŚĻąĶ¬µÄČŻĘ÷ÖŠ£¬ĘšŹ¼ĶØČėŅ»¶ØĪļÖŹµÄĮæµŖĘų”¢ĒāĘų”¢°±Ęų£¬ÓūŹ¹Ę½ŗāŹ±°±ĘųµÄĢå»ż·ÖŹżŅ²ĪŖ¦Õ£¬ĒŅĘšŹ¼Ź±·“Ó¦±ķĻÖĪŖĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬Ōņ³äČėµŖĘųµÄĪļÖŹµÄĮæa(mol)µÄȔֵ·¶Ī§_______________”£
28£®(5·Ö)Č¼ĮĻµē³ŲŹĒŹ¹ĘųĢåČ¼ĮĻŃõ»ÆÖ±½Ó²śÉśµēĮ÷µÄ×°ÖĆ£¬ÕāŹĒ±¾ŹĄ¼Ķ×ī¾ßĢōÕ½ŠŌµÄæĪĢāÖ®Ņ»”£×ī½üÓŠČĖÖĘŌģĮĖŅ»ÖÖČ¼ĮĻµē³Ų£¬Ņ»øöµē¼«ĶØČėæÕĘų£¬ĮķŅ»µē¼«ĶØČė¶”Ķ飬µē³ŲµÄµē½āÖŹŹĒ²ōŌÓĮĖY2O3(ČżŃõ»Æ¶žīĘ)µÄZrO2(¶žŃõ»ÆļÆ)¾§Ģ壬ĖüŌŚøßĪĀĻĀÄÜ“«µ¼O2£”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)øƵē³Ų·ÅµēŹ±µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ___________________________________________”£
(2)øĆČ¼ĮĻµē³ŲµÄµē¼«·“Ó¦Ź½ĪŖ£ŗ
µē³ŲÕż¼« 13O2+52e£”””” 26O2£””””””
µē³Ųøŗ¼« 2C4H10+26O2££52e£”””” ””8CO2+10H2O
Ōņ¹ĢĢåµē½āÖŹÖŠµÄO2£Ļņ________¼«ŅʶÆ(Ģī”°Õż”±»ņ”°øŗ”±)
(3)ij½šŹōµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ52.00£¬ÓĆÉĻŹöµē³Ųµē½āøĆ½šŹōµÄŅ»ÖÖŗ¬ŃõĖįŃĪµÄĖįŠŌĖ®ČÜŅŗŹ±£¬Ńō¼«Ćæ·Å³ö3360mL(±ź×¼×“æö)ŃõĘų£¬Ņõ¼«Īö³ö½šŹō10.4g£¬ŌŚøĆŗ¬ŃõĖįŃĪÖŠ½šŹōµÄ»ÆŗĻ¼ŪĪŖ____£¬ŌŚøĆŹµŃéÖŠ£¬Čō²»æ¼ĀĒÄÜĮæµÄĖšŹ§£¬µē³ŲÖŠĻūŗĶ”ĶéµÄÖŹĮæ×īÉŁŹĒ________g(½į¹ū¾«Č·ÖĮ0.01g)”£
27£®(8·Ö)A”¢B”¢CĪŖ֊ѧ³£¼ūµ„ÖŹ£¬ĘäÖŠŅ»ÖÖĪŖ½šŹō£»Ķس£ĒéæöĻĀAĪŖ¹ĢĢ唢BĪŖŅŗĢ唢CĪŖĘųĢ唣D”¢E”¢F”¢G”¢H”¢X¾łĪŖ»ÆŗĻĪļ£¬ĘäÖŠXŹĒŅ»ÖÖĪŽŃõĒæĖį”¢EĪŖŗŚÉ«¹ĢĢ壬HŌŚ³£ĪĀĻĀĪŖŅŗĢ唣ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾(Ęä֊ijŠ©·“Ó¦Ģõ¼žŗĶ²æ·Ö·“Ó¦²śĪļŅŃĀŌČ„)”£
(1)Š“³öĻĀĮŠĪļÖŹµÄ»ÆѧŹ½£ŗD______________£»X______________”£
(2)ŌŚ·“Ó¦¢Ł-¢ßÖŠ£¬²»ŹōÓŚŃõ»Æ»¹Ō·“Ó¦µÄŹĒ________________(Ģī±ąŗÅ)”£
(3)·“Ó¦¢ÜµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ_________________________________________”£
(4)ĶłGČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ¹Ū²ģµ½µÄĻÖĻóŹĒ____________________________________”£
(5)·“Ó¦¢ßµÄ»Æѧ·½³ĢŹ½ĪŖ__________£»øĆ·“Ó¦ÖŠĆæĻūŗÄ0.3molµÄA£¬æÉ×ŖŅʵē×Ó_____mol”£
(6)Š“³öDµÄČÜŅŗÓėŠ”ĖÕ“ņČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______”” _”£
26£®(5·Ö)¶ĢÖÜĘŚµÄĮłÖÖŌŖĖŲA”¢B”¢C”¢X”¢Y”¢Z£¬Ō×ÓŠņŹżŅĄ“Ī±äŠ”£¬ĘäÖŠX”¢Y”¢ZŌ×ÓŗĖĶāµē×Ó²ćŹżÖ®ŗĶŹĒ5”£XŌŖĖŲŌ×Ó×īĶāµē×Ó²ćÉĻµÄµē×ÓŹżŹĒYŗĶZĮ½ŌŖĖŲŌ×Ó×īĶāµē×Ó²ćÉĻµÄµē×ÓŹżµÄ×ÜŗĶ£»YŌŖĖŲŌ×ÓµÄ×īĶāµē×Ó²ćÉĻµÄµē×ÓŹżŹĒĖüµÄµē×Ó²ćŹżµÄ2±¶£¬XŗĶZæÉŅŌŠĪ³É10µē×Ó»ÆŗĻĪļQ£»CÓėX“¦ÓŚĶ¬ÖÜĘŚ£¬B+ÓėC2-µÄŗĖĶāµē×ÓÅŲ¼ĻąĶ¬£¬AÓėB“¦ÓŚĶ¬ÖÜĘŚ£¬ĒŅŠĪ³ÉBAŠĶ»ÆŗĻĪļ”£Ēė»Ų“š£ŗ
(1)»ÆŗĻĪļQµÄæռ乹ŠĶĪŖ_______________£»»ÆŗĻĪļYC2µē×ÓŹ½ŹĒ________________£»
(2)A”¢B”¢CµÄĄė×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖ____________________(ÓĆŌŖĖŲĄė×Ó·ūŗűķŹ¾)£»
(3)ŌŖĖŲ×é³ÉĪŖXZ5YC3ŗĶBCZ(×ćĮæ)»ÆŗĻĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________________£»
(4)¹¤ŅµÉĻ£¬ČōŹäĖĶŌŖĖŲAµÄµ„ÖŹµÄ¹ÜµĄĀ©Ęų£¬ÓĆQ½ųŠŠ¼ģŃ鏱æɹŪ²ģµ½“óĮæ°×ŃĢ£¬Ķ¬Ź±ÓŠXµÄµ„ÖŹÉś³É£¬Š“³öÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½_______________________________________”£
25£®ÓŠŃõ»ÆĶŗĶČżŃõ»Æ¶žĢśµÄ»ģŗĻĪļag£¬¼ÓČė2mol/LµÄHClČÜŅŗ50mL£¬Ē”ŗĆĶźČ«Čܽā£¬Čō½«2agøĆ»ģŗĻĪļŌŚCOĘųĮ÷ÖŠ¼ÓČČ²¢³ä·Ö·“Ó¦£¬ĄäČ“ŗó£¬Ź£Óą¹ĢĢåµÄÖŹĮæĪŖ(”” )
”””” A£®(2a£1.6)g”””””””””””” B£®(2a£3.2)g”””””””””””” C£®1.6ag”””””””””””””” D£®0.8ag
24£®½«ČÜŅŗ(»ņĘųĢå)XÖš½„¼ÓČė(»ņĶØČė)µ½Ņ»¶ØĮæYČÜŅŗÖŠ£¬²śÉś³ĮµķµÄÖŹĮæÓė¼ÓČėXµÄĪļÖŹµÄĮæ¹ŲĻµČēĻĀĶ¼£¬·ūŗĻĶ¼ÖŠĒéæöµÄŅ»×éĪļÖŹŹĒ(”” )
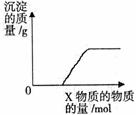
|
”” |
A |
B |
C |
D |
|
X |
Ba(HCO3)2 ČÜŅŗ |
Na2CO3 ČÜŅŗ |
KOH ČÜŅŗ |
CO2 ĘųĢå |
|
Y |
NaOH ČÜŅŗ |
CaCl2 ČÜŅŗ |
Mg(HSO4)2 ČÜŅŗ |
ŹÆ»ŅĖ® |
23£®ŅŌĢśĪŖŃō¼«£¬ĶĪŖŅõ¼«£¬¶Ō×ćĮæµÄNaOHČÜŅŗ½ųŠŠµē½ā”£Ņ»¶ĪŹ±¼äŗóµĆµ½2molFe(OH)3³Įµķ£¬“Ė¼ä¹²ĻūŗÄĖ®µÄĪļÖŹµÄĮæĪŖ(”” )
A£®2mol”””” ”””””””””””””” B£®3mol”””””” ”””””””””””””” C£®4mol ”””””””””””””” D£®5mol
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com