
7.下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是 ( )
A. 、
、 、
、 、
、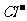 B.
B. 、
、 、
、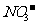 、
、
C. 、
、 、
、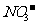 、
、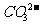 D.
D. 、
、 、
、 、
、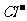
6.下列分子中所有原子都满足最外层8电子结构的是 ( )
A. B.
B. C.
C. D.
D.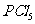
25.(7分)我国锑(Sb)的蕴藏量世界第一。提取锑的方法第一步:高温条件下Sb2S3与O2和Fe反应,得到Sb4O6与FeS;第二步:高温条件下用碳还原Sb4O6得到单质锑。
(1)第一步的化学反应方程式是 ;氧化剂是 氧化产物是 。
(2)用400吨含Sb2S385%的矿石,理论上可以冶炼得到多少吨单质锑?
24.(12分)某有机物X是农药生产中的一种中间体,其结构简式为(如下图)

(1)X的分子式为
(2)X分子中含有的官能团有 (用结构简式表示)
(3)X可能发生多种反应,下列有关X发生化学反应的叙述中正确的是( )(多选扣分)
A.在氢氧化钠醇溶液中共热能发生消去反应
B.在铜作催化剂时加热,可被氧气氧化生成能发生银镜反应的物质
C.在深硫酸存在时加热可发生消去反应
D.在铁作催化剂时,可跟液溴发生取代反应
(4)写出X跟足量氢氧化钠稀溶液共热时所发生反应的化学方程式 。
(5)X可能有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式 。
①苯环只有分处在对位的两个取代基
②遇氯化铁溶液不变色,但遇pH试纸显红色
23.(12分)实验室进行某项实验的装置如下图.
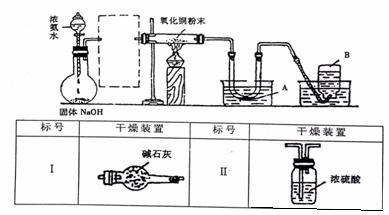
实验现象记录如下:
①黑色的氧化铜粉末变为光亮的红色;
②生成物A能使无水硫酸铜粉末变蓝色;
③镁带能在另一种生成物B中燃烧生成一种固态物质C,C与A起反应生成碱性物质D和一种能使湿润的红色石蕊试纸变蓝的气体E:已知B中原子均达到8电子稳定构型
回答以下问题:
(1)虚线方框内应选的干燥装置是 (填标号)
(2)A的分子式为 ;B的分子式为 .
(3)在制氨的装置中,固体NaOH的作用是 .
(4)写出下列反应的化学方程式:
①氨与灼热氧化铜的反应 . ②C与A的反应 .
22.(19分)Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,Q的最外层电子数是次外层的两倍,R与Q同族,Y与Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固体属于 晶体,俗名叫 。
(2)R在同期表中的位置是 。R与Q的最高价氧化物熔点高的是 (填化学式)
(3)Q分别与Y、Z形成的共价化合物的化学式是 和 ;Y与Z的离子半径的大小r(Y离子) r(Z离子),(填“>”“<”“=”);Q与Y形成的分子的电子式是 ,属于 分子(填“极性”或“非极性”)。
(4)X的常见氢化物的空间构型是 ;X的氢化物与最高价氧化物对应的水化物能发性反应生成盐,离子方程式为 。
(5)工业上利用R的最高价氧化物与单质Q在高温条件下反应制备单质R,化学方程式是 。
(6)常温常压下,24gQ在氧气中燃烧生成其低价氧化物放出221kJ的热量,该反应的热化学方程式是 。
21.20g由两种金属粉末组成的混合物,与足量的盐酸充分反应后得到11.2L氢气(标准状况),这种金属混合物的组成可能是 ( )
A.Mg和Al B.Al和Fe C.Fe和Zn D.Zn和Cu
|
20.用一定物质的量浓度的NaOH溶液,使相同体积的FeSO4溶液和Fe2(SO4)3溶液中的
Fe2+、Fe3+完全沉淀,如果所用的NaOH溶液的体积相同,FeSO4溶液和Fe2(SO4)3
溶液的物质的量浓度之比为 ( )
A.1:1 B.1:3 C.3:1 D.3:2
19.香兰素的结构简式如下图所示,它有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料。下列关于香兰素的判断不正确的是( )
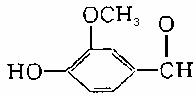
A.可与银氨溶液反应
B.可与氢氧化钠溶液反应
C.分子中所有原子都在同一平面上
D.可与浓溴水发生取代反应
18.如下图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是 ( )

①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
②Y的氢化物沸点比它上一周期同族元素的氢化物沸点低
③Z的单质在常温下是液体
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A.①②③④ B.①②③④⑤ C.只有③ D.只有①④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com