
4.“善待地球-科学发展,构建和谐”是“世界地球日”的主题。你认为下列行为不符合这一主题的是 ( )
A.控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源
B.开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料
C.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展
D.实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle)
3.“嫦娥一号”月球探测卫星在西昌卫星发射中心由“长征三号甲”运载火箭发射升空。卫星发射后,经过调相轨道段、地月转移轨道段和环月轨道段飞行,已经开始成功执行科学探测任务。“长征三号甲”运载火箭的第一、二级发动机的燃料为偏二甲肼(C2N2H8),四氧化二氮(N2O4)为氧化剂,发生的化学反应是:C2N2H8+2N2O4=2CO2+4H2O+3N2+Q(Q>0)。以下说法正确的是( )
A.上述反应中生成的N2是火箭燃料燃烧后的氧化产物
B.推动火箭飞行的强大动力源于该反应瞬间产生的大量高温气体
C.火箭发射时看到的红棕色气体是火箭起飞后,保险活动门自动开启,排出部分高压氧化剂在空气中氧化的结果
D.从能量变化上看,上述反应是热能转化为动能
2.已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)  =-820KJ·mol-1。则下列说法中正确的是
( )
=-820KJ·mol-1。则下列说法中正确的是
( )
A.反应过程中的能量变化关系可如下图所示

B.11.2LCH4完全燃烧放出热量410KJ
C.CH4的燃烧热为820KJ
D.凡是有水生成的氧化还原反应都是放热反应
1.下列说法正确的是 ( )
A.反应热是指反应过程中放出的热量
B.1molH2SO4和1molBa(OH)2完全中和所放出的热量为中和热
C.相同条件下,将两份碳燃烧,生成CO2的反应比生成CO的反应放出的热量多
D.物质发生化学变化都伴随着能量变化
32.(12分)现有NaOH和NaHCO3固体混合物0.2 mol, 在密闭容器中加热到250℃,使其充分反应后,排出气体,冷却,称得残留固体质量为W g.
(1)写出可能发生反应的化学方程式.
(2)设混合物中NaOH为x mol(0<x<0.2).当x取不同值时,推断残留物质的种类,并计算W的数值(可以用含有“x”的代数式表示).请填表回答:
|
_ X值 |
残留固体(化学式) |
W值(g) |
|
X=0.1 |
|
|
|
0<x<0.1 |
|
|
|
0.1<x<O.2 |
|
|
(3)在下面坐标中,画出w值随x值变化的曲线.

31.(12分)A、B、C三种物质均属于同一种金属的化合物.用铂丝蘸取A、B、C三种物质的溶液,在无色火焰上灼烧,均呈浅紫色.已知:A与B反应生成C;加热B得到 D;D与A的水溶液反应生成B或生成C;B可与酸和碱反应;D是一种无色、无味的气体.
(1)A是 , B是 ,
C是 ,D是 .
(2)写出下列反应的离子方程式: :
A+B
B+HCl
A-B
A-C
29(6分)欲用98%的浓硫酸(ρ=1.84g/cm)配制成浓度为0.5mol/L的稀硫酸500mL。
(1)主要仪器有:量筒、烧杯、玻璃棒、 、 。
(2)简要回答下列问题:
①所需浓硫酸的体积为 ;
②如果实验室有15mL、20mL、50mL的量筒应选用 mL的量筒最好。
③在转入容量瓶前烧杯中液体应冷却至室温,否则会使结果浓度偏 。(填“高”、“低”、下同)
④定容时必须使溶液的凹液面的最低点与刻度相平,若俯视会使结果浓度偏
30.(14分)某课外活动小组欲制取次氯酸钠和氯化钠的混合溶液,为提高次氯酸钠含量,用如下图所示装置。 图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸。(据资料显示:C12与NaOH在不同温度下,产物不同。在较高温度下易生成NaClO3) 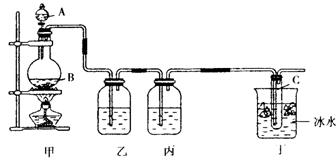
试回答:
(1)烧瓶B中盛 ,试管C中盛 。
(2)有同学认为可以省去某些装置,你认为怎样:
①能否省去乙装置 (填“能”或“不能”),理由是
②能否省去丙装置 (填“能”或“不能”),理由是 。
(3)有同学认为还必须加入某些装置,你认为怎样? (填“需要”或“不需要”),如果你认为需要,请指出该装置的作用是 。
(4)丁装置中冰水的作用是 。
28.下列说法正确的是 ( )
A.需要加热才能发生的反应一定是吸热反应
B.放热的反应在常温下一定很容易发生
C.是放热还是吸热反应必须看反应物和生成物具有的总能量的相对大小
D.吸热反应在通常条件下一定不能发生
II卷(非选择题 共44分 请将答案写在答题纸上)
27.化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2=2HCl推测:H2+Br2=2HBr。但类比是相对的,如根据2Na2O2+2CO2= Na2CO3+ O2, 类推2Na2O2+2SO2= Na2SO3+ O2是错误的,应该是Na2O2+SO2= Na2SO4。 下列各组类比中正确的是 ( )
A.由NH4Cl NH3↑+HCl↑,推测:NH4I
NH3↑+HCl↑,推测:NH4I NH3↑+HI↑
NH3↑+HI↑
B.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推测:2SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO
C.由2CO2+Ca(ClO)2+2H2O=Ca(HCO3)2+2HClO,推测:O2+NaClO+H2O=NaHCO3+HClO
D.由Na2SO3+2HCl=2NaCl+H2O+ SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+ SO2↑
26.下列化合物中,只能在溶液中才能导电的电解质是 ( )
A.NaCl B.H2SO4 C.NH3 D.CaO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com