
17.(10分)某化学兴趣小组利用饱和氯水与石灰石的反应,制取较浓的HClO溶液,并对所得溶液中的部分阴离子进行检验。
|
|
实验操作 |
实验现象 |
|
步骤l |
在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,过滤,将滤液分为若干份 |
有少量气泡产生,溶液的黄绿色褪去 |
|
步骤2 |
将第一份滤液与稀盐酸混合 |
产生大量气泡 |
|
步骤3 |
将第二份滤液加热 |
溶液变浑浊,且有大量无色气体产生 |
(1)步骤l过滤的目的是 。
(2)步骤2、步骤3的实验目的都是 ;为达到该实验目的,还可以采取的方法是 。
(3)请你设计一个简单的实验方案,证明步骤l所得滤液中的HClO浓度比饱和氯水中HCl浓度大: 。
16.某温度下。在容积固定不变的密闭容器中发生下列可逆反应:、X(g)+2Y(g) 2Z(g),平衡时,X、Y、Z的物质的量分别为l mol、1mol、2tmol,保持温度不变,再向容器中分别充人l mol、1 mol l、2mol的X、Y、Z,则下列叙述中正确的是
2Z(g),平衡时,X、Y、Z的物质的量分别为l mol、1mol、2tmol,保持温度不变,再向容器中分别充人l mol、1 mol l、2mol的X、Y、Z,则下列叙述中正确的是
A.刚充人时,反应速率 (正)减小,
(正)减小, (逆)增大
(逆)增大
B.达到新平衡时,容器内气体的百分组成和原来相同
C.达到新平衡时,容器内气体的压强是原来的两倍
D.达到新平衡时,容器内气体的密度是原来的两倍
15.铜的冶炼大致可分为:
(1)富集:将硫化物矿进行浮选;
(2)焙烧:主要反应为:2CuFeS2+4O2====Cu2S+3SO2+2FeO(炉渣)
(3)制粗铜:在1200℃下发生的主要反应为:2Cu2S+3O2====2Cu2O+2SO2;
2Cu2O+Cu2S====6Cu+SO2↑
(4)电解精炼。
下列说法正确的是
A.上述灼烧过程的尾气均可直接排入空气
B.由6 mol CuFeS2生成6 mol Cu,反应共消耗15 mol O2
C.反应2Cu2O+ Cu2S====6Cu+SO2↑中,氧化剂只有Cu2O
D.电解精炼时,粗铜应与外电源正极相连
14.阿伏加德罗常数约为 。下列叙述中正确的是
。下列叙述中正确的是
A.1L 的FeCl3溶液中,Fe3+的数目约为6.02×1022
的FeCl3溶液中,Fe3+的数目约为6.02×1022
B.在标准状况下,2.24 L的CCl4中含有C-Cl键的数目约为0.4×6.02×1023
C.7.89 Na2O2中含有的阴离子数目约为6.02×1022
D.0.1 mol NH2离子中所含的电子数约为6.02×1023
13.下列各组物质,只用水作溶剂,就能鉴别的是
A.四氯化碳、甲苯、乙醛三种液体
B.NaCl、Na2O2、Na2CO3三种固体
B.BaSO4、NaHCO3、CaCO3三种白色粉末
D.BaSO4、Mg3N2、Al2S3三种固体
12.痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中的一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上。如果将溶液①小心地涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线。用下列化学式表示这3种物质都正确的是
A.①AgNO3 ②NaBr ③AgBr
B.①AgNO3 ②NaCl ③AgCl
C.①AgCl ②AgNO3 ③NaCl
D.①AgNO3 ②NaI ③AgI
11.下列叙述中不正确的是
A.电解池的阳极上发生氧化反应,阴极上发生还原反应
B.原电池跟电解池连接后,电子从电池负极流向电解池阳极
C.电镀时,电镀池里的阳极材料发生氧化作用
D.电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气
10.下列反应的离子方程式正确的是
A.氯化铝溶液中加入过量氨水:
B.氨气通人醋酸溶液中: 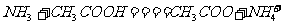
C.澄清石灰水中通入过量二氧化碳: 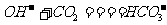
D.硫酸铜溶液中加入过量氢氧化钡溶液: 
9.下面有关pH的说法正确的是
A.在pH=12的溶液中.水电离出的 定等于
定等于
B.将pH=2和pH=l2的酸碱溶液等体积混合后,溶液的pH一定等于7
C.若强酸、强碱中和后pH=7,则中和之前酸、碱的pH之和一定等于14
D.含等物质的量的HNO3、Na2CO3、CH3COOH的溶液混合后。溶液的pH一定大于7
8.进行下列实验肯定不能获得成功的是
A.用pH试纸鉴别浓硫酸与浓硝酸
B.用硝酸银溶液区分二氧化氮和溴蒸气
C.用酸性高锰酸钾溶液除去二氧化碳中混有的少量二氧化硫
D.用溴水除去苯中溶有的少量苯酚
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com