
17.(10分)A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如下图所示(图中部分产物未列出):

请填写下列空白
(1)A是 ,G的电子式 。
(2)H与盐酸反应生成E的离子方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D的离子方程式是 。
16.2LN2和CH4的混合气体与4LO2点燃充分反应后,用干燥剂除去水分,剩余气体的体积5L。原来混合气体中N2和CH4的物质的量之比(各气体体积都在相同的温度、压强下测定)为 ( )
A.1:3 B.1:1 C.2:1 D.3:1
第Ⅱ卷(非选择题 共52分)
15.下列叙述中指定粒子的数目大于6.02×1023的是 ( )
A.2g重水(D2O)中含有的中子数
B.0.1 mol F-中含有的电子数
C.标准状况下,11.25LN2和NO混合气体中的原子数
D.1L1 mol/Lna2SO4溶液中的Na+数
14.在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2↑中,若有5molH2O参加反应,则被水还原的BrF3的物质的量为 ( )
A.3mol B. mol C.
mol C.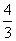 mol D.2 mol
mol D.2 mol
13.中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是( )
A.用反应物、产物中键能数据可判断对应反应的热效应
B.用沸点数据推测将一些液体混合物用分镏的方法分离开来的可能性
C.有反应热数据的大小判断不同反应的反应速率的快慢
D.用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性的强弱
12.在一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后,恢复到原来的温度,下列说法中正确的是 ( )
A.溶液的pH不变,有H2放出
B.溶液的pH值增大,有O2放出
C.溶液中c(Na+)增大,有O2放出
D.溶液中Na+数目减少,有O2放出
11.用NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.0.1mol/L稀硫酸100mL中含有硫酸根个数为0.1NA
B.1molCH3+(碳正离子)中含有电子数10NA
C.2.4g金属镁与足量的盐酸反应,转移电子数为2NA
D.12.4g白磷中含有磷原子数为0.4NA
10.有一无色溶液,可能含有K+、Al3+、NH4+、Mg2+、Cl-、SO42-、HCO3-、MnO4–中的一种或几种。为确定其成分,做如下实验:(1)取部分溶液,加入适量Na2O2固体、产生无色无味的气体并生成白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;(2)另取部分原溶液,加入HNO3酸化的Ba(NO3)2有白色沉淀产生。下列推断正确的是( )
A.肯定有K+、HCO3-、MnO4– B.肯定有Al3+、Mg2+、HCO3-
C.肯定有Al3+、Mg2+、SO42-、Cl- D.肯定有Al3+、Mg2+、SO42-
9.在含有NaI、Na2SO3和FeBr2各1mol的溶液中通入足量的Cl2,将溶液在空气中加热蒸干并充分灼烧,最终得到剩余的固体物质是 ( )
A.NaCl、FeCl3、Na2SO4、I2 B.NaCl、FeBr3、Na2SO4
C.NaCl、Fe2O3、Na2SO4 D.NaBr、FeCl3
8.下列离子方程式中书写正确的是 ( )
A.在碳酸氢按稀溶液中加入足量的氢氧化钠稀溶液
NH4++H++2OH-=NH3·H2O+H2O
B.等物质的量浓度、等体积的氢氧化钡溶液与硫酸溶液混合Ba2++SO42-‑=BaSO4↓
C.氯化铁溶液中通入碘化氢气体 2Fe3++2I-=2Fe2++I2
D.稀硝酸除银镜 Ag+2H++NO3-=Ag++NO2↑+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com