
1.化工生产必须在遵循科学原理、实现某个反应的基础上,着重考虑综合经济效益。从硫酸工业遵循的科学原理和综合经济效益分析,下列说法不正确的是
A.硫酸厂不应建在人口稠密的居民区和环保要求高的地区
B.硫酸厂靠近原料产地比靠近硫酸消费中心更为有利
C.硫酸厂生产过程中的污水,含有硫酸等杂质,可用石灰乳中和处理
D.可利用硫酸厂生产过程中产生的“废热”来供热和发电
25.(10分)某研究性学习小组拟用铜屑、氧化铜的混合物与硫酸、硝酸组成的混酸反应制取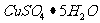 晶体。混酸中硝酸的还原产物为NO,反应过程中不产生
晶体。混酸中硝酸的还原产物为NO,反应过程中不产生 ,反应后的溶液中不含有
,反应后的溶液中不含有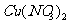 ,反应中固体完全溶解,两种酸恰好完全反应。设固体混合物的总质量为240g,其中氧化铜的质量分数为x,试回答下列问题:
,反应中固体完全溶解,两种酸恰好完全反应。设固体混合物的总质量为240g,其中氧化铜的质量分数为x,试回答下列问题:
(1)所得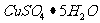 晶体的质量y的表达式为 g(用x表示)。
晶体的质量y的表达式为 g(用x表示)。
(2)若要保证固体全部溶解,混酸恰好反应,则混酸中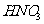 、
、 的物质的量浓度之比A的取值范围为 。
的物质的量浓度之比A的取值范围为 。
(3)若 ,反应结束时将所得气体在NaOH溶液中全部转化为
,反应结束时将所得气体在NaOH溶液中全部转化为 ,至少需要30%的双氧水多少克?
,至少需要30%的双氧水多少克?
24.(8分)为测定某固体物质中 的质量分数,现在用
的质量分数,现在用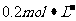
 溶液滴定含1g样品的溶液(使样品中的氯化物与硝酸银恰好完全反应)。
溶液滴定含1g样品的溶液(使样品中的氯化物与硝酸银恰好完全反应)。
(1)若消耗 溶液V mL,计算样品中
溶液V mL,计算样品中 的质量分数。
的质量分数。
(2)如果为了省去计算过程,当所取的样品质量为某一数据时,可使滴定中所消耗的 溶液毫升数等于样品中
溶液毫升数等于样品中 的质量分数a%中的a,应称取的样品的质量为 。
的质量分数a%中的a,应称取的样品的质量为 。
23.(10分)已知①卤代烃(如 )可以和金属反应生成烃基金属有机化合物。后者又能与含羰基的化合物反应生成醇:
)可以和金属反应生成烃基金属有机化合物。后者又能与含羰基的化合物反应生成醇:
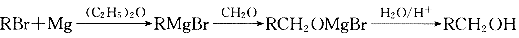
②有机酸和 反应可以得到羧酸的衍生物酰卤:
反应可以得到羧酸的衍生物酰卤:
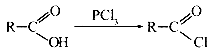
③苯在 催化下能与卤代烃作用生成烃基苯:
催化下能与卤代烃作用生成烃基苯:

分子式同为 的两种有机物A、B,都可经上述反应合成,并都能与钠反应放出氢气,但两者都不能从羰基化合物直接加氢还原得到。A、B分别与硫酸共热,前者可得到C和
的两种有机物A、B,都可经上述反应合成,并都能与钠反应放出氢气,但两者都不能从羰基化合物直接加氢还原得到。A、B分别与硫酸共热,前者可得到C和 ,而后者得到D和
,而后者得到D和 。C、D分子中所有碳原子均可共处于同一平面上,而
。C、D分子中所有碳原子均可共处于同一平面上,而 和
和 却不可。以最基础的石油产品(乙烯、丙烯、丙烷、苯等)并任选无机试剂为原料依下图所示路线可以合成B。
却不可。以最基础的石油产品(乙烯、丙烯、丙烷、苯等)并任选无机试剂为原料依下图所示路线可以合成B。

请回答以下问题:
(1)写出A、B、 、D的结构简式及2、6所代表的物质的结构筒式。A ;
、D的结构简式及2、6所代表的物质的结构筒式。A ;
B ; ;D ;2 ;6 。
;D ;2 ;6 。
(2)写出下列转化的化学方程式:
8→9
22.(8分)某烃的含氧衍生物A的相对分子质量为240,其碳的质量分数为80.0%,氧的质量分数是氢的质量分数的2倍,分子中含有2个苯环,每个苯环上都只有一个取代基,且该取代基无支链。A在稀酸溶液中加热时发生水解反应,得到B和C,C的相对分子质量为108。
请回答下列问题:
(1)A的分子式为 ,C的结构简式为 。
(2)B有多种同分异构体,请按要求回答下列问题:
①B的同分异构体中,苯环上只有一个取代基的羟基醛有 种;
②D为B的同分异构体,属于酯,且苯环上的一氯取代物有两种,分子内只含一个甲基。请写出D的一种结构简式 。
21.(10分)随着经济的发展和人民生活水平的提高,近年来我省汽车拥有量呈较快增长趋势。
(1)乙丙橡胶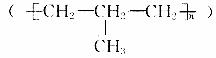 因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是 。
因柔韧性好而被用于制造汽车门窗密封胶条,工业生产乙丙橡胶的单体是 。
(2)金属防护对汽车工业具有重要意义。铝的阳极氧化是一种常用的金属表面处理技术.它能使铝的表面生成一层致密的氧化铝薄膜,该氧化膜不溶于电解时使用的电解液一稀硫酸。写出该过程阳极反应的电极反应式: 。

(3)在发动机和三i元催化转化器问的尾气流中安装一个称为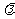 探测器的电化学元件,可测定
探测器的电化学元件,可测定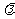 (
(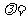 人口处的空气量/完全燃烧需要的空气量)值,如下图所示。当汽车速度增加时,入口处的空气量增大,此时排出尾气中的主要污染物是
。在转化器的前半部,一氧化碳和氮氧化物(
人口处的空气量/完全燃烧需要的空气量)值,如下图所示。当汽车速度增加时,入口处的空气量增大,此时排出尾气中的主要污染物是
。在转化器的前半部,一氧化碳和氮氧化物( )通过催化剂发生反应转化为无污染的气体,其反应的化学方程式为
。为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。已知:甲醇燃烧热为726kJ/mol。请写出甲醇燃烧的热化学方程式: 。
)通过催化剂发生反应转化为无污染的气体,其反应的化学方程式为
。为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。已知:甲醇燃烧热为726kJ/mol。请写出甲醇燃烧的热化学方程式: 。
20.(10分)化合物A、B的水溶液及其产物发生的一系列反应如下图所示(反应条件及生成的水均已略去)。其中D、X为固体。E、G常温下为气体,I、J含有相同的阳离子。

(1)写出化学式:A ,G ,H 。
(2)写出离子方程式:
反应①
反应⑤
19.(8分)移动电话是利用微波数字通信实现语言通信的通信工具。近年来,中国移动电话用户的增长速度令世人瞩目。移动电话的电池主要有镍镉电池和锂电池,镍镉电池的总化学反应可以表示为:Cd+2NiO(OH)+2H2O 2Ni(OH)2+ Cd(OH)2。电池放电时,其正极反应为 ,电池充电时,其阴极周围溶液的pH不断 (填“减小”或“增大”)。锂电池的负极材料是可插入锂的碳材料,本身就是离子、电子混合导体,正极材料是过渡金属氧化物(例如
2Ni(OH)2+ Cd(OH)2。电池放电时,其正极反应为 ,电池充电时,其阴极周围溶液的pH不断 (填“减小”或“增大”)。锂电池的负极材料是可插入锂的碳材料,本身就是离子、电子混合导体,正极材料是过渡金属氧化物(例如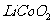 )混以一定量的导电添加物构成的混合导体,电解质溶液为可传导锂离子的有机溶剂。锂电池负极的电极反应式是 ,该电池具有很大能量密度的原因是 ;该电池的电解液使用有机溶剂的原因是 ;将
)混以一定量的导电添加物构成的混合导体,电解质溶液为可传导锂离子的有机溶剂。锂电池负极的电极反应式是 ,该电池具有很大能量密度的原因是 ;该电池的电解液使用有机溶剂的原因是 ;将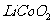 改写为氧化物的形式为 。
改写为氧化物的形式为 。
18.(12分)下图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未i面出)。图中:A为无水乙醇(沸点为78℃,B为螺旋状的细铜丝,C为无水 粉末,D为碱石灰,F为新制的碱性
粉末,D为碱石灰,F为新制的碱性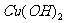 悬浊液。
悬浊液。

(1)在上述装置中,实验时需要加热的仪器有(填仪器某部位的代号) ,E处是一种纯净物,其发生反应的化学方程式为 。
(2)为使A中乙醇平稳地汽化成乙醇蒸气,可采取的措施是 。D处使用碱石灰的作用是
(3)能证明乙醇的反应产物的实验现象是 。
(4)本实验中若不加热E处,其他操作不变,则发现C处无明显变化,而F处现象与(3)相同,推断B处发生反应的化学方程式 。
17.(10分)有一瓶无色透明溶液A中,可能含有 、
、 、
、 、
、 、
、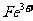 和
和 、
、 、
、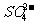 中的某些离子,在试管中各放人1mLA溶液进行实验,其实验操作、现象或结果如下表所示
中的某些离子,在试管中各放人1mLA溶液进行实验,其实验操作、现象或结果如下表所示
|
实验过程 |
现象或结论 |
|
在第l支试管中加入浓盐酸 |
没有沉淀,放出无色无刺激性气味的气体 |
|
在第2支试管中滴人NaOH溶液.共热 |
没有沉淀,放出尢色有刺激性气味的气体 |
在第3支试管中加入过量 溶液 溶液 |
析出l.487g白色沉淀 |
|
将滤出的沉淀放入盐酸中 |
沉淀量减少,放出无色无刺激性气味的气体(若将该气体全部通入过量澄清石灰水中,可析出0.4g沉淀) |
(1)A溶液中肯定含有的离子是
(2)不能肯定A溶液中是否含有的离子是 。
(3)A溶液中含有阴离子的物质的量浓度分别为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com