
10.下列说法正确的是 ( )
A.含有金属元素的化合物一定是离子化合物
B.ⅠA族和ⅦA族原子化合时,一定生成离子键
C.由非金属元素形成的化合物一定是共价化合物
D.活泼金属与非金属化合时,能形成离子键
9.下列各组物质性质的比较中,错误的是 ( )
A.氧化性:Cs+<K+<Na+<Mg2+ B.酸性:H2CO3<H3PO4<H2SO4<HClO4
C.半径:K+>Na+>O2->F- D.热稳定性:SiH4<NH3<H2O<HF
8.两个体积相同的容器,一个盛有NO,另一个盛有N2和O2(N2和O2间未发生化学反应)。在同温同压下,两容器内的气体一定具有相同的 ( )
A.原子总数 B.质子总数 C.中子总数 D.质量
7.苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有 ( )
A.氧化牲 B.还原性 C.碱性 D.酸性
6.硼有两种天然同位素 、
、 ,硼元素的相对原子质量为10.80,则对硼元素中的
,硼元素的相对原子质量为10.80,则对硼元素中的 质量百分比含量的判断正确的是 ( )
质量百分比含量的判断正确的是 ( )
A.20% B.略大于20 C.略小于20% D.80%
5.已知HIO既能和酸,又能和碱发生中和反应,则它与盐酸反应的产物是
A.IO- B.H2O C.HI D.ICl
4.将4.6g金属钠投入到95.4g水中,所得溶液中溶质的质量分数 ( )
A.等于4.6% B.等于8% C.小于8% D.大于8%
3.跟100mL 0.1mol·L-1(NH4)2SO4溶液中的NH4+ 浓度相同的是 ( )
A.0.1mol·L-1 NH4NO3溶液100mL B.0.2mol·L-1氨水溶液100mL
C.0.2mol·L-1 NH4Cl溶液200mL D.0.2mol·L-1(NH4)2SO4溶液50 mL
2.据最新报道,放射性同位素钬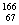 Ho可有效地治疗肝癌。该同位素原子核内的中子数与核外电子数之差是 ( )
Ho可有效地治疗肝癌。该同位素原子核内的中子数与核外电子数之差是 ( )
A.32 B.67 C.99 D.166
1.为维持人体内电解质平衡,人在大量出汗后应及时补充的离子是 ( )
A.Mg2+ B.Ca2+ C.Na+ D.Fe3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com