
4.化学用语是学习化学的重要工具。下列化学用语中,正确的是 ( )
A.硫离子的电子排布式:1s22s22p63s23p6
B.钠离子的电子式: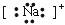
C.次氯酸的结构式:H-Cl-O
D.丙烷的分子式:CH3CH2CH3
3.下列四种微粒中,能使水电离出来的氢离子浓度等于10-8 mol/L的是 ( )
A.NH4+ B.Al3+ C.H+ D.K+
2.下列说法正确的是 ( )
A.乙酸、蔗糖都是弱电解质 B.CO2、H2O都是非极性分子
C.C6H6O、C7H8O一定互为同系物 D.食盐、金属钠、干冰的熔点依次降低
1.不同元素的原子间的共价键称极性共价键。下列固体熔化时必须破坏极性共价键的是( )
A.干冰 B.晶体硅 C.碘片 D.石英
24.向铜片中加入某浓度的硫酸120mL,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500mL,再加入足量锌粉,使之充分反应收集到标准状况下氢气2.24 L,过滤残留固体,干燥后称量,质量减轻了7.5 g。
(1)求溶解的铜的质量。
(2)求原硫酸的物质的量浓度。
23.(9分)某课外学习小组的同学设计了如图的装置,以验证SO2的氧化性、还原性和漂白性。回答以下问题:

(1)用Na2SO3固体和硫酸溶液制取SO2气体,应选用__________(选“A”或“C”)做气体发生装置,不选用另一装置的理由是 。
小组同学发现产生气体的速率缓慢,可能的原因是 。
(2)课外学习小组的同学用FeS固体和稀硫酸制取H2S气体,
反应的方程式为 ____ 。
(3)SO2气体通过D装置时现象是 ,
通过E装置时现象是 ;
SO2与H2S在B装置中反应,现象是_______________________________。
(4)F中盛有碱石灰,其作用是_____________________________________________。
22.(2分)下列说法不正确的是(填写标号) .
A.用托盘天平进行称量,一般可准确到0.01g.
B.容量瓶上标有温度和容量,使用前要检查是否漏水.
C.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛.
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再慢慢注入浓硫酸.
E.用四氯化碳、苯或汽油均可以从溴水中萃取溴.
21.(8分)物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。
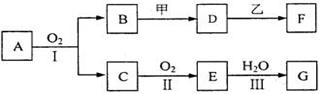
(1)若A为硫酸工业的重要原料,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成。则
①工业上反应Ⅱ在 中进行(填设备名称),
工业上反应Ⅲ用于吸收E的试剂是 。
②反应I的化学方程式是 。
(2)若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。则
①甲的电子式是 。
②写出B和甲反应的化学方程式是 。
③若17gA与O2反应生成气态的B和C时放出226.7kJ热量,
写出该反应的热化学方程式: 。
20.(11分)Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于______________晶体,俗名叫_______________;
(2)R的氢化物分子的空间构型是____________,属于________分子(填“极性”或“非极性”) ;它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是___________;
(3)X的常见氢化物的空间构型是________________;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是__________________;
(4)Q分别与Y、Z形成的共价化合物的化学式是_________ 和__________;Q与Y形成的分子的电子式是________________,属于_________分子(填“极性”或“非极性”)。
19.(8分)有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素。已知A、C及B、D分别是同主族元素,且B、D两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍,在处于同周期的C、D、E三元素中,E 的原子半径最小,通常情况下,五种元素的单质中有三种气体两种固体。
(1)试比较D、E两元素的最高价氧化物对应的水化物的酸性强弱(填化学式):____>____
(2)A和B可形成原子个数比为1∶1的化合物,其电子式为____________。
(3)将E单质通入A、B、C三种元素组成的化合物的水溶液中,
写出反应的化学方程式__________________________________________________。
(4)写出两种均含A、B、C、D四种元素的化合物在溶液中相互反应且生成气体的离子方程式__________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com