
16.(8分)2008年9月25 H,神州七号太空飞船被长征2号F型火箭送入太空。
(1)神舟七号太空飞船的外壳是一种新型结构陶瓷材料,它的主要成分是氮化硅。依据氮、硅原子的结构特点,推测氮化硅的化学式为 。工业上使用SiCl4和N2在H2气下生成氮化硅,其化学反应式为 。
(2)神舟七号太空飞船采用某种电化学装置,消除宇航员呼吸过程中产生的CO2,提供呼吸所需要的氧气。该装置可实现如下转化:2CO2=2CO+O2,CO可作燃料。
若该过程的阳极反应为4OH–+4e–=O2↑+2H2O,则该过程的阴极反应为 。
(3)长征2号F型火箭的推进剂是液氢和液氧。已知:2H2(g)+O2(g)=2H2O(1)
△H=﹣571.6kj•mol–1;H2(g)=H2(1) △H =﹣0.92 kj•mol–1;O2(g)=O2(1)
△H =﹣6.84 kj•mol–1;H2O(g)=H2O(1) △H=﹣44.0kj•mol–1。
请写出液氢和液氧生成气态水的热化学方程式: 。
15.下列溶液中有关物质的量浓度关系不正确的是
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:
c(H+)+c(M+)=c(OH–)+c(A–)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液
c(NaOH)<c(Na2CO3)<c(CH3COONa)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO–)+2c(OH–)=2c(H+)+c(CH3COOH)
D.0.1mol•L-1NaHA溶液,其pH等于4:c(HA–)>c(H+)>c(H2A)>c(A2–)
第Ⅱ卷(非选择题,共55分)
14.化学实验室中常将溶液或试剂进行酸化,下列酸化处理合理的是
A.配制氯化铝溶液时,为防止其水解,可加入稀硫酸酸化
B.为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化
C.除NaCl溶液中混有的CaCl2时,应加入足量的Na2CO3,过滤,滤液用硝酸酸化
D.用氯化钡溶液鉴别溶液中是否有SO42–时,溶液可用盐酸酸化
13.下列说法正确的是
①非金属氧化物一定不是碱性氧化物
②NH4SO4溶液的pH比NH4NO3溶液的pH小
③含有阴离子的物质中一定含有阳离子
④常温下在pH=3的溶液中,K+、Fe2+、C1–、CO32–不能大量共存
⑤因为SO2有漂白性,所以向酸性高锰酸钾溶液中通入SO2,溶液褪色
A.①②③④⑤ B.①②③④ C.①③④ D.①④⑤
12.金属材料在日常生活以及生产中有着广泛的运用。下列说法不正确的是
A.镁铝合金的性质与镁、铝单质的性质不完全相同
B.中国南海正在打捞的明代沉船上存在大量铝制餐具
C.镁铝合金因坚硬、轻巧、美观、易于加工而成为新型建筑装潢材料
D.镁铝虽然活泼,但却具有良好的抗腐蚀性
11.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素x,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列结论正确的是:
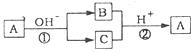
A.x元素可能为铝 B.反应①和②互为可逆反应
C.x元素可能是金属,也可能是非金属 D.反应①和②一定为氧化还原反应
10.某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g) 2AB3(g)化学平衡状态的影响。得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的判断结论正确的是
2AB3(g)化学平衡状态的影响。得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的判断结论正确的是
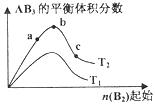
A.反应速率a>b>c B.达到平衡时A2的转化率大小为:b>a>c
C.若T2>T1,则正反应是放热反应 D.达到平衡时,AB3的物质的量大小为:c>b>a
9.下列说法正确的是
A.仅由非金属元素组成的化合物一定是共价化合物
B.电能与化学能的相互转化过程中一定有新物质产生
C.向饱和AgCl溶液中加入盐酸,Ksp变大
D.F、Cl、Br、I的氢化物稳定性逐渐减弱,其水溶液的酸性也逐渐减弱
8.运用元素周期律分析下面的推断,其中推断错误的是
A.氢氧化铍[Be(OH)2]的碱性比氢氧化镁弱.
B.砹(At)为有色固体;HAt不稳定;AgAt感光性很强,且不溶于水也不溶于稀酸
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是无色、有毒,比H2S稳定的气体
7.将SO2通入CuSO4和NaCl的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀分析,测得含Cl:35.7%,Cu:64.3%,SO2在上述反应中作用是
A.酸 B.漂白剂 C.氧化剂 D.还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com