
23.生活中常见的金属防腐的方法很多。下列措施不能起到防腐的是
A.健身器材刷油漆
B.衣架和电线的外面包上一层塑料层
C.在轮船船身上装上一定数量的铜块
D.在钢铁的表面镀上一层锌
22.不同国家垃圾的分类方法不同。我国国家标准《城市生活垃圾分类标准》中有六个粗分的一级类别和八个细分的二级类别。下列标志属于垃圾回收标志的是

21.下列属于天然高分子化合物的是
A.油脂 B.蔗糖 C.聚乙烯 D.淀粉
21.(12分)下面是某化学研究性学习小组对某水样成分的检验过程,已知该水样中只可能含有 和
和 离子中的若干种,该小组同学取100mL水样进行实验:
离子中的若干种,该小组同学取100mL水样进行实验:
向样品中先滴加BaCl2溶液,再滴加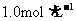 的盐酸,实验过程中沉淀质量的变化如下图所示:
的盐酸,实验过程中沉淀质量的变化如下图所示:

请回答下列问题:
(1)水样中一定含有的阴离子是___________,其物质的量之比为___________。
(2)写出BC段曲线所表示反应的离子方程式_________________________________。
(3)由B点到C点变化过程中消耗盐酸的体积为___________。
(4)试根据实验结果推测 是否存在?___________(填“是”或“否”);若存在,
是否存在?___________(填“是”或“否”);若存在, 的物质的量浓度
的物质的量浓度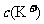 的范围是_________。(若
的范围是_________。(若 不存在,则不必回答该问)
不存在,则不必回答该问)
20.(10分)已知A、B、D、H是中学化学中常见的单质,J为蓝色溶液。转化关系如下(部分生成物及反应条件已略去):

(1)若A、B均为气体时,当用玻璃棒分别蘸取C、G的浓溶液并使它们靠近时,有白烟生成,则:①请写出下列物质的化学式D_____________,E_____________。②请写出反应Ⅱ的化学方程式_________________________________。
(2)若A为气体,B为固体时,已知C在D中完全燃烧可生成E和水。E是一种常见的空气污染物,且将C与E混合可生成淡黄色固体B。写出C与E反应的化学方程式_________________________________。简述检验气体E的方法___________ _______________________________________________________。
19.(16分)目前国际上使用的“海水淡化”主要技术之一是蒸馏,将海水变成蒸汽,蒸汽经过冷却得到淡水,剩余的溶液可用来提取氯化钠、氯化镁等多种工业原料。工业上用电解熔融NaCl或MgCl2的方法分别制备金属钠和镁。同时得到氯气。
(1)若金属钠长期暴露在空气中,最终转化为___________,取一定量的该物质溶于水配制成饱和溶液,通入CO2气体后发现溶液变浑浊,写出发生反应的化学方程式____________________________________________。
(2)若金属钠着火,不能用干冰灭火器灭火,原因是(用化学方程式表示)__________ ________________________________。若金属镁着火,也不能用干冰灭火器灭火,原因是(用化学方程式表示)____________________________________________。
(3)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
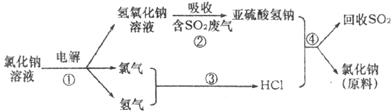
写出反应②的化学方程式_________________________________________;
写出反应④的化学方程式__________________________________________。
氯气排放会污染环境,可用NaOH溶液来吸收Cl2,写出该反应的化学方程式_______________________________________________________。
18.(14分)某化学活动小组对社区内一个化工厂排放的废水进行研究。经咨询该厂技术人员知,该废水中含有多种阳离子,仅含有 一种阴离子。
一种阴离子。
(1)该小组的同学首先通过实验确定了该废水中存在 。证明溶液中存在
。证明溶液中存在 ,常用的试剂是___________。
,常用的试剂是___________。
(2)在技术人员的协助下,该小组同学确定该废水中只含有
 、
、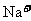 五种阳离子。某同学认为可从该废水中提取铜,并提出了如下实验方案:
五种阳离子。某同学认为可从该废水中提取铜,并提出了如下实验方案:

①当向溶液中加入足量铁粉时,能发生多个化学反应,写出相应的离子方程式_______________________________________________________。
②进行过滤操作时,下列仪器中不需要的是___________(填写序号字母)。
A.漏斗 B.玻璃棒 C.量筒 D.酒精灯 E.烧杯
③若向滤液中通入氯气,发生反应的离子方程式(不要求写出水跟氯气反应的离子方程式)____________________________________________。
④该实验方案存在明显缺陷,请你帮助该同学纠正这个缺陷(简要叙述正确的做法)_______________________________________________________。
17.(8分)实验室现需配制物质的量浓度为 的NaOH溶液480mL。
的NaOH溶液480mL。
(1)实验过程中用到的玻璃仪器有:烧杯、量筒、胶头滴管、___________、___________。
(2)要配制此溶液,需要称量NaOH固体的质量为___________。
(3)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请解释原因(用化学方程式表示)____________________________________________。
16.在石灰窑中烧制生石灰,1molCaCO3完全分解所需要的能量,可通过完全燃烧0.50mol碳(与空气中的O2反应生成CO2)来提供。设空气中O2体积分数为0.20,N2为0.80,则石灰窑的气体中CO2的体积分数(保留两位小数)是
A.0.39 B.0.41 C.0.43 D.0.49
第Ⅱ卷(非选择题 共60分)
15.下列反应的离子方程式不正确的是
A.盐酸加入氨水:
B.铜片插入硝酸银溶液:
C.碳酸钙加入醋酸:
D.铜粉加入稀硝酸: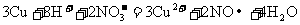
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com