
28.(14分)A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应,B、C、F都是气态单质,且B为黄绿色;反应③中有水生成,反应②需要放电才能发生,A和D相遇有白烟生成。

(1)反应③的化学方程式为: ;
(2)反应①中每生成1 molC,转移的电子数为 ;
(3)A与D的水溶液恰好完全反应时,其生成物的水溶液呈 性(填“酸”“碱”或“中”),该水溶液中存在着如下关系,用粒子浓度符号填写。
① c(H+)+ = c(OH-)+ ;② c(H+)= c(OH-)+ ;
(4)元素X与组成B的元素同周期,X的单质既可与酸反应也可与碱反应且都生成H2,则① X的单质与碱反应的离子方程式 ;
② X、空气、海水可以组成新型海水标志灯的电池。该电池以海水为电解质溶液,靠氧气使X不断氧化而源源不断产生电流,只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20~50倍。则该新型电池的正极的电极反应式为 ;原电池的总反应方程式为 。
15.常温下,0.1mol·L-1某一元酸(HA)溶液中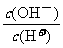 =1×108,下列叙述正确的是( )
=1×108,下列叙述正确的是( )
A.该一元酸溶液的pH=1
B.该溶液中由水电离出的c(H+)=1×10-11mol·L-1
C.该溶液中水的离子积常数为1×10-22
D.用pH=11的NaOH溶液V1L与V2L0.1 mol·L-1该一元酸(HA)溶液混合,若混合溶液的pH=7,则V1<V2
第Ⅱ卷(必做120分+选做32分,共152分)
第Ⅱ卷共16个小题。其中23-30题为必做部分,31-38为选做部分,考生必须从中选2个物理、1个化学和1个生物题作答。不按规定选做者,阅卷时将根据所选科目题号的先后顺序只判前面的2个物理题、1个化学题和1个生物题,其他作答的题目答案无效。
[必做部分]
14.下列实验的失败是因为缺少必要的实验步骤造成的是 ( )
①将乙醇和乙酸混合,再加入稀硫酸供热制乙酸乙酯
②将在酒精灯火焰上灼烧至表面变黑的Cu丝冷却后插入乙醇中,Cu丝表面仍是黑色
③要除去甲烷中混有乙烯得到干燥纯净的甲烷,将甲烷和乙烯的混合气体通过溴水
④做葡萄糖的还原性实验时,当加入新制的氢氧化铜碱性悬浊溶液后,未出现红色沉淀
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入银氨溶液后未析出银镜
A.①④⑤ B.①③④⑤ C.③④⑤ D.④⑤
13.下表是五种银盐的溶度积常数(25℃)
|
化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
|
溶度积 |
1.8×10-10 |
1.4×10-5 |
6.3×10-50 |
7.7×10-13 |
8.51×10-16 |
下列说法错误的是 ( )
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀
C.氯化银、溴化银和碘化银三种物质在常温下的溶解度按氯、溴、碘的顺序减小
D.向100mL0.1mol·L-1的Na2SO4溶液中加入1 mL0.1mol·L-1的AgNO3溶液,有白色沉淀生成
12.短周期元素X、Y、Z的原子序数一次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子束是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是 ( )
A.X的最高价氧化物的水化合物显弱酸性
B.Y的氧化物是离子化合物
C.Z的氢化物的水溶液在空气中存放不易变质
D.X的氢化物和Z的氢化物会反映生成一种对热稳定的化合物
11.下列反应的离子方程式正确的是 ( )
A.向铁粉中加入稀盐酸:2Fe+6H+=3Fe3++3H2↑
B.在Ca(HCO3) 2溶液中加入过量NaOH溶液:Ca2++OH-+HCO3-=CaCO3↓H2O
C.铜片加入稀硝酸中:Cu+NO3-+4H+=Cu2++NO↑+2H2O
D.氯化铝溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH) 3↓+3NH4+
10.下列说法中不正确的是 ( )
A.向鸡蛋清溶液中加入(NH4)2SO4饱和溶液,有沉淀析出,再加水沉淀不溶解
B.聚乙烯和聚氯乙烯塑料薄膜均可通过加聚反应得到,其中聚乙烯可做食品包装袋,而聚氯乙烯不能
|
D.食用植物油的主要成分是不饱和高级脂肪酸甘油酯,是人体必需的营养物质
9.化学与科学发展、生产、生活密切相关。下列说法中错误的是 ( )
A.卫生部公布的首批非法食品添加剂中的三聚氰胺是一种含氮量很高的蛋白质
B.“神七”飞船返回舱的绝热层所使用的耐高温、抗氧化的新型材料
C.“碳纳米泡沫”被称为第五形态的单质碳,与石墨互为同素异形体
D.陶瓷、欧力、水泥是使用量很大的无机非金属材料,都属于硅盐酸产品
23.(8分)将标准状况下的11.2L氨气溶于100mL水中,得到密度为0.868 g·cm 的氨水。该气体的物质的量=___________mol;溶液的体积=___________L;所得氨水的物质的量浓度= _____________mol·L
的氨水。该气体的物质的量=___________mol;溶液的体积=___________L;所得氨水的物质的量浓度= _____________mol·L 。
。
22.(11分)某化学兴趣小组为检验碳和浓硫酸反应生成的产物,设计如下图装置(已知SO2能使溴水褪色),请回答:

(1)指出仪器名称:甲______________ 乙________________
(2)乙仪器中发生反应的化学方程式为_________________________________;
(3)证明有二氧化碳产生的实验现象是_________________________________;
(4)F试管中离子反应方程式为________________________;
(5)若把B玻璃管移到F试管后连接,是否可行___________(填“可行”或“不可行”),理由___________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com