
23.下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。

(1)在表中画出主族与非主族的交界线。
(2)元素j是由法国科学家Marguerite Perey发现的,为了纪念她的祖国,她将该元素称为francium,元素符号为Fr。下列元素中,得名的原因和j元素相同的是_______
A.氯 B.锗 C.钋 D.氮
(3)比较f和g气态氢化物水溶液的酸性强弱:________>_________(填化学式)比较c和e单质的熔点高低:_________>_________(填化学式)
(4)画出d元素原子的轨道式____________________
(5)描述i元素在周期表中的位置_____________________,i元素原子的最外层电子数为2,请画出该元素的原子结构示意图__________________,描述元素i所形成单质的一个特性_____________________________________
22.常温下,0.1 mol·L-1某一元酸(HA)溶液中 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.该溶液中由水电离出的c(H+)=1×10-11 mol·L-1
B.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
C.0.1 mol·L-1HA溶液与0.05 mol·L-1 NaOH溶液等体积混合后所得溶液中c(A-) + c(HA) =c(Na+)
D.0.1 mol·L-1HA溶液与0.05 mol·L-1 NaOH溶液等体积混合后所得溶液中2c(H+)+ c(HA) =c(A-) + 2c(OH-)
21.化学家们合成了如下图所示的一系列的星烷,如三星烷、四星烷、五星烷等。下列说法正确的是:

A.它们之间互为同系物
B.六星烷的分子式为C18H24
C.三星烷与丙苯互为同分异构体,四星烷与 互为同分异构体
互为同分异构体
D.它们的一氯代物均只有两种,而三星烷的二氯代物有四种
20.以下集气装置中不正确的是:

19.实验室可用下图装置(启普发生器)制取氢气。欲使得到氢气的速率加快,下列措施可行的是:

A.将稀硫酸改用浓硫酸
B.向稀硫酸中加入少量浓H2SO4
C.向稀硫酸中加入Cu(NO3)2溶液
D.给装置中发生反应的部分加热
18.以下决定物质性质的因素全面,正确的是:
A.元素的化学性质:元素原子的最外层电子数
B.KNO3的溶解度:温度
C.分子间作用力:相对分子质量
D.气体摩尔体积:温度、压强
17.将0.2mol KMnO4在一定条件下加热后生成a mol O2,将剩余固体与过量的浓盐酸混合加热后又生成b mol Cl2,此时锰元素均以Mn2+存在,若a+b=m,则m的值可能是:
A.0.35 B.0.45 C.0.55 D.0.60
16.FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时生成H2S2,H2S2类似H2O2易分解,实验室用稀盐酸与FeS2颗粒混合,反应完毕后,不可能生成的物质是:
A.H2S B.S C.FeS D.FeCl2
15.下列化学反应的离子方程式正确的是:
A.用小苏打治疗胃酸过多: HCO3- + H+ →CO2↑+ H2O
B.往碳酸镁中滴加稀盐酸: CO32- + 2H+→CO2↑+ H2O
C.往氨水中滴加氯化铝: Al3+ + 4OH- →AlO2- + 2H2O
D.氢氧化钡溶液与稀硫酸反应: Ba2+ + SO42- + H+ + OH- →BaSO4↓+ H2O
14.N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是:
A.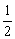 N2H4(g)+
N2H4(g)+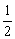 O2(g)→
O2(g)→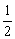 N2(g)+H2O(l)+267
kJ
N2(g)+H2O(l)+267
kJ
B.N2H4(g)+O2(g)→N2(g)+2H2O(l)+133.5 kJ
C.N2H4(g)+O2(g)→N2(g)+2H2O(g)-534 kJ
D.N2H4(g)+O2(g)→N2(g)+2H2O(g)+534 kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com