
11.下列叙述正确的是
A.常温常压下 气体与水反应生成
气体与水反应生成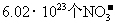 离子
离子
B.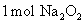 与足量水反应转移电子数为
与足量水反应转移电子数为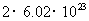 个
个
C.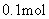 碳酸钠溶于水所得溶液中阴离子总数大于
碳酸钠溶于水所得溶液中阴离子总数大于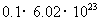 个
个
D.标准状况下,含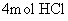 的浓盐酸与足量
的浓盐酸与足量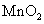 反应可生成
反应可生成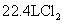
10.下列实验能获得成功的是
A.无水乙酸和乙醇共热制取乙酸乙酯
B.将苯逐滴滴入浓硝酸和稀硫酸的混合液中,并用沸水浴加热制取硝基苯
C.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复原来的红色
D.淀粉用酸催化水解后的溶液加入新制Cu(OH)2溶液,加热可看到砖红色沉淀出现
9.下列说法正确的是
A.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水
B.废弃的塑料、金属、纸制品及玻璃等都是可回收再利用的资源
C.凡含有食品添加剂的食物对人体健康均有害,不宜食用
D.某些不合格大理石装潢材料中含有严重超过规定标准,对人体有害的放射性同位素氡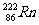 ,其原子中的质子数为136
,其原子中的质子数为136
29.(14分)请根据下图所示填空:
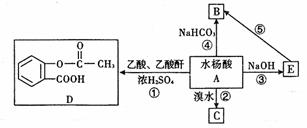
(1)化合物 A中含有的官能团名称为 ;
(2)反应②的反应类型是 ;
(3)1molD跟NaOH溶液供热反应,最多需要NaOH的物质的量为 mol;
(4)写出下列反应的化学方程式
A→D: ;
E→B: ;
(5)符合下列三个条件的A的同分异构体的数目有 个。
i)苯环上有一氯代物;ii)能与氯化铁溶液发生显色反应;iii)能发生银镜反应。
写出其中任意一个同分异构体的结构简式 。
28.(共16分)实验室中,用如下图所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略装置内空气中的CO2。
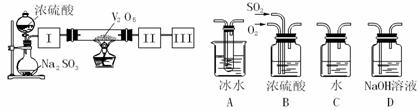
(1)已知0.5 mol SO2被O2氧化成气态SO3,放出49.15 kJ热量,反应的热化学方程式
为 。
(2)烧瓶中发生反应的化学方程式为 。
(3)根据实验目的,请从上面右图A→D四个装置中选择Ⅰ、Ⅱ、Ⅲ处合适的装置,将其序号填入空格中:装置Ⅰ ,装置Ⅱ ,装置Ⅲ 。
(4)开始进行实验时,首先应进行的操作是 。
(5)停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3被充分吸收,操作方法是 。
(6)实验结束后,若装置Ⅱ增加的质量为b g ,装置Ⅲ增加的质量为a g,则此条件下二氧化硫的转化率是 ;
27.(共14分)中学化学常见物质A、B、C、D、E、F、G之间有如下图所示的转化关系(反应条件已省略)
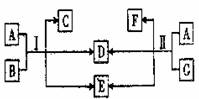
(1)若A是黑色非金属固体单质,C、D、F是气体,且C的相对分子质量小于F,E
在常温下呈液态。
① D分子的空间构型为 ;
② 反应Ⅱ的化学方程式为 ;
③ 将C和F的混合气体通入下列溶液中,会出现白色沉淀的是 (填字母编号)
a.BaCl2 b.Ba(NO3) 2 c.Na2SiO3 d.Ba(OH) 2
(2)若A是红色金属,B、G是同种溶质不同浓度的溶液,C、F是气体,且C可通过化合反应生成F。
① 反应Ⅰ的离子方程式为 ;
② 实验室测定F的相对分子质量时,得到的实验值总是比理论值大,其原因是
。
(3)若A是Ca(OH) 2,D是一种极易溶于水的气体,当1molA分别与B、G完全反应,反应Ⅰ、Ⅱ生成的物质的量之比为2:1,则B、G的化学式分别为 。
26.(共16分)
(1)已知氢氰酸(分子式为HCN)分子中各原子均达到稳定状态且氮元素显-3价,则氢氰酸分子的电子式为 ;又知常温时,0.1mol/L氢氰酸溶液的pH=5,则KCN 溶液的pH 7(填“>”、“<”或“=”)
(2)氰化物有毒,工业生产中通常用氯氧化法处理含CN-的废水。液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),发生如下反应 KCN+2KOH+Cl2===KOCN+2KCl+H2O。投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平化学方程式:

某厂废水中含KCN,其浓度为650mg/L,若采用上述方法处理废水20L,要使KCN完全转化为无毒物质,至少需液氯 g。
(3)HCN分子中的氢原子被氨基(-NH2)取代后可得氰胺分子的结构式为:
。
(4)三聚氰胺由于含氮量高而被一些厂家非法掺入奶粉中提高其产品的含氮量,以提高食品检测中蛋白质的含量指标,欺骗消费者,但长期服用这样的奶粉会使婴儿得肾结石,严重时则危及生命。
① 已知乙炔在一定条件下可以三聚生成苯:
三聚氰胺也可以由氰胺发生类似于乙炔三聚生成苯的反应而得到,又知三聚氰胺分子是非极性分子,则三聚氰胺分子的结构简式
②若由氰胺合成三聚氰胺反应的转化率为75%,则反应后的混合物中氮元素的质量分数为 %(小数点保留一位)
13.取0.2mol/L HX溶液与0.2mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化,)测得混合后溶液的pH=8,则下列说法中正确的是 ( )
A.混合溶液中c(X-)+c(HX)=0.1mol/L
B.HX为一元强酸
C.混合溶液中由水电离出的c(OH-)小于原NaOH溶液中由水电离出的c(OH-)
D.混合溶液中各离子浓度关系为c(X-)>c(Na+)>c(OH-)>c(H+)
第Ⅱ卷 (非选择题 共10题,共174分)
12.如图所示:用惰性电极电解足量的硫酸铜溶液,通电一段时间后,当电路中有0.04mol电子通过时,停止反应,下列说法中正确的是 ( )
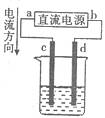
A.c为阳极,发生还原反应
B.电解后溶液的pH>7
C.d极上可析出金属1.28g
D.向电解后溶液中添加0.02molCu(OH)2时,可恢复到电解前浓度
11.在一密闭容器中进行如下反应:2SO2(g)+O2(g)  2SO3(g) ,已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
2SO3(g) ,已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
A.SO2为0.5mol/L,O2为0.2mol/L B.SO2为0.25 mol/L
C.SO2、SO3均为0.15 mol/L D.SO3为0.4 mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com