
33.[化学-有机化学基础](8分)
A-K分别代表不同的机物。它们之间的相互转化关系如下图:
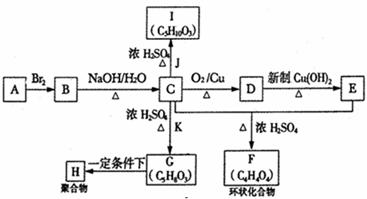
(1)A的结构式为 ;指出C→G的反应类型
(2)写出下列转化的化学方程式。
①C→D
②G→H
(3)与有机物I互为同分异构体,结构中含有羧基和羟基且不能被催化氧化的有机物的结构简式 、
32.[化学-物质结构与性质](8分)
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素

试回答下列问题:
(1)元素f的基态原子电子排布式__________________________________________
(2)a与c形成的化合物,其分子够型为________,中心原子的杂化形式为___________。
(3)由b原子跟d原子以1:1相互交替结合而形成的晶体,晶型与晶体d相同,但其熔点比晶体d高,原因为:_____________________________________________________________
(4)1183K以下e晶体的基本结构单元如图1所示,1183K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的e的原子间距离相同。
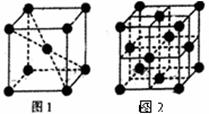
①在1183K以下的晶体中,与e原子等距离且最近的原子数为________个;在1183K以上的晶体中,与e原子等距离且最近的原子数为________;
②转变温度前后两者的密度比(1183K以下与1183K以上之比)________。(均可用根号表示)
31.[化学-化学与技术](8分)
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
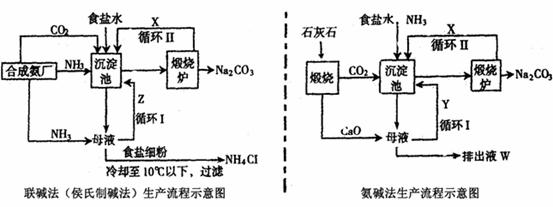
(1)沉淀池中发生反应的化学方程式中__________________________________________;
(2)从理论上分析,在氨碱法生产过程中_______(填“需要”、“不需要”)补充氨气;
(3)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确的是
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯鞍更多析出
c.加入食盐细粉目的是提高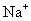 的浓度,促进碳酸氢钠结晶析出
的浓度,促进碳酸氢钠结晶析出
(4)联碱法中,每当通入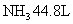 (标准状况下)时可以得到纯碱100.0g,则
(标准状况下)时可以得到纯碱100.0g,则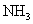 的利用率________。相比于氨碱法,指出联碱法的一项优点
的利用率________。相比于氨碱法,指出联碱法的一项优点
30.(18分)某校化学研究性学习小组的同学在学习了氨的性质后,谈论氨气的还原性,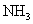 能否还原CuO呢?他们设计实验来研究这个问题。
能否还原CuO呢?他们设计实验来研究这个问题。
I.(1)实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,写出反应的化学方程式_______________________________________________________。
(2)实验室还可用___________和浓氨水反应快速制取少量氨气。
Ⅱ.该小组成员设计实验研究氨气还原性及其产物,实验装置(夹持及尾气处理装置未画出)图如下:

(1)该装置在设计上有一定的缺陷,为确保实验结果的准确性,你对该装置改进措施是______________________________________________________________________________,
______________________________________________________________________________。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO 变蓝,同时生成一种无污染的气体。请写出
变蓝,同时生成一种无污染的气体。请写出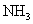 与
与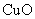 反应的化学方程式________________________
反应的化学方程式________________________
Ⅲ.该小组成员用氨气还原氧化铜的方法测定铜的近似相对原子质量,如果选用测定反应物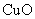 和生成物
和生成物 的质量
的质量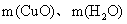 时,请用下图所示的仪器设计一个简单的实验方案。
时,请用下图所示的仪器设计一个简单的实验方案。

(1)仪器连接的顺序是_________(填编号,仪器可重复使用);
(2)D中浓硫酸的作用是_______________;
(3)列出计算铜的近似相对原子质量的表达式_______________;
(4)下列情况将使测定结果偏大的是____________
A.CuO未全部还原为Cu B.CuO受潮 C.CuO中混有Cu
[选做部分]
共8个题,考生必须从中选择2个物理题、1个化学题和1个生物题,并在答题纸上规定的区域作打。
29.(12分)
Ⅰ.回答下列有关常数的问题:
(1)Kw的数学表达式是 ,温度升高Kw (选填“变大”、“变小”或“不变”),若定义pOH=-lgc(OH-),则pH+pOH= (用含Kw的代数式表示)
(2)Ka通常表示弱酸的电离平衡常数,Ka值越大表示该弱酸的酸性_________。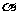 通常称为电离度,顾名思义是表示弱电解质的电离程度大小的一个指标,对于某一元弱酸,当用蒸馏水稀释该酸时,Ka______(选填“变大”、“变小”或“不变”),
通常称为电离度,顾名思义是表示弱电解质的电离程度大小的一个指标,对于某一元弱酸,当用蒸馏水稀释该酸时,Ka______(选填“变大”、“变小”或“不变”),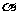 _____________(选填“变大”、“变小”或“不变”)。
_____________(选填“变大”、“变小”或“不变”)。
(3)K表示难溶物的溶度积常数,该常数越大表示__________________________。
Ⅱ.由于温室效应和资源短缺等问题,如何降低大气中的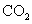 含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用
含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用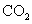 生产燃料甲醇。一定条件下发生反应:
生产燃料甲醇。一定条件下发生反应: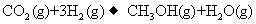 ,下图表示该反应的下列说法中,正确的是________。
,下图表示该反应的下列说法中,正确的是________。
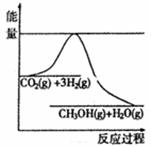
A.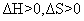 B.
B.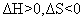 C.
C. D.
D.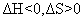
(2)该反应平衡常数K的表达式为________________________。
(3)温度降低,平衡常数K_____(填“增大”、“不变”或“减小”)。
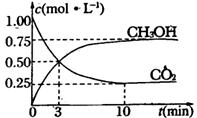
(4)在体积为1L的密闭容器中,充入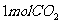 和
和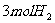 ,测得
,测得 和
和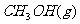 的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率
的浓度随时间变化如下图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率
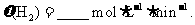
(5)下列措施中能使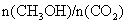 增大的有__________。
增大的有__________。
A.升高温度 B.加入催化剂 C.将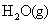 从体系中分离
从体系中分离
D.再充入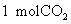 和
和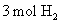 E.充入
E.充入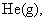 使体系总压强增大
使体系总压强增大
28.(12分)
已知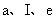 为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
|
粒子代码 |
a |
I |
e |
|
原子粒数 |
单核 |
四核 |
双核 |
|
粒子的电荷数 |
一个单位正电荷 |
0 |
一个单位负电荷 |
物质A由a、e构成,B C D K X都是单质,X是地壳中含量最多的金属元素形成的单质,反应①-⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示:
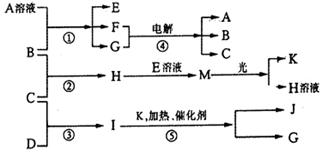
请填写下列空白:
(1)写出下列物质的化学式:B: J:
(2)写出反应④的离子方程式:
(3)写出下列反应的化学方程式反应⑤:
X与A的水溶液:
(4)E溶液中离子浓度由大到小的顺序:
15.将一定量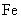 和
和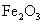 的混合物放入
的混合物放入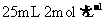 的
的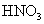 溶液中,反应完全后,无固体剩余,生成
溶液中,反应完全后,无固体剩余,生成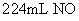 气体(标准状况),再向反应后的溶液中加入
气体(标准状况),再向反应后的溶液中加入 的
的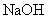 溶液,要使铁元素全部沉淀下来,所加
溶液,要使铁元素全部沉淀下来,所加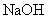 溶液的体积最少是
溶液的体积最少是
A.40mL B.45mL C.50mL D.55mL
第Ⅱ卷(必做题+选做题)
[必做部分]
14.某无色溶液中可能含有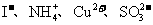 ,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含 ; ②肯定不含
; ②肯定不含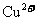 ③肯定含有
③肯定含有 ;
;
④可能含有 ; ⑤可能含有
; ⑤可能含有 ;
;
A.①②③ B.②④⑤ C.①②⑤ D.②③④
13.2007年1月8日,国防科工委举行新闻发布会,明确承认“中国具备制造航空母舰的能力”。初步计划,预计国产大功率镍氢动力电池将在制造航空母舰中发挥作用。常用镍氢电池的某极是储氢合金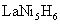 (
(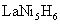 中各元素化合价均为零),电池反应通常表示为
中各元素化合价均为零),电池反应通常表示为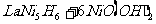

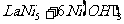 ,下列说法不正确的是
,下列说法不正确的是
A.放电时储氢合金作负极
B.充电时储氢合金作阴极
C.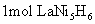 参加放电,能提供12mol电子
参加放电,能提供12mol电子
D.充电是将电能转化为化学能的过程
12.已知①向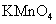 晶体滴加浓盐酸,产生黄绿色气体;②向
晶体滴加浓盐酸,产生黄绿色气体;②向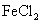 溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性: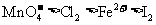
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明 具有还原性
具有还原性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com