
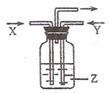
14.下列各组物质中,气体X和气体Y在通常条件下同时通入盛有溶液z的洗气瓶中(如下图所示),一定没有沉淀生成的是
|
|
X |
Y |
Z |
|
A |
NO2 |
SO2 |
BaCl2 |
|
B |
NH3 |
O2 |
Al2(SO4)3 |
|
C |
NH3 |
CO2 |
NaCl(饱和) |
|
D |
CO |
O2 |
Ca(OH)2 |
13.常温下,物质的量浓度均为0.1mol·L-1的两溶液HA、BOH。其中HA溶液的pH>1,BOH溶液中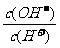 =1012,则下列有关说法正确的是
=1012,则下列有关说法正确的是
A.HA溶液中水的电离程度小于BOH溶液中水的电离程度
B.将HA、BOH溶液稀释相同的倍数,pH值变化前者大于后者
C.若两溶液混合时:V(BOH)≥V(HA) ,则必有混合液中c(B+)>c(A-)
D.将HA、BOH混合,若所得溶液的pH=7,则溶液中必有
c(B+)=c(HA)+c(A-)
12.X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.由于氢键的影响,3种元素的气态氢化物中X的气态氢化物最稳定
D.原子半径由小到大的顺序为Z<Y<X
11.T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变化如图(I)所示。保持其他条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示。下列结论正确的是
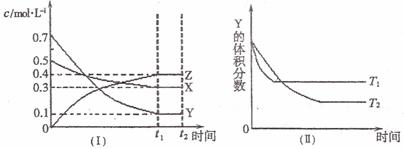
A.t2时,保持其它条件和物质状态不变,增加压强,化学平衡向逆反应方向移动
B.T℃时,若密闭容器中各物质起始浓度为:0.4 mol/L X、0.4 mol/L Y、0.2 mol/L Z。保持其他条件不变,达到平衡时z的浓度为0.4 mol/L
C.图(Ⅱ)中T1>T2,正反应是吸热反应
D.其他条件不变,若升高温度,正、逆反应速率均增大,且X的转化率增大
10.A、B、C三种物质,每个分子中都含有18个电子,且B、C均为两种元素组成的化合物。其中A的分子属于非极性分子,且只有非极性键;B的分子由四个原子构成,既有极性键也有非极性键;C的分子由八个原子构成。A、B、C在常温下状态分别是
A.固、液、液 B.气、液、气
C.液、液、气 D.气、气、气
9.实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是

A.装置①常用于分离互不相溶液体混合物
B.装置②可用于吸收HCl气体,并防止倒吸
C.以NH4HCO3为原料,装置③可用于实验室制备少量NH3
D.装置④b口进气可收集CO2、NO等气体
8.下列离子方程式正确的是
A.用惰性电极电解硫酸铜溶液: Cu2+ +2OH-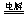 Cu↓ +
H2↑+O2↑
Cu↓ +
H2↑+O2↑
B.浓烧碱溶液中加入铝片:Al+2OH-=AlO2-+H2↑
C.在水中加入少量的过氧化钠粉末 2O22- + 2H2O=4OH- + O2↑
D.Ba(OH)2溶液中滴入NaHSO4溶液至恰好为中性:
2H+ +SO42- + Ba2+ +2OH-=BaSO4↓+2H2O
7.F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解。其中6XeF4+12H2O=2XeO3+4Xe↑+24HF+3O2↑,下列推测正确的是
A.XeF2分子中各原子均达到八电子的稳定结构
B.某种氟化氙的晶体结构单元如下图所示,可推知其化学式为XeF6

C.XeF4按已知方式水解,每生成4mol Xe转移16mol电子
D.XeF2加入水中,在水分子的作用下,将重新生成Xe和F2
6.下列两种气体的分子数一定相等的是
A.等温、等体积的CO和CO2 B.等体积、等密度的CO和C2H4
C.等温、等压的N2和C2H4 D.等压、等体积的NO2和CO2
5.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.在25℃,压强为1.01×105Pa时,11.2L氮气所含的原子数目为NA
B.23g Na与足量的O2完全反应,失去的电子数目为NA
C.32 g S8(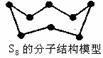 )单质中含有的S-S键个数为2NA
)单质中含有的S-S键个数为2NA
D.28.6g Na2CO3·10H2O在晶体中或在溶液中,含有的CO32-离子均为0.1NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com