
17.(10分)通风是关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成尿酸钠(NaUr)晶体,有关平衡如下:
①Hur(尿酸,aq) Ur-(尿酸根,aq)+H+(aq)(37℃时,Ka=4.0×10-6)
Ur-(尿酸根,aq)+H+(aq)(37℃时,Ka=4.0×10-6)
②NaUr(s) Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)
(1)37℃时,1.0 L水中最多可溶解8.0×10-3mol尿酸钠,此温度下尿酸钠的Ksp为________。
(2)关节炎发作多在脚趾和手指的关节处,这说明温度降低时,尿酸钠的Ksp为______(填“增大”、“减小”或“不变”),生成尿酸钠晶体的反应是___________(填“放热”或“吸热”)反应。
(3)37℃时,某尿酸结石病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3mol·L-1,其中尿酸分子的浓度为5.0×10-4mol·L-1,该病人尿液的c(H+)为________,pH_______(填“>”、“=”或“<”=7。
16.(8分)下图是由短周期元素组成的物质之间的转化关系。其中,A的相对分子质量为144,反应①中生成C、D物质的量之比为3∶1,D是不溶于水的白色固体,除反应③⑤外其它反应均在溶液中进行,F、G是气态非金属单质,K是一种常见的非极性有机溶剂,密度比水大。(某些生成物和反应条件已略去)。
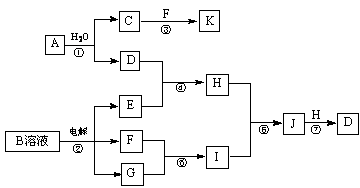
(1)A的分子式是_________________;
(2)E中金属阳离子的检验方法是______________________________;
(3)写出反应②的化学方程式__________________________________;
(4)写出反应⑦的离子方程式__________________________________;
(5)用离子方程式表示H溶液显碱性的原因_____________________。
15.(10分)某学习小组研究Cr2O3催化氧化SO2成SO3的部分实验装置如下图所示。

(1)C处发生反应的化学方程式是__________________。
(2)实验中能证明有SO3生成的现象是__________________________。
(3)欲使进入C反应器内O2和SO2的体积比为2∶1,监控方法是____________。
(4)实验中观察到E瓶内有气泡,而在D瓶中没有明显现象,原因是_________。
(5)如果用止水夹夹紧k处的乳胶管,D瓶中可见持续稳定的气泡出现。证明浓硫酸能吸收SO3的方法是_____________。
14.铜的冶炼过程大致可分为:
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为:
2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6 Cu+SO2↑;
④电解精炼铜。
下列说法正确的是 ( )
A.冶炼过程中的可用来制硫酸
B.上述过程中,由1 mol CuFeS2制取1 mol Cu时共消耗2 mol O2
C.在反应2Cu2O+ Cu2S=6 Cu+SO2↑中,只有Cu2O作氧化剂
D.电解精炼铜的过程中,每转移1mol电子时,阳极溶解铜的质量为32g
13.某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0-t1阶段c(B)未画出]。图乙为t2后改变互不相同的某一条件时反应速率跟时间的关系,其中t3-t4阶段使用催化剂。下列说法正确的是( )
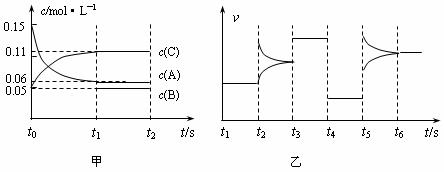
A.若t1=15 s,生成物C在t0-t1时间段的平均反应速率为0.004mol·L-1·s-1
B.t4-t5阶段改变的条件为降低反应温度
C.B的起始物质的量为0.02mol
D.t5-t6阶段改变的条件是增大反应物浓度
12.目前。我国城市供水处理技术由混凝、沉淀、过滤和消毒等过程组成。下列说法中,不正确的是 ( )
A.传统的无机混凝剂按金属盐可分为铝盐系和铁盐系两大类
B.NCl3可用于水消毒的原因是因为NCl3跟水反应生成了NH3
C.用ClO2代替Cl2作消毒剂可减少有害氯代有机物的浓度
D.新型水处理剂高铁酸钠(Na2FeO4)既是消毒剂又是混凝剂
11.下列溶液中有关物质的量浓度关系正确的是 ( )
A.10℃时pH=2的NaOH溶液与40℃时pH=12的NaOH溶液中:c(OH-)相等
B.25℃时pH=10的NaOH溶液与pH=10的氨水中:c(Na+)=c(NH4+)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
D.0.1mol·L-1 (NH4)2Fe(SO4)2 溶液中:c(NH4+)+c(Fe2+)+c(NH3·H2O)=0.3mol·L-1
10.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得。
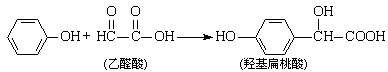
下列有关说法正确的是 ( )
A.苯酚和羟基扁桃酸互为同系物
B.常温下,1mol羟基扁桃酸只能与1mol Br2反应
C.乙醛酸的核磁共振氢谱中只有1个吸收峰
D.羟基扁桃酸分子中至少有12个原子共平面
9.下列关于物质分离和提纯的方法正确的是 ( )
A.CuCl2酸性溶液中含有少量FeCl3:加入Cu(OH)2调节溶液pH=4,再过滤
B.苯中含有少量苯酚:加入浓溴水后过滤
C.CaCO3中混有少量CaSO4:加入饱和Na2CO3溶液,充分搅拌后过滤,再用水多次洗涤沉淀
D.乙酸乙酯中混有少量乙酸:加入NaOH溶液后萃取
8.在下列溶液中,各组离子能够大量共存的是 ( )
A.pH=7的溶液中:Cl-、CO32-、SO32-、Na+
B.强酸性溶液中:NH4+、NO3-、CH3COO-、K+
C.加入KSCN溶液显血红色的溶液中:Fe2+、Mg2+、Cl-、SO42-
D.含大量HCO3-的溶液中:Ca2+、Cl-、Al3+、NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com