
11.用 表示阿伏加德罗常数,下列说法中一定正确的是
表示阿伏加德罗常数,下列说法中一定正确的是
A.1 mol甲烷中的氢原子被氯原子完全取代,需要 分子2
分子2 个
个
B.标准状况下,22.4 L 中所含的分子数为
中所含的分子数为
C.常温常压下,m g乙烯与m g丙烯中均含有
 对共用电子对
对共用电子对
D.1 mol.
 溶液中含有
溶液中含有 的数目为2
的数目为2
10.下列式子哪一个能用来精确地计算任意稀盐酸溶液中的氢离子浓度c( )的是(Kw为水的离子积常数)
)的是(Kw为水的离子积常数)
A.c( )=c(HCl) B.c(
)=c(HCl) B.c( )=c(HCl)+Kw/c(
)=c(HCl)+Kw/c( )
)
C.c( )=C(HCl)+Kw
D.c(
)=C(HCl)+Kw
D.c( )=c(HCl)一Kw/c(
)=c(HCl)一Kw/c( )
)
9.在复杂的体系中,确认化学反应先后顺序有利于解决问题。下列化学反应先后顺序判断正确的是
A.在含等物质的量的 的溶液中,逐滴加入盐酸:
的溶液中,逐滴加入盐酸:

B.在含等物质的量的 、
、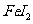 的溶液中,缓慢通入氯气:
的溶液中,缓慢通入氯气:
C.在含等物质的量的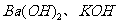 的溶液中缓慢通入
的溶液中缓慢通入 :
:

D.在含等物质的量的 的溶液中加入锌粉:
的溶液中加入锌粉:
8.室温下,下列四种溶液:①0.1 mol· 氨水; ②0.1 mol·
氨水; ②0.1 mol· N
N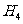 CI溶液;③0.2 mol·
CI溶液;③0.2 mol· 盐酸与0.2 mol·
盐酸与0.2 mol· N
N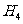 Cl溶液等体积混合; ④0.1 mol
Cl溶液等体积混合; ④0.1 mol 的N
的N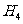 HC
HC 溶液;四种溶液中
溶液;四种溶液中 由大到小的顺序正确的是
由大到小的顺序正确的是
A.②③①④ B.③②④①
C.①②③④ D.③④②①
7.下列关于元素周期表和元素周期律的说法不正确的是,
A.从氟到碘,生成的氢化物熔沸点逐渐升高,稳定性逐渐减弱
B.因为钠原子比铝原子容易失去电子,所以钠比铝的还原性
C.从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强
D.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强
6.下列每组物质发生状态变化时,所克服微粒间的相互作用属于同种类型的是
A.食盐和蔗糖溶解 B.钠和硫熔合
C.碘和干冰升华 D.二氧化硅和氧化镁熔合
22.(9分)标准状况下,将a L Cl2通入到1 L b mol/L的FeI2溶液中,充分反应后,所得溶液中Fe2+的物质的量浓度与a、b的关系如下表,请完成其余空格。
|
a、b的关系 |
Fe2+的物质的量浓度(mol/L) |
|
a ≤22.4b |
①
|
|
②
|
0 |
|
22.4b ≤a
≤33.6b |
③
|
21.(8分)过碳酸钠和盐酸反应的化学方程式为: 2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O,商品过碳酸钠中一般都含有Na2CO3,为了测定它的纯度,取一定量的样品和盐酸反应,通过测量产生的氧气的体积,可以计算出过碳酸钠的含量。
(1)根据下图提供的仪器装置,组装一套测定商品过碳酸钠的实验装置,这些装置的连接顺序是(填接口字母): 。

(2)装置④的作用: 。
(3)如果实验时,称取wg样品和过量盐酸反应后,测得生成的氧气的体积(标准状况)为VmL(不考虑氧气在溶液中的溶解),则此样品的纯度为 。
(4)某次实验,称取0.9g样品进行测定,实验室有50mL,100mL,150mL三种规格的量筒,应选用规格为 的量筒进行实验。
20.(8分)现有中学常见的三种单质甲、乙、丙,它们在一定条件下能发生如下变化(次要生成物略去)
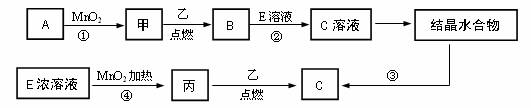
(1)已知乙元素的+2价离子与Ne原子具有相同的电子层结构,则④的离子方程式为 ;
(2)若反应①可在常温下进行,则A的名称是___________。若反应①需在加热条件下进行,则反应的化学方程式为 ;
(3)从C溶液中得到C需经过两步操作:先从C溶液中得到晶体,再将得到的晶体转化为C。将得到的晶体转化为C的实验条件是 。
19.(10分)下面是一张空白的元素周期表,请按要求填空:
|
① |
|
|
|||||||||||||||
|
② |
④ |
|
|
|
⑤ |
⑥ |
|
|
|||||||||
|
|
|
|
|
|
⑦ |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
③ |
|
|
|
|
|
|
|
|
|
|
|
|
(1)表中编号为②、③两元素的原子序数之差为 ;
(2)表中编号为⑥、⑦两元素形成氢化物稳定性 > (用相应物质的化学式填空);
(3)A、B分别是由①、⑤、⑥三种元素组成的化合物,其中:
I、常温时,0.1mol/LA的水溶液pH=1,则A的化学式为 ;
Ⅱ、B溶液中水的电离被促进,则B的化学式为
(4)人们发现有些元素的化学性质与它在周期表中左上方或右下方的另一主族元素相似,这称为对角线规则,如元素④的单质与Al的性质相似。则元素④的单质与NaOH溶液反应的化学方程式为 : 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com