
9.下列离子方程式书写正确的是
A.硫酸氢钠溶液中加入氢氧化钡至溶液呈中性:
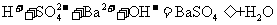
B.向漂白粉溶液中通入少量SO2:

C. 溶液与过量NaOH溶液反应:
溶液与过量NaOH溶液反应:

D.偏铝酸钠溶液中通入过量的 :
:

8.为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
|
|
被提纯的物质 |
除杂试剂 |
分离方法 |
|
A |
溴化钠溶液(NaI) |
氯水、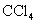 |
萃取、分液 |
|
B |
苯(苯酚) |
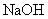 溶液 溶液 |
过滤 |
|
C |
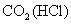 |
饱和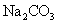 溶液 溶液 |
洗气 |
|
D |
乙醇(乙酸) |
新制生石灰(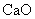 ) ) |
蒸馏 |
7.化学与生活、社会密切相关。下列说法不正确的是
A.化石燃料不可再生,使用太阳能代替化石燃料,有利于节约资源、保护环境
B.三聚氰胺(cyanuramide,分子式 )含氮量很高,可作为饲料添加剂
)含氮量很高,可作为饲料添加剂
C.我国规定商家不得无偿提供塑料袋,目的是为了减少“白色污染”
D.甘蔗渣经化学反应可制得酒精
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较用下图装置进行实验,实验时均以生成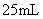 气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
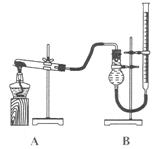
|
实验序号 |
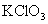 质量 质量 |
其它物质质量 |
待测数据 |
|
④ |
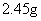 |
无其他物质 |
|
|
⑤ |
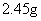 |
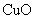  |
|
|
⑥ |
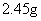 |
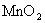  |
|
回答下列问题:
(4)上述实验中的“待测数据”指 ;
(5)本实验装置图中量气装置B由干燥管、乳胶管和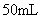 滴定管改造后组装而成,此处所用滴定管是
(填“酸式”或“碱式”)滴定管;
滴定管改造后组装而成,此处所用滴定管是
(填“酸式”或“碱式”)滴定管;
(6)若要证明实验⑤中干燥管内收集的气体是 ,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
;
,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
;
(7)若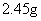 氯酸钾完全分解,则在标准状况下可得氧气多少
氯酸钾完全分解,则在标准状况下可得氧气多少 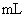 。
。
28.(12分)在某个容积为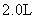 的密闭容器内,在T℃时按下图1所示发生反应:
的密闭容器内,在T℃时按下图1所示发生反应:
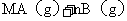

 ,
, (
(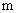 、
、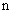 、
、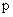 、
、 为最简整数比)。
为最简整数比)。
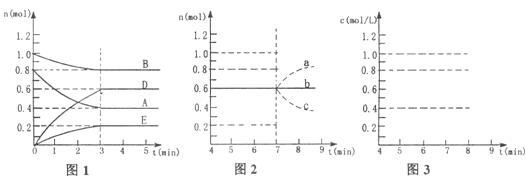
(1)据图l所示,反应开始至达到平衡时,用D表示该反应速率为 ;
(2)该反应的化学平衡常数K的数值为 (保留至两位小数);
(3)反应达到平衡后,第7min时:
①若降低温度,D的浓度变化最可能的是 (用图2中a-c的编号回答):
②若在7min时仍为原平衡,此时将容器的容积压缩为原来一半,请在图3中画出7min后D浓度变化情况。
(4)在T℃时,相同的容积为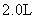 的密闭容器内,若开始时加入
的密闭容器内,若开始时加入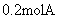 、
、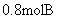 、
、 、
、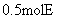 反应,达到平衡后,A的浓度范围为
。
反应,达到平衡后,A的浓度范围为
。
(5)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是 。
A.利用化学反应速率理论可指导怎样在一定时间内快出产品
B.加快反应速率可提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
29.(16分)我国目前的身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式为:
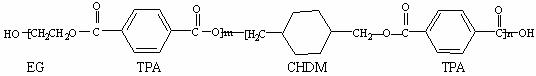
已知:
(1)

(2) (
( 、
、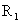 、
、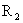 表示烃基)这种材料可采用下合成路线:
表示烃基)这种材料可采用下合成路线:
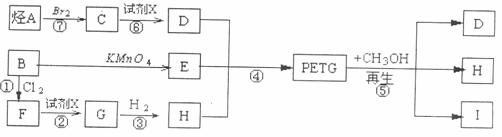
试回答下列问题:
(1)反应②⑥加入的试剂X是
(2)①的反应类型是
(3)写出结构简式:B I
(4)合成时应控制的单体的物质的量
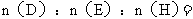 : : (用m、n表示)
: : (用m、n表示)
(5)写出化学方程式:
反应③ 反应⑥:
(6)物质I的同分异构体符合下列条件
①苯环上有三个取代基且分别处于间位,其中一个是醛基
②能与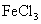 溶液发生显色反应
溶液发生显色反应
③不能与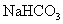 溶液反应放出
溶液反应放出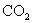 气体,但能在
气体,但能在 溶液中发生水解反应符合以上条件的I的同分异构体有
种,写出其中任意两种的结构简式:
溶液中发生水解反应符合以上条件的I的同分异构体有
种,写出其中任意两种的结构简式:
、
(一)制取氧化铜
①称取 研细后倒入烧杯,加
研细后倒入烧杯,加 蒸馏水溶解;
蒸馏水溶解;
②向上述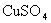 溶液中逐滴加入
溶液中逐滴加入 溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后放在研钵中研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),过滤时所用到的主要玻璃仪器的名称是 ;
(2)步骤③中洗涤沉淀的操作是 ;
(3)步骤③中洗去的杂质主要是 ;
7.化学与科技、社会、生产、生活密切相关,下列有关说法不正确的是( )
A.航天员的舱内航天服主要成分是由碳化硅陶瓷和碳纤维复合而成,它是一种新型无机非金属材料
B.塑料制品容易被微生物分解,所以废弃塑料不会对环境造成严重影响
C.奥运会开幕式上的绚丽焰火是焰色反应的实际应用例子之一
D.目前我国对奶粉中蛋白质含量的检测,是以奶粉中的含氮量为标准来检验的,在奶粉中加入三聚氰胺(结构如图,分子式为 ,能显著提高奶粉的含氮检测量
,能显著提高奶粉的含氮检测量

8.下列有关实验操作图与对应的实验目的不相符合的是( )
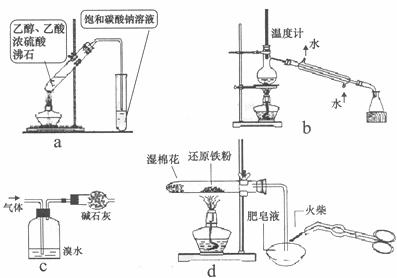
A.a图制取乙酸乙酯
B.b图分离两种互溶但沸点相差较大的液体混合物
C.c图检验并除去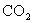 中的
中的 气体
气体
D.d图检验铁粉与水蒸气反应产生的氢气
9.向三份体积均为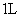 的
的
 溶液中分别加入
溶液中分别加入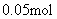 冰醋酸、
冰醋酸、
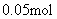
 、
、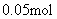
 固体,则溶液中
固体,则溶液中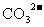 浓度的变化依次为:( )
浓度的变化依次为:( )
A.减小、减小、增大 B.减小、减小、减小
C.增大、减小、减小 D.减小、增大、增大
10.设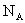 代表阿伏加德罗常数的数值,下列说法中正确的是:①常温常压下,
代表阿伏加德罗常数的数值,下列说法中正确的是:①常温常压下,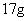 甲基
甲基 所含的中子数为
所含的中子数为 ;②常温常压下,
;②常温常压下,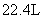
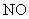 气体的分子数小于
气体的分子数小于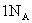 ;③
;③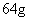 的铜发生氧化还原反应,一定失去
的铜发生氧化还原反应,一定失去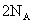 个电子;④常温常压下,
个电子;④常温常压下,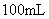
 的乙酸溶液中,乙酸的分子数目小于
的乙酸溶液中,乙酸的分子数目小于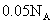 ;⑤标况时,
;⑤标况时,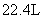 二氯甲烷所含有的分子数为
二氯甲烷所含有的分子数为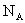 ;⑥常温常压下,
;⑥常温常压下,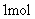 氦气含有的核外电子数为
氦气含有的核外电子数为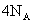
A.①② B.③④ C.②④ D.⑤⑥
11.禁止运动员使用兴奋剂是当代健康体育的重要举措之一。以下两种兴奋剂的结构分别为:
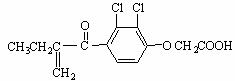
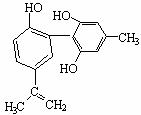
利尿酸 兴奋剂X
关于它们的说法中正确的是( )
A.它们遇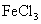 溶液均显紫色,均为芳香族化合物
溶液均显紫色,均为芳香族化合物
B.在考虑充分反应的条件下,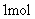 利尿酸也只能消耗
利尿酸也只能消耗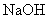
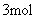
C.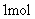 兴奋剂X在一定条件下最多与
兴奋剂X在一定条件下最多与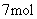
 加成
加成
D.两种分子中的所有碳原子均不可能共平面
12.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰。电池总反应为:
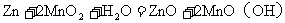 。关于此电池,下列说法正确的是( )
。关于此电池,下列说法正确的是( )
A.该电池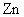 为负极,
为负极,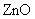 为正极,
为正极,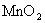 催化剂
催化剂
B.该电池的正极反应为: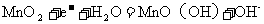
C.导电时外电路电子由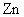 流向
流向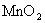 ,内电路电子由
,内电路电子由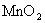 流向
流向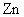
D.电池工作时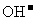 能通过薄层纸片向附着二氧化锰的电极移动
能通过薄层纸片向附着二氧化锰的电极移动
13.下列溶液中各微粒的浓度关系不正确的是( )
A.
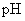 为4的
为4的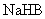 溶液中:
溶液中: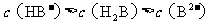
B.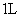

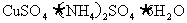 的溶液中:
的溶液中:
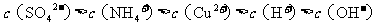
C.

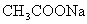 溶液与
溶液与
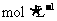 盐酸混合:
盐酸混合:
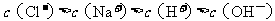
D.
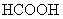 溶液中:
溶液中: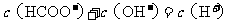
第Ⅱ卷 (非选择题 共174分)

(1)上表中的粗实线是元素周期表中部分边界,请在表中用粗实线补全主族元素边界。
(2)元素甲是第三周期ⅦA族元素,化合物A是由甲元素等非金属元素组成的离子化合物,写出其化学式 ,该物质的水溶液呈 性,用离子方程式表示原因 。
(3)元素乙是第三周期金属元素中原子半径最小的元素,写出工业上制金属乙的化学方程式 。
(4)化合物B是由甲元素和乙元素形成的化合物,将化合物A与化合物B等物质的量溶于水中,向其中滴加过量的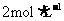 氢氧化钠溶液,直至形成透明溶液。请根据实验现象出现的先后顺序,依次写出离子方程式① 、② 、③ 。
氢氧化钠溶液,直至形成透明溶液。请根据实验现象出现的先后顺序,依次写出离子方程式① 、② 、③ 。
27.(16分)某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
29.(15分)某有机化合物X(C10H10O2)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
(1)X是下列化合物之一,已知X不能与FeCl3溶液发生显色反应,则X是 (填字母)

(2)下列有关X的叙述中正确的是 (填字母)
A.能与溴的四氯化碳溶液发生加成反应
B.不能使酸性高锰酸钾溶液褪色
C.在碱性条件下能发生水解反应
D.不可能发生加聚反应
(3)G为X的一种同分异构体,其分子结构模型如下图所示(图中○、●、 表示不同的原子,连结表示原子间的共价键)则G的结构简式为
。
表示不同的原子,连结表示原子间的共价键)则G的结构简式为
。

(4)用芳香烃A为原料合成G的路线如下:
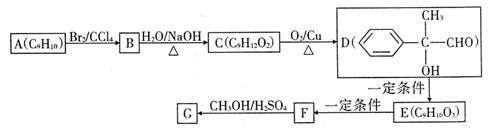
请根据合成G的路线回答下列问题:
①E中的官能团有 (填名称);
②B→C的反应类型是 ;
③写出F→G反应的化学方程式 ;
④写出符合下列条件的F的同分异构体的结构简式 。
a.分子内含有苯环,且苯环上只有一个支链;
b.一定条件下,1mol该物质与足量的银氨溶液充分反应,生成4mol银单质。
28.(16)某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。
其实验流程图如下:

(1)测定硝酸的物质的量
反应结束后,从下图B装置中所得100mL溶液中取出25.00mL溶液,用0.1mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如右上图所示。在B容器中生成硝酸的物质的量为 mol。
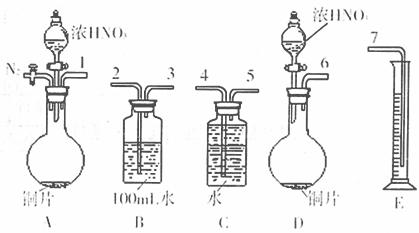
(2)测定NO的体积
①从上图所示的装置中,你认为应选用 装置进行Cu与浓硝酸反应实验,选用的理由是 。
②选用上图所示仪器组合一套可用来完成实验并测定生成NO体积的装置,其合理 的连接顺序是(填各导管口编号) 。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的 位置 (“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析:若实验测得NO的体积为112.0mL(已折算到标准状况),则Cu与浓硝酸反应的过程中 (填“有”或“没有”)NO产生,作此判断的依据是 。
(4)实验前,用托盘天平称取的铜片至少应为 g。
27.(13分)A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。现做如下实验:
|
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
请回答下列问题:
(1)根据以上事实推断A-E的化学式:
A ;B ;C ;D ;E 。
(2)请用离子方程式表示A溶液显碱性的原因 。
(3)写出②、③、④的离子方程式:② ;③ ;④ 。
26.(16分)W、X、Y、Z四种短周期元素,原子序数依次增大,在周期表中X、Y位于同一族,它们能组成YX2、YX3两种常见化合物。已知W与Z形成的化合物WZ3相是一种黄色、油状、具有刺激性气味的液体,W元素的氢化物与Z元素的氢化物反应只生成一种盐a。
请回答下列问题:
(1)X元素位于周期表中第 族,Y元素名称为 ;
(2)Y、Z两元素对应氢化物的稳定性大小为 > (填对应的化学式);
(3)已知WZ3分子中W与Z均满足8电子稳定结构,则WZ3的电子式为 ;
(4)若在盐a溶液中加入少量镁粉,可观察到的现象是 ;
(5)W元素的氢化物与Z元素的单质在一定条件下可生成化合WZ3与盐a。写出该反应的化学方程式 ;
(6)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com