
8ЃЎШчЯТЭМЫљЪОЕФзАжУЃЌCЁЂDЁЂEЁЂFЁЂXЁЂYЖМЪЧЖшадЕчМЋЁЃНЋЕчдДНгЭЈКѓЃЌЯђ(вв)жаЕЮЁЁ ШыЗгЬЊШмвКЃЌдкFМЋИННќЯдКьЩЋЁЃдђвдЯТЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
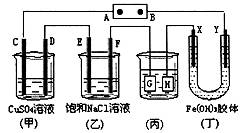
ЁЁЁЁЁЁ AЃЎЕчМЋBМЋЪЧе§МЋ
ЁЁЁЁЁЁ BЃЎ(Мз)ЁЂ(вв)зАжУЕФCЁЂDЁЂEЁЂF ЕчМЋОљгаЕЅжЪЩњГЩЃЌЦфЮяжЪЕФСПжЎБШ1ЃК2ЃК2ЃК2
ЁЁЁЁЁЁ CЃЎгћгУ(Бћ)зАжУИјЭЖЦвјЃЌHгІИУЪЧAgЃЌЕчЖЦвКЪЧAgNO3ШмвК
ЁЁЁЁЁЁ DЃЎзАжУ(ЖЁ)жаПДЕНЕФЯжЯѓЪЧXМЋИННќКьКжЩЋБфЩю
7ЃЎЪвЮТЪБЃЌФГШмвКжаЫЎЕчРыГіЕФc(H+)=10-13mol/LЃЌЯТСаРызгдкШмвКжавЛЖЈФмДѓСПЙВДцЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎFe3+ЁЂNH4+ЁЂCl-ЁЂI-ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎBa2+ЁЂNa+ЁЂCl-ЁЂNO3-
ЁЁЁЁЁЁ CЃЎK+ЁЂHCO3-ЁЂBr-ЁЂBa2+ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎK+ЁЂCO32-ЁЂNO3-ЁЂAl3+
6ЃЎЯТСаИїЯюжаЕФСНИіСПЃЌЦфБШжЕвЛЖЈЮЊ2ЃК1ЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎ100mL1.0molЁЄL-1Fe(NO3) 2ШмвКгы200m0.5molЁЄL-1HNO3ШмвКЛьКЯЃЌЛьКЯЧАКЭЛьКЯКѓc(NO3-)жЎБШ
ЁЁЁЁЁЁ BЃЎЯрЭЌЮТЖШЯТЃЌ0.2 molЁЄL-1ДзЫсШмвКгы0.1 molЁЄL-1ДзЫсШмвКжаc(H+)жЎБШ
ЁЁЁЁЁЁ CЃЎNH4+ХЈЖШЯрЭЌЪБЃЌCH3COONH4ШмвКгы(NH4) 2SO4ШмвКЕФЮяжЪЕФСПХЈЖШжЎБШ
ЁЁЁЁЁЁ DЃЎЪвЮТЪБpH=2ЕФHClШмвКгыpH=12ЕФBa(OH) 2ШмвКЕФЮяжЪЕФСПХЈЖШжЎБШ
5ЃЎЯТСаРызгЗНГЬЪНжае§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎNaHCO3ШмвКгызуСПЕФCa(OH)2ШмвКЃК
Ca2++2HCO3-+2OH-=2H2O+CaCO3Ё§+CO32-
ЁЁЁЁЁЁ BЃЎЭгыЯЁЯѕЫсЗДгІЃК3Cu+8H++2NO3-=3Cu2++2NOЁќ+4H2O
ЁЁЁЁЁЁ CЃЎТШЛЏТСШмвКгыЙ§СПЕФАБЫЎЗДгІЃКAl3++4NH3ЁЄH2O=AlO2-+4NH4++2H2O
ЁЁЁЁЁЁ DЃЎТШЦјЭЈШыЫЎжаЃКCl2+H2O=Cl-+ClO-+2H+
4ЃЎЯТСаЖдгаЙиЪЕбщЪТЪЕЕФНтЪЭе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЫсадKMnO4ШмвКжаЭЈШыSO2КѓЃЌбеЩЋЭЪШЅЃЌЪЧвђЮЊSO2ОпгаЦЏАзад
ЁЁЁЁЁЁ BЃЎЬњдкКЃЫЎжаБШдкЕЫЎжаИќвзИЏЪДЃЌЪЧвђЮЊКЃЫЎжаКЌЗсИЛЕФбѕЦј
ЁЁЁЁЁЁ CЃЎГЃЮТЯТЃЌНЋТСЦЌЗХШыХЈСђЫсжаЮоУїЯдЯжЯѓЃЌЪЧвђЮЊТСВЛКЭРфЕФХЈСђЫсЗДгІ
ЁЁЁЁЁЁ DЃЎХЈЯѕЫсдкЙтееЬѕМўЯТБфЛЦЃЌЪЧвђЮЊХЈЯѕЫсЗжНтЩњГЩЕФгаЩЋВњЮяШмгкХЈЯѕЫс
3ЃЎЩшNAБэЪОАЂЗќйЄЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎГЃЮТГЃбЙЯТ33.6LCl2гызуСПFeЗДгІЃЌзЊвЦЕФЕчзгЪ§ЮЊ3NA
ЁЁЁЁЁЁ BЃЎ1molNO2гызуСПH2OЗДгІЃЌзЊвЦЕФЕчзгЪ§ЮЊNA
ЁЁЁЁЁЁ CЃЎгЩCO2КЭO2зщГЩЕФЛьКЯЮяЙВгаNAИіЗжзгЃЌЦфжаЕФбѕдзгЪ§ЮЊ2NA
ЁЁЁЁЁЁ DЃЎ1molCO2ЗжзгжаЙВМлМќзмЪ§ЮЊ2NA
2ЃЎЯТСазАжУФмДяЕНЪЕбщФПЕФЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
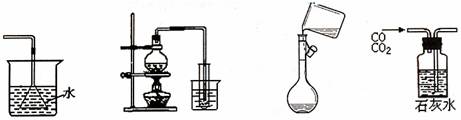
ЁЁЁЁЁЁ AЃЎЮќЪеАБЦјжЦАБЦј BЃЎжЦШЁЩйСПеєСѓЫЎCЃЎзЊвЦШмвКЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎГ§ШЅдгжЪЦјЬхCO2
1ЃЎЯТСагаЙиЮяжЪЗжРрЛђЙщРре§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ Ђй ЫсадбѕЛЏЮяЃКSO2ЁЂNO2ЁЂCO2ЁЂSiO2
ЁЁЁЁЁЁ Ђк ЗЧЕчНтжЪЃКвКАБЁЂАБЫЎЁЂвКЬЌТШЛЏЧтЁЂЙ§бѕЛЏЧт
ЁЁЁЁЁЁ Ђл ЕчНтжЪЃКТШЛЏТСЁЂЕЈЗЏЁЂБљДзЫсЁЂСђЫсБЕ
ЁЁЁЁЁЁ Ђм ЭЌЮЛЫиЃКHЁЂDЁЂTЁЂHD
ЁЁЁЁЁЁ Ђн ЭЌЫивьаЮЬхЃКC60ЁЂC70ЁЂН№ИеЪЏЁЂЪЏФЋ
ЁЁЁЁЁЁ Ђо РызгЛЏКЯЮяЃКCH3COONaЁЂAl2O3ЁЂNa2O2ЁЂCaC2
ЁЁЁЁЁЁ AЃЎЂйЂлЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂкЂмЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂйЂкЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂлЂнЂо
28ЃЎ(18Зж)ЯТЭМЪЧФГЪЕбщЪвВтЖЈЛЦЬњПѓжаСђдЊЫиЕФжЪСПЗжЪ§ЕФзАжУЃК
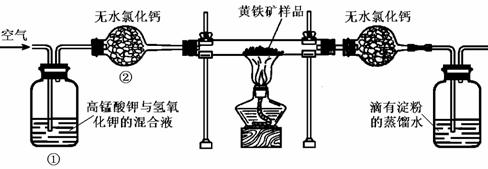
ЪЕбщЪБгаШчЯТВйзїЃКAЃЎНЋВЃСЇЙмжабљЦЗМгШШЕН800Ёц~850ЁцЁЃЁЁ BЃЎГЦШЁбаЯИЕФЛЦЬњПѓбљЦЗЁЃ CЃЎСЌНгКУШЋВПвЧЦїЃЌВЂМьВщЦфЦјУмадЁЃ DЃЎНЋбљЦЗаЁаФЗХШыгВжЪВЃСЇЙмжаВПЁЃEЃЎвдОљКуЕФЫйЖШВЛЖЯЙФШыПеЦјЁЃFЃЎгУБъзМЕтШмвКЕЮЖЈКЌЕэЗлЕФSO2ЫЎШмвКЁЃ
ЁЁ (1) е§ШЗЕФЪЕбщВНжшЕФДЮађЪЧ(вдAЁЂBЉЉЕФађКХБэЪО)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2) зАжУЂйЕФзїгУЪЧЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛзАжУЂкЕФзїгУЪЧЁЁЁЁ ЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3) ЕтИњSO2ЫЎШмвКЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4) ИљОнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЯжЯѓХаЖЯЕЮЖЈвбДяЕНжеЕуЁЃ
ЁЁ (5)гаЭЌбЇШЯЮЊгУЩЯЪізАжУВтГіЕФЛЦЬњПѓжаСђдЊЫиЕФжЪСПЗжЪ§ЭЈГЃНЋЦЋЕЭЃЌФуЪЧЗёЭЌвтИУЙлЕуЁЁЁЁ ЁЁ(ЬюЪЧЛђЗё)ЃЌЧыЫЕГіФуЕФжївЊРэгЩЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁ (6)МйЖЈПѓбљжаЕФСђШЋВПзЊЛЏЮЊSO2ЃЌВЂШЋВПБЛЫЎЮќЪеЁЃШєГЦЕУПѓбљЕФжЪСПЮЊ0ЃЎ0900gЃЌЕЮЖЈЙмжаЕтШмвКЕФГѕЖСЪ§ЮЊ1ЃЎ10mLЃЌФЉЖСЪ§ЮЊ25ЃЎ60mLЃЌБъзМЕтШмвКЕФХЈЖШЮЊ0ЃЎ0500 molЁЄL-1ЃЌдђИУЛЦЬњПѓбљЦЗжаСђдЊЫиЕФжЪСПЗжЪ§ЮЊЁЁЁЁЁЁЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com