
31.(8分)[化学--化学与技术]
亚氯酸钠(NaC1O2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
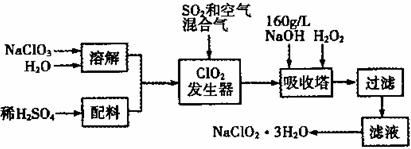
已知:①NaC1O2的溶解度随温度升高而增大,适当条件下可结晶体析出NaCIO2·3H2O
②纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
(1)发生器中鼓入空气的作用可能是________ _。
(2)吸收塔内的反应的化学方程式为________ _。
(3)在碱性溶液中NaC1O2比较稳定,所以吸收塔中应维持。NaOH稍过量,判断NaOH是否过量的简单实验方法是________ _。
(4)从滤液中得到NaC1O2·3H2O粗晶体的实验操作依次是________ _。
30.(13分)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;C元素的最高价氧化物对应水化物与其氢化物反应生成一种盐X;E与A同主族,且与F同周期;F元素的最外层电子数是其次外层电子数的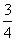 倍,A、B、C、E、F这五种元素,每一种与D元素都能形成原子个数比不相同的若干种化合物。请回答下列问题:
倍,A、B、C、E、F这五种元素,每一种与D元素都能形成原子个数比不相同的若干种化合物。请回答下列问题:
(1)写出D元素在元素周期表中的位置 _________。。
(2)F的最高价态与A、D、E三种元素形成酸式盐Y的化学式是_________,0.1mol/L的该盐溶液中的离子浓度由大到小的顺序是_________。
(3)常温时,C元素的最高价氧化物对应水化物的溶液的pH为n,则该溶液中由水电离出来的H+浓度为________ _。
(4)由A、B两元素组成的化合物中,A的质量分数最高的化合物Q与氢氧化钠溶液在一定条件下可形成燃料电池,写出电池负极的电极反应式________ _。
[选做部分]
任选2题回答。
28.(14分)向一密闭容器中加入2molA、0.6molC和一定量的B三种气体。一定条件下发生反应,恒条件下各物质浓度随时间变化如图一所示,图二为t2时刻后改变条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件(不同时充入反应物和生成物)。已知只有t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。
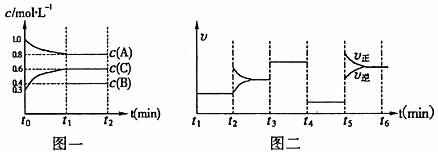
(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)= 。
(2)t5时改变的条件为 。各阶段平衡时对应的平衡常数如下表所示:
|
t1-t2 |
t2-t3 |
t3-t4 |
t4-t5 |
t5-t6 |
|
K1 |
K2 |
K3 |
K4 |
K5 |
则K1= (保留两位小数),K3、K4、K5之间的关系为 (用“>”、“<”或“=”连接)。
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式 。
(4)在相同条件下,若起始时容器中加入a molA、bmolB和cmolC,要达到t1时刻同样的平衡状态,a、b、c必须满足的条件为 、 。
14.物质的提纯是化学实验中的一项重要操作,也是化工生产及物质制备中的主要环节。下列有关叙述中,不正确的是 ( )
A.乙酸乙酯中混有乙酸,可选用饱和Na2CO3溶液洗涤,然后将两层液体分开
B.洗涤过滤后的AgCl沉淀,用稀盐酸洗涤比用蒸馏水洗涤沉淀损失少
C.油脂的提纯中,可将油脂加人浓NaOH溶液中加热,然后过滤,滤出的溶液即为较纯的油脂
D.甘蔗是制备蔗糖的主要原料,榨出的甘蔗汁因含色素而呈棕黄色,可先加入适量的活性炭,搅拌、过滤,将滤液蒸发结晶,即得较纯的蔗糖
l5.下表为元素周期表前四周期的一部分,下列有关X、W、Y、R、Z五种元素的叙述中正确的是 ( )
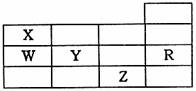
A.常温常压下,五种元素的单质中有两种是气态
B.Y、z的阴离子的电子层结构都与R原子的相同
C.w的氢化物比x的氢化物熔沸点高
D.Y元素最高价氧化物对应水化物的酸性比w元素的弱
第Ⅱ卷(必做+选做)
[必做部分]
13.用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.56gFe与稀HNO4完全反应时一定转移3NA个电子
B.1mol甲基中含有9NA个电子
C.常温常压下,0 .lNA个Al与足量氢氧化钠溶液反应生成3.36LH2
D.已知热化学方程式2SO2(g)+O2(g) SO3(g)△H=-QkJ/mol(Q>0),则将2NA个SO2分子和NA个O2分子置于一密闭容器中充分反应后放出QkJ的热量
SO3(g)△H=-QkJ/mol(Q>0),则将2NA个SO2分子和NA个O2分子置于一密闭容器中充分反应后放出QkJ的热量
12.要证明某酸是弱酸,下列方法正确的是 ( )
A.将串联小灯泡的该酸溶液与串联一相同小灯泡的硫酸溶液并联,接通电源后,若与该酸溶液串联的小灯泡较暗,则说明该酸是弱酸
B.测定该酸的钠盐溶液常温下的pH,若pH>7,则说明该酸是弱酸
C.用该酸与金属锌反应,若产生气泡较慢,则说明该酸是弱酸
D.若中和等体积等浓度的NaOH溶液消耗该酸的量大于硫酸,则说明该酸是弱酸
11.下列叙述不正确的是 ( )
A.往下水道中倾倒硫酸溶液,会加快铁制管道的腐蚀
B.钢铁的表面涂一层油脂或油漆,可以减慢钢铁的腐蚀
C.镁与稀盐酸反应剧烈,加入醋酸钠晶体可以减慢反应速率
D.铁放入稀硫酸中,再加入硝酸钠可以加快铁与稀硫酸反应放出氢气的速率
10.为验证人体呼出气体中含有的CO2不是来自空气,而是人体代谢作用产生的。某学校学生齐全外活动小组设计了如图所示装置(为防止液体被吸入口中或被吹出瓶外,呼吸时要慢或采取必要措施),你认为该装置I、II中应分别选用的试剂是 ( )

A.Ca(OH)2 NaOH B.NaOH Ca(OH)2
C.稀盐酸 Ca(OH)2 D.NaOH BaC12
9.“化学是人类进步的关键”,下列有关说法能反映正确化学观点的是 ( )
A.改变物质的性质一定要通过化学变化
B.天然物质都比人造物质好
C.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
D.根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com