
10.设NA表示阿伏加德罗常数的值,下列叙述中正确的是 ( )
A.1 L0.1 mol•L-1的CH3COONa溶液中CH3COO-的总数是0.1NA
B.常温常压下,1.6 gO2和O3混合气体中质子总数为0.8NA
C.一定条件下,2 molSO2和1 molO2发生反应,转移的电子总数一定是2NA
D.1L0.1mol•L-1的葡萄糖溶液中分子总数为0.1NA
29.(16分)2009年2月22日凌晨,山西屯兰煤矿发生瓦斯爆炸事故。煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷。目前利用甲烷与G发生反应制取副产品M溶液的设想在工业上已经实现。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:

根据要求回答问题:
(1)B装置有三种功能:①_____________ ②_____________ ③_______________。
(2)设V(G)/V(CH4) =x,若理论上欲获得更多的M,则x的值应___________。
(3)D装置的石棉中均匀混有KI粉末,其作用是_________________________。
(4)F装置的作用是____________(填编号)。
A.吸收M 物质 B.吸收G物质 C.防止倒吸
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,试写出置换出黑色小颗粒的化学方程式:_________________________________。
(6)反应结束后,F装置中还含有一定量的有机物,从F中分离出M的最佳方法为___________。(填操作名称)。该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为____________________。
28.(14分)现有分子式为C9H9O2X的物质甲(X为卤族元素),在一定条件下有如下转化关系,其中E可作为工业上的增塑剂。

(1)写出下列物质的结构简式:甲_________________,A_________________,F _______________。
(2)上述反应中属于取代反应的有__________________。
(3)D的某种同类同分异构体,苯环上的一氯代物只有两种,写出该同分异构体的结构简式_____________________。
(4)写出下列反应的化学方程式:
②的反应___________________________________________;
⑧的反应____________________________________________。
26.(16分)A、B、C、D、E、F、G都是短周期的主族元素,它们的核电荷数依次增大。元素A 的原子核内仅有一个质子,A、D同主族,B、C同周期且与A能形成相同电子数的化合物,C与F同主族,F的质子数为C的2倍,元素E 的最外层电子数比K层电子数多1,B、C、F的质子数之和等于E、G的质子数之和。请回答下列问题:
(1)写出由上述至少两种元素组成的具有漂白作用的物质的化学式______(请写出四种)。]
(2)A分别与B、F、G能形成相应的常见的三种化合物,同温同压下这三种化合物在水中的溶解度由大到小的顺序为_______________________(用化学式表示)。
(3)由A、B、C、D四种元素组成的一种常见化合物X的溶液分别与由C、D、E三种元素组成的一种化合物 Y的溶液和由E、G两种元素组成的一种化合物Z的溶液都能反应得到同一种白色沉淀,写出上述两个反应的离子方程式X+Y:_________________________;
X+Z:________________________________________。
(4)D、E两种元素的原子都能形成相应的离子,则两离子半径大小关系为_____________(用离子符号表示);将D、E两种元素的单质同时投入水中,充分反应后,测得溶液中只有一种溶质,且无固体剩余,则所投入到水中的D、E单质的质量比为_____________,上述反应总的化学方程式为________________________________。
|
已知在常温下测得浓度均为0.1 mol∙L-1下列6种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.1 |
8.8 |
11.6 |
10.3 |
11.1 |
11.3 |
(1)请根据上述信息判断下列反应能发生的是_____________(填编号)。
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CO2+H2O+ C6H5ONa →NaHCO3+ C6H5OH
D.CO2+H2O+ 2C6H5ONa →Na2CO3+ 2C6H5OH
E.Na2CO3+ C6H5OH →NaHCO3+ C6H5ONa
F.CH3COOH+NaCN = CH3COONa+HCN
(2)一些复分解反应的发生还遵循其他规律。下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液。
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体。
③蒸发 KCl和NaNO3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为________________。
(3)物质的量浓度均为0.05 mol∙L-1的下列5种物质的溶液中,pH由大到小的顺序是_____________(填编号)。
①C6H5OH ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(4)一定温度下,向等体积的纯水中分别加入等物质的量的下列物质:①NaOH ②CH3COOH ③NaClO,则水的电离程度最大的是__________(填编号)。一定温度下,向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,两溶液中离子的总物质的量分别为n1和n2,则它们的关系为n1_____n2(填“>”、“<”或“=”)。
13.已知Cu(NO3)2受热分解的化学方程式为:2Cu(NO3)2  2CuO+4NO2↑+O2↑。某学生将适量的Cu(NO3)2固体放入试管中加热使其分解,用集气瓶收集产生的气体,将带火星的木条伸入集气瓶中,木条复燃。下列有关说法正确的是: ( )
2CuO+4NO2↑+O2↑。某学生将适量的Cu(NO3)2固体放入试管中加热使其分解,用集气瓶收集产生的气体,将带火星的木条伸入集气瓶中,木条复燃。下列有关说法正确的是: ( )
A.木条复燃主要是因为反应中生成了O2
B.NO2能支持燃烧
C.NO2不能支持燃烧
D.不能确定NO2是否能支持燃烧
II卷(非选择题、本卷共10题。)
12.在密闭容器中充入等物质的量的A和B,一定温度下发生反应:


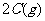 达到平衡后,只改变反应的一个条件,测得容器中物质A、C的浓度及反应速率随时间变化如下图所示。下列说法中正确的是: (
)
达到平衡后,只改变反应的一个条件,测得容器中物质A、C的浓度及反应速率随时间变化如下图所示。下列说法中正确的是: (
)
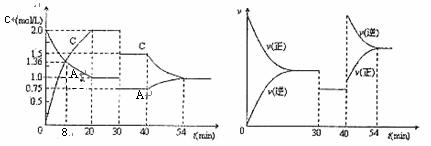
A.30min时降低温度,40min时升高温度
B.8min前A的平均速率为0.064mol∙L-1∙min-1
C.反应方程式中x=1,正反应为放热反应
D.30-40min间该反应使用了催化剂
11.a molFeS与b molFe3O4投入到VL c mol∙L-1的硝酸溶液中恰好完全反应,假设只生成NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的HNO3为 ( )
A(a+b)mol B.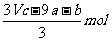
C. D.
D.
10.已知14 mol∙L-1H2SO4溶液的质量分数为80%,则7 mol∙L- 1H2SO4溶液的质量分数为 ( )
A.等于40% B.大于40%
C.小于40% D.无法确定
9.如图是工业上采用离子交换膜法电解足量饱和食盐水的示意图。下列有关说法中不正确的是: ( )
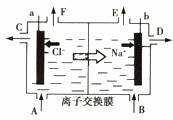
A.从E口逸出的是氢气
B.向B口中加入含少量NaOH 的溶液以增强导电性
C.标准状况下每生成22.4LCl2,便产生2molNaOH
D.向电解后的阳极室溶液中加入适量盐酸,各物质可以恢复到电解前的浓度
8.下列反应的离子方程式书写正确的是 ( )
A.乙醛的银镜反应:CH3CHO+2Ag(NH3)2OH→CH3COO-+NH4++3NH3+2Ag↓+H2O
B.向Ca(HCO3)2溶液中加入足量的澄清石灰水:
Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.向Na2CO3溶液中通入少量的HCl:CO32-+2H+=CO2↑+H2O
D.向含2molFeBr2溶液中通入2molCl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com