
14.下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法正确的是 ( )

A.该硫酸的物质的量浓度为9.2 mol·L-1
B.1mol Zn 与足量的该硫酸反应,标准状况下产生22.4L气体时,转移的电子数为NA
C.配制200mL 4.6 mol·L-1的稀硫酸需取该硫酸50mL
D.该硫酸与等体积的水混合后所得溶液的物质的量浓度等于9.2 mol·L-1
13.下列有关实验的叙述正确的是 ( )
A.检验溶液中SO42-的方法是:先加入BaCl2溶液,再加盐酸
B.从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏
C.证明气体分子中含有“C=C”的方法是:将该气体通入KMnO4酸性溶液
D.除去CO2中少量HCl的方法是:将混合气体通过盛有Na2CO3溶液的洗气瓶
12.下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解质溶液,下列有关说法中不正确的是 ( )

A.该能量转化系统中的水也是可以循环的
B.燃料电池系统产生的能量实际上来自于水
C.水电解系统中的阳极反应:4OH--4e- =2H2O+O2↑
D.燃料电池放电时的负极反应:H2-2e-+2OH-=2H2O
11.2008年北京奥运会的国家游泳中心(水立方)采用了高分子膜材料“ETFE”,该材料是 四氟乙烯(CF2=CF2)与乙烯(CH2=CH2)发生聚合反应得到的高分子材料。下列说法不正确的是 ( )
A.“ETFE”分子中可能存在“-CF2-CH2-CF2-CH2-”的连接方法
B.合成“ETFE”的反应为加聚反应
C.CF2=CF2和CH2=CH2均是平面型分子
D.该材料是一种合成高分子材料,不可以与氢气发生加成反应
10.中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是( )
A.用反应物、产物中键能的数据可判断化学反应的反应热
B.用沸点数据推测将一些液体混合物用分馏的方法分离开来的可能性
C.用反应热数据的大小判断不同反应的反应速率的快慢
D.用卤素阴离子半径数据推断其还原性的强弱
9.为保障人体健康,必须严格限制用量的是 ( )
A.用SO2漂白食品 B.用小苏打制作糕点
C.用食醋清洗热水瓶胆内壁附着的水垢 D.用O3对游泳池中的水进行消毒
33.(8分)[化学--有机化学基础]
乙基香草醛( )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
)是食品添加剂的增香原料,其香味比香草醛更加浓郁。
(1)任意写出两种乙基香醛分子中含氧官能团的名称 。
(2)乙基香草醛的同分异构体A是一种有机酸,A可以发生以下变化:
提示:①RCH2OH→RCHO
②与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基

(a)由A→C的反应属于 (填反应类型)
(b)写出A的结构简式 。
(3)乙基香草醛的另一种同分异构体D(CH3O- -COOCH3)是一种医药中间体,请设计合理方案用茴香醛(CH2O-
-COOCH3)是一种医药中间体,请设计合理方案用茴香醛(CH2O- -CHO)合成D(其它原料自选,用反应流程图表示,并注明必要的反应条件)。
-CHO)合成D(其它原料自选,用反应流程图表示,并注明必要的反应条件)。

32.(8分)[化学--物质结构与性质]
(1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是: 。

(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是 ,分子构型是 ,从成键方式看,该分子中含有的共价键的类型和数目分别是 。
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙 甲,其原因是
。
31.(8分)[化学--化学与技术]
某试剂厂用银(含杂质铜)和硝酸(含杂质Fe3+)反应制取硝酸银。步骤如下:
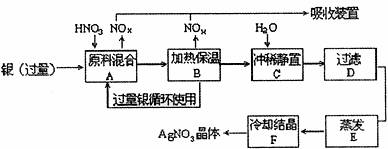
依据上述步骤,完成下列填空:
(1)溶解银的硝酸应该用 硝酸(填浓或稀),原因是 。
a.减少过程中产生NOx的量
b.减少原料银的消耗量
c.节能硝酸物质的量
(2)步骤B加热保温的作用是
a.有利于加快反应速度
b.有利于水反应的硝酸挥发
c.有利于硝酸充分反应,降低溶液中c(H+)
(3)步骤C是为了除去Fe3+、Cu2+等杂质。冲稀静置时发生的化学反应是 (选类型),产生的沉淀物化学式 。
a.置换反应 b.水解反应 c.氧化-还原反应
30.(11分)碘是人体的必需微量元素之一。加碘食盐中加重主的碘酸钾是一种白色结晶粉末,常温下很稳定。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物等还原性物质反应。
I.工业生产碘碳钾的流程如下:

已知步骤①发生反应为6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑
反应中还原剂是 (填化学式),转移电子数为 。
II.已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(1)检验加碘食物中的碘元素。
学生甲利用碘酸与碘化钾在酸性条件下发生反应,检验是否有碘单质生成所需要的试剂是 ,判断碘单质存在的现象是 ;若要进一步分离提纯碘单质,用到的主要玻璃仪器有 。
(2)测定加碘食盐中碘的含量。学生乙设计的实验步骤如下:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好完全反应(I2+2S2O2-3=2I-+S4O2-6)。则加碘食盐样品中的碘元素含量是 mg./kg(以含w的代数式表示)。
(3)有人认为可以用碘化钾代替食盐中的碘酸钾,学生丙又进行了下列实验:
|
操作步骤 |
实验现象 |
|
取1g纯净的NaCl,加3mL水配成溶液。 |
溶液无变化 |
|
滴入5滴淀粉溶液和1ml0.1mol/L
KI溶液,振荡。 |
溶液无变化 |
|
然后再加入少量食醋,振荡。 |
溶液变蓝色 |
根据学生丙的实验结果,回答下列问题
①你认为能否用碘化钾代替食盐中的碘酸钾 (填“能、不能或不确定”)②你认为学生乙的实验结果 (填“偏高、偏低、无影响”)。
[选做部分]
考生从中选择1个化学题作答。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com