
27.(14分)
A、D、E、G是中学化学常见物质,它们有如图所示的变化关系。
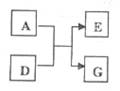
请根据下列各种情况回答问题:
I.A、D均由两种元素组成,其中一种元素为氧元素,E在常温常压下为气态单质,G的焰色为黄色。
(1)A为日常生活中最常见的无色液体,则G物质的电子式为 ;
(2)A是一种不支持燃烧的无色无味气体(常温常压),则A与D反应的化学方程式为
。
II.点燃条件下,单质D在氧化物A中燃烧生成白色固体G和黑色固体单质E,G是一种高熔点的氧化物。则A与D反应的化学方程式为 。
III.A在常温常压下为红棕色固体。
(1)A、D、G均为氧化物且D、G常温常压下为气体。则A与D反应的化学方程式为
;
(2)D、G既能和盐酸反应又能和NaOH溶液反应。则A与D反应的化学方程式为:
。
26.(15分)
周期表前20号的主族元素X、Y、Z、W,原子序数依次增大,X和W位于同主族。常温常压下,只有X的单质为气体。Y、Z、W的最高价氧化物对应的水化物依次为甲、乙、丙。甲、乙、丙是中学化学中的常见物质,其中只有甲难溶于水且能和乙、丙的水溶液分别反应得到澄清溶液:乙、丙都是强电解质。根据以上信息填写下列空白:
(1)画出Z的原子结构示意图 ;
(2)甲和乙、丙的水溶液分别反应得到两种澄清溶液,将这两种澄清溶液混合时所发生反应的离子方程式为 ;
|
(4)化合物W2Z的水溶液显碱性,试用有关的离子方程式解释其原因
;
(5)用Y单质和生活中最常用的金属作电极,用导线连接后插入丙的溶液中构成原电池,该原电池负极的电极反应式为 。
13.已知:11P+15CuSO4+24H2O==5Cu3P+6H3PO4+15H2SO4。有关该反应的下列说法中正确的是 ( )
A.氧化剂和还原剂的物质的量之比为15:11
B.上述反应中的电子转移总数为15
C.1mol CuSO4参加反应时,转移电子2mol
D.Cu3P既是氧化产物又是还原产物
第Ⅱ卷(非选择题 共174分)
本卷共10题,共174分。
12.某有机物的结构简式为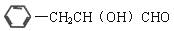 ;下列各类反应中,该有机物可能发生的是 ( )
;下列各类反应中,该有机物可能发生的是 ( )
①加成反应; ②水解反应; ③氧化反应; ④中和反应;
⑤酯化反应;
A.①④⑤ B.②③④ C.①②⑤ D.①③⑤
11.在密闭容器中进行的可逆反应为:2NO2(g)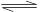 N2O4(g);△H<0。一定条件下达到平衡后,改变下列条件的有关判断错误的是 ( )
N2O4(g);△H<0。一定条件下达到平衡后,改变下列条件的有关判断错误的是 ( )
A.保持容积不变,充入NO2,平衡向右移动,NO2的体积分数减小
B.保持容积不变,充入N2O4,平衡向左移动,NO2的体积分数增大
C.保持容积不变,升高温度,容器中气体颜色加深
D.保持容积不变,充入N2使容器中压强增大,上述平衡不移动
10.下列各组离子在溶液中一定能大量共存的是 ( )
A.Na+、K+、Br-、SO32- B.Ca2+、K+、Cl-、CO32-
C.NH4+、Ba2+、OH-、NO3- D.Na+、Al3+、SO42-、HCO3-
9.NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.5.6g铁与足量稀盐酸完全反应转移的电子数为0.3NA
B.1.0L 0.20mol·L-1的NaOH溶液和氨水中OH-离子均为0.2NA
C.标准状况下,11.2L NH3与11.2LH2O2所含原子数均为2NA
D.6.0g SiO2晶体中含有Si-O键的数目为0.4NA
8.下列叙述没有错误的是 ( )
A.分子晶体中不一定含化学键 B.离子晶体中不一定含离子键
C.原子晶体中可能含离子键 D.熔化状态下不导电的物质一定是共价化合物
7.已知某离子40R+与Ar原子具有相同的核外电子排布结构,则下列说法正确的是( )
A.40R原子核内的中子数为19 B.40R原子的核外电子数为19
C.40R原子核内的质子数为21 D.R位于周期表第4周期第IIA族
6.下列说法正确的是 ( )
A.氧化物都是非电解质
B.非金属氢化物的水溶液都是无氧酸
C.溶液和胶体都是混合物
D.混合物中一定含有两种或两种以上元素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com