
25.(16分)某芳香化合物A的化学式为RX2(R代表烃基,X代表卤素原子),其相对分子质量为175,分子中碳、氢元素的质量比为12:1,含X元素的质量分数为40.6%。
请回答:

(1)卤代烃RX2的分子式 。
(2)已知:
|
②试剂X为 。
③写出反应Ⅱ的化学方程式 。
(3)检验A分子中的卤素原子,简述实验方案 。
(4)苯环上的一溴代物只有一种,与A互为同分异构体的物质有 种,写出其中一种的结构简式 。
12.常温下,关于下列溶液的叙述错误的是 ( )
A.pH=3的弱酸溶液和pH =11的强碱溶液等体积混合后溶液呈酸性
B.pH =5的硫酸溶液稀释到原来的500倍,稀释后溶液中c(SO42-)与c(H+)之比约为
1:10
C.向1L0.3mol/L的NaOH溶液缓缓通入CO2气体至溶液增重8.8g,则溶液中
2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
D.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则
C[(NH4)2SO4]>c[(NH4)2CO3]>c[(NH4)2Fe(SO4)2]
第Ⅱ卷
11.某工业生产中有一主要反应CuFeS2+4Fe3+=5Fe2++Cu2++2S。下列说法正确的是 ( )
A.氧化剂为Fe3+,还原剂为Cu2+和S2-
B.氧化产物是S,还原产物是Fe2+和Cu2+
C.当转移1mol电子时,有46g CuFeS2参加反应
D.氧化性由强到弱到顺序Fe3+>Fe2+>Cu2+
10.几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
|
元素代号 |
A |
B |
D |
E |
G |
X |
Y |
Z |
|
化合价 |
-1 |
-2 |
+4、-4 |
-1 |
+5、-3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.099 |
0.110 |
0.143 |
0.160 |
0.186 |
A.A元素的单质能将E单质从XE3的溶液中置换出来
B.A、X、Z的离子半径由大到小顺序是A->Z+>X3+
C.G元素的单质不存在同素异形体
D.Y元素的单质在DB2中燃烧生成两种化合物
9.一定条件下密闭容器中的可逆反应2A(g)+B(g)  2C(g),△H<0达到平衡后,改变一个条件x,y的变化一定符合图中曲线的是 ( )
2C(g),△H<0达到平衡后,改变一个条件x,y的变化一定符合图中曲线的是 ( )

①再加入C,A的体积分数的改变情况
②缩小体积,A的转化率的改变情况
③保持压强不变通入少量He,B的物质的量改变情况
④升高,混合气体的平均相对分子质量的改变情况
A.①② B.②③ C.③④ D.②④
8.为达到预期的实验目的,下列方法可行的是 ( )
A.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
B.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
C.可用水鉴别己烷、四氯化碳、乙醇三种无色液体
D.向混有乙酸的乙酸乙酯中加入NaOH溶液再分液,提纯乙酸乙酯
7.将1mol NaHCO3和1mol Na2O2固体混合,在加热的条件下使其充分反应,则最后所得固体为 ( )
A.1mol Na2CO3和1mol NaOH B.lmol Na2CO3和2molNaOH
C.2mol Na2CO3和2molNaOH D.2mol Na2CO3
6.用NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.1mol Na2O2中阴阳离子的总数为4NA
B.标准状况下,22.4L CCl4含有的共价键数为4NA
C.标准状况下,14g N2含有的核外电子数为5NA
D.3mol铁与足量的水蒸气充分反应,转移8NA个电子
5.下列叙述正确的是 ( )
A.90℃时水的离子积 ,此时水的pH<7
,此时水的pH<7
B.镀锡铁制品的镀层破损后仍能对铁制品起保护作用
C.依据溶液导电能力的大小,将电解质分为强、弱电解质
D.非金属氧化物和水反应一定没有气体产生
31.[化学--有机化学基础](13分)
咖啡酸苯乙酯(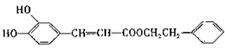 )是一种天然抗癌药物,在一定条件下能发生如下转化:
)是一种天然抗癌药物,在一定条件下能发生如下转化:
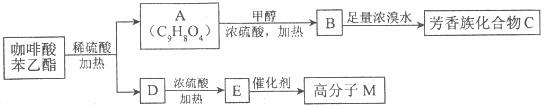
请填写下列空白。
(1)D分子中的官能团是___________。
(2)高分子M的结构简式是___________。
(3)写出A→B反应的化学方程式:___________
(4) B→C发生的反应类型有___________。
(5)A的同分异构体很多种,其中,同时符合下列条件的同分异构体有_______种。
①苯环上只有两个取代基; ②能发生银镜反应;
③能与碳酸氢钠溶液反应; ④能与氯化铁溶液发生显色反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com