
7.X、Y、Z三种主族元素,X+和Y-两种离子具有相同的电子层结构,Z原子核内质子数比Y原子核内质子数少9个,Y-在一定条件下可被氧化生成YZ3-离子。下列说法正确的是
( )
A.离子半径X+>Y- B.X、Y、Z均属于短周期元素
C.化合物XYZ的溶液具有漂白性 D.Y属于第ⅤA族元素
6.下列实验现象的解释正确的是
|
|
实验现象 |
解释 |
|
A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
淀粉能与Cl2发生显色反应 |
|
B |
浓硝酸在光照条件下变黄 |
浓硝酸见光分解,生成NO2溶于浓硝酸 |
|
C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
一定是由于该溶液中含有SO42- |
|
D |
铜片放入冷的浓硫酸中,无明显变化 |
铜在冷的浓硫酸中发生钝化 |
5.已知阿伏加德罗常数的值为NA,下列说法正确的是 ( )
A.1 mol CH3+(甲基碳正离子)含有的电子数目为9NA
B.7.2g C5H12含有的C-C键的数目为0.5 NA
C.14 g N2和CO的混合气体含有的分子数目为0.5 NA
D.标准状况下2.24L甲苯含有的碳原子数目为0.7 NA
4.三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体。它无色、无臭,在潮湿的空气中能发生下列反应:3NF3+5H2O=2NO+HNO3+9HF下列有关说法正确的是( )
A.反应中NF3是氧化剂,H2O是还原剂
B.反应中被氧化与被还原的原子物质的量之比为2∶1
C.若反应中生成0.2mol HNO3,则反应共转移0.2mol e-
D.NF3在潮湿空气中泄漏会产生白雾、红棕色气体等现象
3.常温下,在pH=1的水溶液中能大量共存的离子组是 ( )
A.Na+、Mg2+、SO42-、Cl- B.Al3+、NH4+、CH3COO-、Br-
C.K+、Fe2+、SO42-、NO3- D.Na+、Ba2+、I-、ClO-
2.下列实验不能达到目的的是 ( )
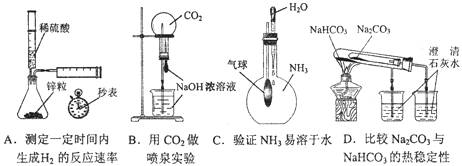
1.2008年诺贝尔化学奖授予钱永键等三位科学家,以表彰他们在发现和研究绿色荧光蛋白(一种蛋白质,简称GFP)方面做出的杰出贡献。下列有关GFP的说法错误的是( )
A.属于高分子化合物 B.遇到CuSO4溶液会发生盐析
C.水解后可得到多种氨基酸 D.可用于蛋白质反应机理的研究
28.(14分)中学化学中几种常见物质的转化关系如图所示。已知A固体由两种元素组成,B是非金属单质,G是金属单质,F的相对分子质量比D大16(部分反应物、生成物未列出)。反应①是工业上制取K的重要反应,反应②为化合反应。
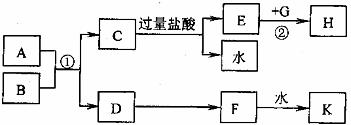
请回答:
(1)工业上反应①在 (填工业设备名称)中进行,反应①的化学方程式为 。
(2)将反应②设计成原电池,正极的反应式为 。
(3)将E的饱和溶液滴入沸水中的离子方程式为 。
(4)实验室中保存少量H溶液可采取的措施 ,简述原因 。
(5)写出H溶液和过量过氧化钠反应的化学方程式 。
27.(16分)某校研究性学习小组选择使用下列仪器和药品,验证铜和适量浓硝酸反应除生 成NO2外,还生成少量的NO(实验中使用的N2和O2的用量可自由控制)。已知:
①NO+NO2+2OH2-=2NO2-+H2O
②气体液化温度: NO2 21℃ NO -152℃
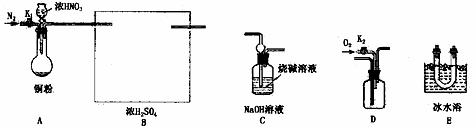
请回答:
(1)写出铜与浓硝酸反应的化学反应方程式 。
(2)装置B的作用是 ,在上图方框内画出B装置。
(3)写出装置的连接顺序(填字母):A接B接 。
(4)实验开始前要先打开A装置中的活塞K1,持续通一段时问氮气后再关闭活塞K1,目的是 。A中的反应停止后,打开D中的活塞K2,并通人氧气,若反应中确有NO产生,则D中出现的现象是 。
(5)如果O2过量,则装置C中发生反应的离子方程式是 。
(6)若铜粉中混入了少量的Ag,已知铜粉质量为a g,反应后固体完全溶解,要测定铜粉中铜的质量分数,只需利用A装置中反应后的溶液进行简单的实验操作,就可以达到实验目的。试简述实验方案 。
26.(14分)已知A、B、C、D、E为原子序数递增的五种短周期元素,A与C、B与D同主族。
请回答:
(1)C2B2的电子式 ,A2B2属于 晶体(填“分子”、“原子”或“离子”)。
(2)甲装置是离子交换膜法电解饱和CE溶液的原理示意图。透过交换膜的离子a是 ,电解的离子方程式 。
(3)为检验E2的性质,某同学做了如下实验:
①Cu丝在E2中燃烧的现象 ,你认为Fe丝在E2也可燃烧的理由是 。
a.Fe与Cu都是金属元素 b.Fe的熔点比Cu高
c.Fe的密度比Cu小 d.Fe的金属性比Cu强
②将乙装置放置在光亮的地方(日光未直射),一段时间后,观察到量筒内壁上有油状液滴生成,量筒内气体颜色变浅等。生成物有 种,水槽中的液体用饱和CE溶液而不用水的原因是 。
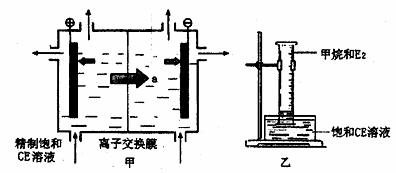
(4)D的单质能跟C的最高价氧化物对应的水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式 。
(5)用铂作电极电解lL含有0.4mol CuDB4和0.2molCE的水溶液,一段时间后,在一个电极上得到了0.3mol Cu,在另一电极上析出的气体在标况下的体积是 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com