
9.下列有关溶液的说法正确的是 ( )
( )
A.在加入Al粉能产生大量H2的溶液中,下列离子一定能大量存在:
K+、Na+、Cl-、NO-3
B.在NaHCO3溶液中加入足量的NaAlO2,发生的反应的离子方程式为
HCO-3+AlO-2+H2O=Al(OH3)↓+CO2-3
C.一定浓度的 溶液呈碱性,则此溶液中各离子浓度由大到小排列正确的是
溶液呈碱性,则此溶液中各离子浓度由大到小排列正确的是
c(K+)>c(HB-)>c(B2-)>c(OH-)>c(H+)
D.10 0.1mol/L的NaOH溶液与10mL0.2mol/L的CH3COOH溶液混合后有
0.1mol/L的NaOH溶液与10mL0.2mol/L的CH3COOH溶液混合后有
2c(OH-)+c(CH3COO-)=2c(H+)+2c(CH3COOH)
8.若用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
( )
A.常温常压下,11.2L甲醛气体所含的质子数为8NA
B.常温常压下,1Llmol/L的H2SO4溶液所含的 的个数为2NA
的个数为2NA
C.对于分子式均为C8H18的烷烃,它有多种同分异构体,不同的异构体之间所含的C-H 键的数目和C-C键的数目均相等
键的数目和C-C键的数目均相等 
D.17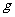 氨气溶于水,得到NH3·H2O的分子数为NA
氨气溶于水,得到NH3·H2O的分子数为NA
7.下列各组物质中,因反应条件、用量、浓度等不同而发生不同化学反应的是 ( )
( )
①C与O2,②P与Cl2,③Fe与S,④Na与O2,⑤CO2与NaOH,⑥Cu与硝酸,⑦AgNO3 与氨水,⑧AlCl3溶液与氨水,⑨NaAlO2与盐酸,⑩Na2CO3与盐酸
与氨水,⑧AlCl3溶液与氨水,⑨NaAlO2与盐酸,⑩Na2CO3与盐酸
A.除③⑨外 B.除③⑧外 C.除③⑦⑩外 D.除⑥⑦⑧外
6.下列有关叙述正确的是 ( )
( )
A.食用油若长期放置有一种哈喇味产生时,只需将油重新加热后仍可继续食用
B.糖类都可以用通式 表示
表示 
C.高纯度的石英是一种极为优良的新型材料,它属于硅酸盐材料
D.同一物质溶于不同的物质可形成不同的分散系,如将NaCl溶于水可形成溶液,溶于酒精则可形成胶体

29.(15分)食用香料A分子中无支链,B分子中无甲基。B能使Br2的CCl4溶液褪色,1 molB与足量Na反应生成0.5 molH2。各物质间有如下转化。

试回答:
(1)在一定条件下能与C发生反应的是__________________。
a.Na b.Na2CO3 c.Br2/CCl4 d.CH3COOH
(2)D分子中的官能团名称是_________,E的结构简式是______________。
(3)B与F反应生成A的化学方程式是___________________________。
(4)F的同分异构体甲能发生水解反应,其中的一种产物能发生银镜反应;另一产物在光照条件下的一氯取代物只有两种,且催化氧化后的产物也能发生银镜反应。甲的结构简式是_________________________。
(5)已知:乙是C的同系物,其催化氧化的产物在常温下为气态。由乙出发可以合成有机溶剂戊(C7H14O3)。丁分子中有2个甲基。
戊的结构简式是__________________________。


28.(16分)固体粉末X由Fe2O3、CuO组成。某研究性学习小组选用下图装置(夹持仪器已略去,实验前均已检查装置气密性)探究X与炭粉的反应。
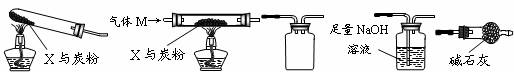
甲 乙 丙 丁 戊
请回答:
|
(2)为使实验测得的数据更能准确说明问题,一些同学按乙→丁→戊的顺序连接装置进行实验,并且加热前先通一会儿气体M,停止加热后再通一会儿该气体。
①气体M可能是 (填字母)。
a. CO2 b. H2 c. N2 d. CO e. O2
②停止加热后再通一会儿气体M的原因是 。
(3)以上两套装置均存在的同样的明显缺陷是 。
(4)该小组同学又设计了如下实验将X进行转化(每一步均反应完全):
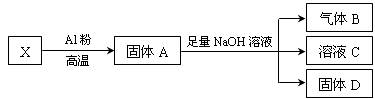
①生成气体B的化学方程式是 。
②将固体D投入过量稀硫酸并充分反应后,过滤,再向滤液加入双氧水,得黄色溶液。写出当加入双氧水时溶液中发生反应的离子方程式: 。
③若已知固体X的质量为7.2 g ,反应中Al粉的质量是2.7 g,气体B在标准状况下的体积为672 mL,则固体D的质量是 g。
27.(15分)主族单质A、B、C有如下转化关系,常温下B是有色气体,A为金属。在化合物F中,A元素以A2+方式存在,A2+有5个电子层,且最外层有两个电子。
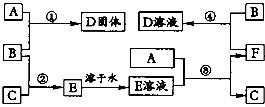
试回答下列问题:
(1)A元素在周期表中位置为
(2)用电子式表示E的形成过程
(3)写出反应③的离子方程式(F是可溶性强电解质)。
(4)测得0.1mol/L的D溶液的pH<7,且固体D遇水蒸气立刻产生白雾。
①用广泛pH试纸测pH的操作是
②如何用D固体配D溶液?
③同温度下,pH相等的D溶液和E溶液中,水的电离程度的关系是D E(填“大于”、“小于”或“等于”)。
26.(14分)根据下列事实,推断相关元素,并回答有关问题。
信息1:常见的短周期元素A、B、C、D,原子序数依次增大,它们的单质在常温下都是固态。
信息2:它们的最高价氧化物(相对分子质量都大于30)有两种可以溶解于盐酸,三种可以溶解于NaOH溶液。
信息3:将它们单质的混合物ag溶解于足量盐酸,过滤后向滤液中加过量NaOH溶液,最后有白色不溶物,过滤得溶液甲。
信息4:将它们单质的混合物ag溶解于足量NaOH溶液,过滤后向滤液中加过量盐酸,最后有白色不溶物,过滤得溶液乙。
信息5:A和D同主族。
试回答下列问题:
(1)只根据信息1可以判断一定不可能是S元素的是 。
(2)根据信息2可以推断出一定有 元素。
根据信息3可以推断出一定有 元素。
根据信息4可以推断出一定有 元素。
综合所有信息,结合信息5,可以推断出A元素是 。
(3)将溶液甲和溶液乙混合,一定会有沉淀吗? (填“一定”或“不一定”)
为什么?
(4)若信息3和信息4中所得到的气体的质量相等,可以推出混合物样品中相关单质的物质的量有何关系?
13.将一定质量的镁、铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物全部是NO)。向反应后的溶液中加入3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列叙述中正确的是 ( )
A.当生成沉淀达到最大值时,消耗NaOH溶液的体积为100mL
B.当金属全部溶解时收集到NO气体的体积为2.24L
C.参加反应的金属的总质量一定是6.6g
D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
第Ⅱ卷(非选择题)
12.已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO42-,某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是 ( )
A.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好是中性
B.水电离出的c(H+)=1×10-10mol/L
C.c(H+) = c (OH-) + c (SO42-)
D.该温度高于25℃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com