
12.有关下图所示化合物的说法不正确的是
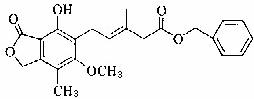
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1mol该化合物最多可以与3molNaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
11.为了检验某含有NaHCO3杂质的Na2CO3样口的纯度,现将w1g样品加热,其质量变为w2g,则该样口的纯度(质量分数)是
A.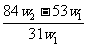 B.
B.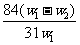 C.
C.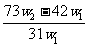 D.
D.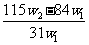
10.用0.10mol·L-1的盐酸0.10mol·L-1的氨水,滴定过程中不可能表现的结果是
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
C.c(Cl-)>c(NH4+),c(OH-)>c(H+)
D.c(Cl-)=c(NH4+-),c(H+)>c(OH+)
9.现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是
A. 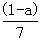 B.
B.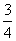 a C.
a C.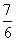 (1-a) D.
(1-a) D.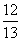 (1-a)
(1-a)
8.下列表示溶液中发生反应的化学方程式错误的是
A.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
B.2KMnO4+HCOOK+KOH=2K2MnO4+CO2↑+H2O
C.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D.K2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+K2SO4+7H2O
7.将15mL、2mol·L-1Na2CO3溶液逐滴加入到40mLl0.5mol·L-1MCln盐溶液中,恰好将溶液中的Mn+离子沉淀为碳酸盐,则MCln中n值是
A.4 B.3 C.2 D.1
6.下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是
A.Ba2+、NO-3、NH4+、Cl-
B.Ca2+、HCO3-、NH4+、AlO3-
C.K+、Ba2+、Cl-、HSO3-
D.Mg2+、NH4+、SO42-、K+
30.(15分)(注意:在试题卷上作答无效)
化合物H是一种香料,存在于金橘中,可用如下路线合成:
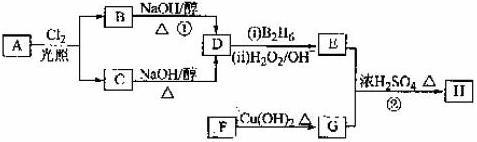
已知:R-CH=CH2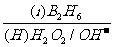 RCH2CH2OH(B2H6为乙硼烷).
RCH2CH2OH(B2H6为乙硼烷).
回答下列问题:
(1)11.2 L(标准状况)的烃A在氧气中充分燃烧可以产生88 gCO2和45 gH2O。
A的分子式是 ;
(2)B和C均为氯化烃,它们的名称(系统命名)分别为
;
(3)在催化剂存在下1 mol F与2 mol H2反应,生成3-苯基-1-内醇。F的结构简式是 ;
(4)反应①的反应类型是 ;
(5)反应②的化学方程式为 ;
(6)写出所有与G具有相同官能团的G的芳香类同分异构体的结构简式: 。
29.(15分)(注意:在试题卷上作答无效)
已知周期表中,元素Q、R、W、相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是 ;
(2)Q的具有相同化合价目可以相互转变的氧化物是 ;
(3)R和Y形成的二元化合物,R呈现最高化合价的化合物的化学式:
;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是
。
②电子总数相同的氢化物的化学式和立体结构分别是
;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氢化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCl气体;W(OH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是
28.(15分)(注意:在试题卷上作答无效)
下图所示装置中,甲、乙、丙,烧杯依次分别盛放100 g 500%的NaOH溶液、足量的CuSO4溶液100 g 10.00%的K2SO4溶液,电极均为石墨电极。
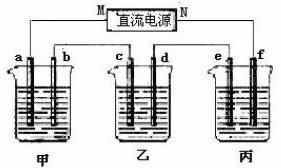
(1)接通电源,经过一后,测得丙中K2SO4溶度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为 极;
②电极b上发生的电极反应为 ;
③列式计算电极b上生成的气体在标准状况下的体积:
;
④电极c的质量变化是 g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液 ;
乙溶液 ;
丙溶液 ;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com