
28.(16分)
提示:

有机物A(C18H17NO5)是一种镇痛解热药品,其结构简式为:
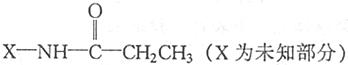
由它可衍生出一系列物质,有关变化如图:
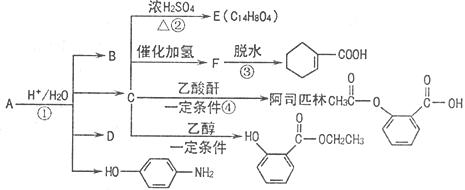
(1)B和D的关系是 (填“同种物质”、“同系物”、“同分异构体”)。
(2)写出E的结构简式: ;反应②的反应类型是 。
(3)写出反应③的化学方程式: 。
(4)A的结构简式是 ;1molA在氢氧化钠溶液中水解,最多消耗氢氧化钠 mol。
(5)能与FeCl3溶液发生显色反应,且属于酯类的C的同分异构体有多种,写出其中一种的结构简式 。
27.(15分)
物质之间的转化如下图所示,A可作为工业生产J的原料,B、C、H、I为非金属单质,C是固体,B、H、I为气体。X的水溶液为一种常见的无色医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见有机氮肥[CO(NH2)2],反应⑦中L与M的物质的量之比为1:2,设备I中发生的是工业制M的化学反应。回答下列问题:

(1)X的电子式为 。
(2)反应②是工业制H的化学反应,写出该反应的化学方程式: 。
(3)写出反应⑦的化学方程式: 。
(4)为提高工业合成M的产率,可采取的措施是 、 、 。
(5)写出E气体通入FeCl3溶液中发生反应的离子方程式:
。
13.将agCuO和Fe3O3的混合物分成质量相同两等份,向其中一份中加入bmL cmol/L的稀硫酸正好完全反应;另一份在加热的条件下用H2还原,反应完全时用去H2 dL(折算成标准状况)。则d等于 ( )
A.22.4bc×10-3
B.44.8bc×10-3
C.22.4(3a-4bc×10-3)
D.22.4(3a-4bc)×10-3
第Ⅱ卷(非选择题 共174分)
A、B、C、X、Y、Z均是由短周期元素的原子构成的分子。均含有10个电子的A、B、C在一定条件下能依次转变为均含有14个电子的X、Y、Z。单质X是空气的主要成分之一,B不完全燃烧生成气体Y。常温下,C是一种常见的无色液体,Z是由4个原子构成的直线型分子。请回答:
(1)B分子的空间构型是 。
(2)Y在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
。
(3)写出A与CuO在一定条件下反应生成X的化学方程式:
。
(4)若Z燃烧热为1300Kj·mol-1,则Z燃烧的热化学方程式为:
(5)由构成X单质的元素的最高价氧化物对应水化物与A化合生成的物质的水溶液呈
(填“酸性”、“碱性”、“中性”),用离子方程式表示其原因
。
12.室温下,某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
A.加入适量的NaOH后,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c (H+)
B.该溶液可能由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.该溶液可能由pH=3的CH3COO-与pH=11的NaOH溶液等体积混合而成
D.加放适量的氨水后,c(CH3COO-)一定大于c(Na+)、c(NH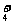 )之和
)之和
11.依他尼酸结构简式如图所示,它是一种在体育比赛中被禁用的兴奋剂,下列有关叙述正确的是 ( )

A.依他尼酸属于芳香族化合物,分子式为C13H12Cl2O4
B.依他尼酸分子中的所有原子可能共平面
C.1 mol依他尼酸与足量NaOH溶液共热反应,最多消耗3 mol NaOH
D.1 mol依他尼酸与足量H2在Ni粉存在下加热反应,最多消耗6 mol H2
10.滴有酚酞和氯化钠溶液的湿润滤纸分别做如图所示的甲、乙两个实验,能发现附近变成红色的电极是 ( )

A.a和c B.b和d
C.a和d D.b和c
9.某温度下,1molA和2molB在一个密闭容器中发生如下反应:
A(g)+2B(g) 2C(g),一段时间后达到平衡,生成n molC。则下列说法正确的是 ( )
2C(g),一段时间后达到平衡,生成n molC。则下列说法正确的是 ( )
A.物质A、B的转化率之比为1:2
B.起始时刻和达到平衡后容器中的压强比 3:(3-n)
C.若升高温度,A的体积分数增大,则该反应的△H>0
D.当2u正(A)=u逆(B)时,可确定反应达到平衡
8.设NA表示阿伏加德罗常数,下列叙述正确的是 ( )
A.常温常压下,32gO2和O3的混合气体中氧原子数为2NA
B.含有1mol碳原子的金刚石中,C-C共价键数为4NA
C.1molFeCl3完全水解转化为氢氧化铁胶后能生成NA个胶粒
D.分解H2O2制取O2,每生成1molO2转移的电子数为4NA
7.下列说法正确的是 ( )
A.同主族元素的原子半径越大,其单质的熔点越高
B.同温同压下,3molC2H2(g)和1molC6H6(g)的密度相等
C.同周期非金属元素的氧化物对应的水化物的酸性从左到右依次增强
D.生成物只有一种的化学反应不一定是化合反应
6.叠氮化钠(NaN3)是抗禽流感药物“达菲”合成过程中的中间活性物质,3molNaN3受撞击会生成Na3N和4mol氮气。下列有关叙述错误的是 ( )
A.NaN3受撞击时,NaN3既是氧化剂又是还原剂
B.NaN3跟水反应时,有NH3生成
C.Na3N中N3-半径比Na+半径大
D.Na3N是离子化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com