
26Θ°(14Ζ÷)»γΆΦΥυ ΨΒΡΉΣΜ·ΙΊœΒ÷–ΗςΈο÷ Ψυ «÷–―ßΜ·―ß÷–ΒΡ≥ΘΦϊΈο÷ Θ§A «Κ§”–ΫαΨßΥ°ΒΡ―ΈΘ§GΓΔKΈΣΙΧΧεΒΞ÷ Θ§HΈΣΈό…ΪΤχΧεΒΞ÷ Θ§CΈΣΚλΉΊ…ΪΖέΡ©Θ§Ω…”ΟΉω”ΆΤαΒΡ―’ΝœΘ§B≥ΘΉωΡΆΜπ≤ΡΝœΓΘ
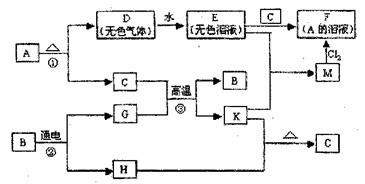
ΓΓΓΓΓΓ «κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΓΓ (1)DΒΡΒγΉ” ΫΈΣΓΓΓΓΓΓΓΓ Θ§BΒΡΙΧΧε τ”ΎΓΓΓΓΓΓΓΓ ΨßΧεΓΘ
ΓΓ (2)AΒΡΥ°»ή“Κ≥ Υα–‘Θ§Τδ‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)
ΓΓ (3)–¥≥ωœ¬Ν–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ
MΓζFΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
B”κNaOH»ή“ΚΖ¥”ΠΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ (4)¥”ΡήΝΩ±δΜ·ΒΡΫ«Ε»Ω¥Θ§ΔΌΔΎΔέΖ¥”Π÷– τ”ΎΓςH<0ΒΡΖ¥”Π «ΓΓΓΓΓΓΓΓ ΓΘ(Χν–ρΚ≈)
13Θ°b gΡ≥Ϋπ τ”κΉψΝΩΒΡœΓΝρΥαΖ¥”ΠΘ§…ζ≥…ΗΟΫπ τΒΡ»ΐΦέ’ΐ―ΈΚΆa g«βΤχΓΘΗΟΫπ τΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°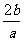 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ° ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ°
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΘ° ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°
ΒΎΔρΨμ(Ζ«―Γ‘ώΧβ Ι≤174Ζ÷)
12Θ°‘Ύ“ΜΨχ»»ΒΡΕ®»ίΟή±’»ίΤς÷–Θ§”–Ω…ΡφΖ¥”ΠA(g) °2B(g)ΓΓΓΓ C(s)+3D(g)ΘΜΓςH<0Θ§Β±―Γœν÷–ΒΡΈοάμΝΩ≤Μ‘Ό±δΜ· ±Θ§±μΟςΗΟΖ¥”Π¥οΤΫΚβΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓ ΓΓΓΓ AΘ°ΜλΚœΤχΧεΒΡΈ¬Ε»ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°ΤχΧεΒΡΉήΈο÷ ΒΡΝΩ
ΓΓ ΓΓΓΓ CΘ°ΜλΚœΤχΧεΒΡ―Ι«ΩΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°A”κBΒΡ≈®Ε»±»
11Θ°ΕΧ÷ήΤΎXΓΔYΝΫ‘ΣΥΊΘ§X‘ΣΥΊ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ”κ¥ΈΆβ≤ψΒγΉ” ΐ÷°≤νΒΡΨχΕ‘÷ΒΒ»”ΎΒγΉ”≤ψ ΐΘ§Y‘ΣΥΊ‘≠Ή”±»x‘≠Ή”Εύ2ΗωΒγΉ”Θ§œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°‘≠Ή”ΑκΨΕX>YΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°ΒΞ÷ ΒΡ»έΒψX>Y
ΓΓ ΓΓΓΓ CΘ°XΚΆYΩ…–Έ≥…άκΉ”Μ·ΚœΈοΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°XΚΆYΩ…–Έ≥…Μ·ΚœΈοXY3
10Θ°NA±μ ΨΑΔΖϋΌΛΒ¬¬ό≥Θ ΐΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓ ΓΓΓΓ AΘ°Ά≠ΓΔ–ΩΚΆœΓΝρΥαΙΙ≥…ΒΡ‘≠Βγ≥ΊΘ§Β±ΉΣ“ΤNAΗωΒγΉ” ±Θ§ΗΚΦΪ≤ζ…ζΒΡΤχΧε‘Ύ±ξΩωœ¬ΒΡΧεΜΐ‘ΦΈΣ11.2L
ΓΓ ΓΓΓΓ BΘ°1.5mol“Μ―θΜ·ΧΦΚΆΕΰ―θΜ·ΧΦΜλΚœΤχΧεΥυΚ§”–ΒΡΧΦ‘≠Ή” ΐΈΣ1.5NA
ΓΓ ΓΓΓΓ CΘ°±ξΉΦΉ¥Ωωœ¬Θ§0.5NAΗωC5H12Ζ÷Ή”ΒΡΧεΜΐ‘ΦΈΣ11.2L
ΓΓ ΓΓΓΓ DΘ°1L 0.1molΘ·LΒΡ¥ΉΥα»ή“Κ÷–ΥυΚ§άκΉ”ΚΆΖ÷Ή”Ήή ΐ «0.1NA
9Θ°Ε଻̷ΕΰΝρ(S2Cl2) «ΙψΖΚ”Ο”ΎœπΫΚΙΛ“ΒΒΡΝρΜ·ΦΝΘ§ΤδΖ÷Ή”ΫαΙΙ»γœ¬ΆΦΥυ ΨΓΘ≥ΘΈ¬S2Cl2 «“Μ÷÷≥»ΜΤ…ΪΒΡ“ΚΧεΘ§”ωΥ°“ΉΥ°ΫβΘ§≤Δ≤ζ…ζΡή ΙΤΖΚλΆ …ΪΒΡΤχΧεΓΘœ¬Ν–ΥΒΖ®÷–¥μΈσΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )

ΓΓ ΓΓΓΓ AΘ°S2Cl2ΒΡΫαΙΙ ΫΈΣCl-S-S-Cl
ΓΓ ΓΓΓΓ BΘ°S2Cl2”κH2OΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΩ…ΡήΈΣΘΚ
ΓΓΓΓ ΓΓ2S2C12+2H2O=SO2Γϋ+3SΓΐ+4HCl
ΓΓ ΓΓΓΓ CΘ°S2Br2”κS2C12ΫαΙΙœύΥΤΘ§»έΖ–ΒψΘΚS2Br2>S2C12
ΓΓ ΓΓΓΓ DΘ°S2Cl2ΈΣΚ§”–ΦΪ–‘ΦϋΚΆΖ«ΦΪ–‘ΦϋΒΡΖ«ΦΪ–‘Ζ÷Ή”
8Θ°œ¬Ν–Μ·―ß”Ο”ο±μ Ψ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°Ϋπ τMg”κHF»ή“ΚΖ¥”ΠΘΚ
ΓΓΓΓΓΓ BΘ°‘ΎΦ”»»ΧθΦΰœ¬Θ§Ά≠Τ§”κ≈® Ζ¥”ΠΘΚ
Ζ¥”ΠΘΚ

ΓΓΓΓΓΓ CΘ°‘ΎNH4Cl”κΑ±Υ°ΜλΚœΚσΒΡΦν–‘»ή“Κ÷–ΘΚ ΘΨ
ΘΨ
ΓΓΓΓΓΓ DΘ°”ΟΧζΉςΒγΦΪΒγΫ⬻̷ΡΤ»ή“ΚΘΚ

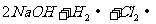
7Θ°œ¬Ν–”–ΙΊ Β―ι≤ΌΉς’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )

ΓΓΓΓΓΓ AΘ°≥ΤΝΩ«β―θΜ·ΡΤΙΧΧεΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓ BΘ°Φλ―ιΧζΖέ”κΥ°’τΤχΖ¥”Π≤ζ…ζΒΡ«βΤχ
ΓΓΓΓΓΓ CΘ°≈δ÷Τ200mL0.10mol/L―ΈΥαΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓ DΘ°Ζ÷άκΝΫ÷÷ΜΞ»ήΒΪΖ–Βψœύ≤νΫœ¥σΒΡ“ΚΧεΜλΚœΈο
6Θ°ΟάΙζΩΤ―ßΦ“¬μΕΓΓΛ≤ιΖ«(Martin Chalfie)ΓΔΟάΙζΜΣ“αΜ·―ßΦ“«°”άΫΓ(Roger Tsien)“‘ΦΑ»’±ΨΩΤ―ßΦ“œ¬¥ε–ό(Osamu Shimomura)“ρΖΔœ÷ΚΆ―–ΨΩ¬Χ…Ϊ”ΪΙβΒΑΑΉ(green fluorescent protein, GFP)ΕχΜώ2008ΡξΕ»≈Β±¥ΕϊΜ·―ßΫ±ΓΘGFP‘ΎΉœΆβœΏ’’…δœ¬ΜαΖΔ≥ωœ ―ό¬ΧΙβΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓΓΓ )
ΓΓΓΓΓΓ AΘ°÷ΊΫπ τάκΉ”Ρή ΙGFP±δ–‘ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°Χλ»ΜΒΑΑΉ÷ τ”Ύ¥ΩΨΜΈο
ΓΓΓΓΓΓ CΘ°GFPΖΔ≥ω”ΪΙβ «ΒΑΑΉ÷ ΒΡ―’…ΪΖ¥”ΠΓΓΓΓ DΘ°ΒΑΑΉ÷ Ά®≥Θ”Ο–¬÷Τ«β―θΜ·Ά≠Φλ―ι
29Θ°(15Ζ÷)
ΓΓΓΓ Ρ≥ΩΈΆβ Β―ι–ΓΉι…ηΦΤΝΥ»γΆΦΥυ ΨΉΑ÷ΟΫχ––ΓΑ“ΜΤςΕύ”ΟΓ±ΒΡ Β―ιΧΫΨΩ(Φ–≥÷ΉΑ÷Ο“―¬‘»Ξ)ΓΘ

ΓΓ (1)ΗΟ–ΓΉιΆ§―ß”ΟΗΟΉΑ÷ΟΫχ––ΓΑH2ΒΡ÷Τ»ΓΦΑ»Φ…’–‘÷ ―ι÷ΛΓ± Β―ιΓΘΥϊΟ«…ηΦΤΝΥ»γœ¬ΒΡ Β―ι≤Ϋ÷ηΘΚ
ΓΓΓΓΓΓΓΓ aΘ°ΉιΉΑΉΑ÷Ο≤ΔΦλ≤ιΤχΟή–‘
bΘ°ΉΑ»κ“©ΤΖΘ§ΙΊ±’Μν»ϊmΚΆnΘ§ΙΧΕ®‘ΎΧζΦήΧ®…œ
cΘ°¥ρΩΣΖ÷“Κ¬©ΕΖΜν»ϊmΘ§ ΙΖ¥”ΠΩΣ Φ
dΘ°Β±Ιέ≤λΒΫB÷–”–ΫœΕύΤχΧε ±Θ§¥ρΩΣΜν»ϊn≤ΔΒψ»ΦΤχΧε
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ“‘…œΡ≥≤Ϋ÷η÷–”–“Μ¥ΠΟςœ‘ΒΡ≤ΌΉς¥μΈσΘ§«κ÷Η≥ω¥μΈσ÷°¥ΠΘΚ
ΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
ΔΎΗΟ–ΓΉιΆ§―ß‘ΎΫχ––c≤Ϋ÷η≤ΌΉς ±Θ§ΖΔœ÷Ζ÷“Κ¬©ΕΖ÷–ΒΡ»ή“Κ≤ΜΡήΒΈœ¬Θ§Ρψ»œΈΣΩ…ΡήΒΡ‘≠“ρ”–ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ (2)ΗΟΉΑ÷ΟΜΙΩ…”Ο”Ύ÷Τ»Γ≤Δ ’Φ·…ΌΝΩΤδΥϊΤχΧεΘ§”ΟΉ÷ΡΗ¥ζΚ≈ΧνΩ’ΓΘ
ΓΓ ΓΓΓΓΓΓΔΌœ¬Ν–ΤχΧε÷–ΡΡ–©Ω…“‘”ΟΗΟΉΑ÷Οά¥÷Τ»ΓΚΆ ’Φ·ΘΩ
ΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜ
ΔΎ»τΫΪΉΑ÷ΟB÷–ΒΡΥ°ΜΜ≥…CCl4Θ§œ¬Ν–ΤχΧε÷–ΡΡ–©Ω…“‘”ΟΗΟΉΑ÷Οά¥÷Τ»ΓΚΆ ’Φ·ΘΩ
ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
AΘ°O2ΓΓΓΓΓΓΓΓ BΘ°NOΓΓΓΓΓΓΓΓ CΘ°SO2ΓΓΓΓΓΓΓΓ DΘ°NH3ΓΓΓΓ EΘ°C2H2 ΓΓΓΓFΘ°C2H4
ΓΓ (3)ΗΟ–ΓΉιΆ§―ß”ΟΗΟΉΑ÷ΟΫχ––Ε®ΝΩ Β―ιΘ§“‘»ΖΕ®Ρ≥Έ»Ε®±ΞΚΆ÷§ΖΨ¥ΦΒΡΫαΙΙΓΘ
ΓΓΓΓΓΓΓΓ ΔΌΖ¥”Π«ΑΘ§œ»Ε‘ΝΩΤχΙήΫχ––ΒΎ“Μ¥ΈΕΝ ΐΘ§ΕΝ ΐΈΣ40.0mLΘ§»ΜΚσ‘ΎA÷–Φ”»κ5g NaΚΆ0.62g¥ΐ≤β¥ΦΘ§≥δΖ÷Ζ¥”ΠΚσΘ§ά以÷Ν “Έ¬Κσ‘ΌΫχ––ΒΎΕΰ¥ΈΕΝ ΐΘ§ΕΝ ΐΈΣ264.0mL(Υυ”– ΐΨίΨυ“―ΜΜΥψ≥…±ξΉΦΉ¥ΩωΒΡ ΐ÷Β)ΓΘΕΝ ΐ ±“ΣΉΔ“βΒΡ «ΘΚ“Μ « Ι ”œΏ”κΑΦ“ΚΟφΉνΒΆ¥ΠœύΤΫΘΜΕΰ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΔΎΈΣΝΥΫχ“Μ≤Ϋ»ΖΕ®ΗΟ¥ΦΒΡΫαΙΙΘ§”÷ΫΪ0.62gΗΟ¥Φ≥δΖ÷»Φ…’Θ§Ω……ζ≥…0.02molCO2ΚΆ0.03molH2OΘ§“―÷ΣΝΫΗωΜρ’ΏΝΫΗω“‘…œΒΡτ«ΜυΝ§‘ΎΆ§“ΜΗωC‘≠Ή”…œ≤ΜΡή–Έ≥…Έ»Ε®ΒΡ¥ΦΘ§ΗυΨί…œ ω–≈œΔΦΤΥψ»ΖΕ®ΗΟ±ΞΚΆ¥ΦΒΡΫαΙΙΦρ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com