
8£Æœ¬¡–∏˜◊È¿Î◊”‘⁄∏¯∂®Ãıº˛œ¬ƒÐ¥Û¡øπ≤¥Êµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °°°° A£Æ∫¨”–¥Û¡øClO-µƒ»Ð“∫£∫SO42-°¢NH4+°¢Na+°¢H+
°° °°°° B£Æc(H+)£æc(OH-)µƒ»Ð“∫£∫K+°¢AlO2-°¢HCO3-°¢Na+°¢
°°°°°° C£Æ∫¨”–¥Û¡øSO42-µƒ»Ð“∫£∫C6H5O-°¢OH-°¢NO3-°¢K+
°° °°°° D£Æ∫¨”–¥Û¡øFe3+µƒ»Ð“∫£∫Na+°¢Mg2+°¢Cl-°¢SCN-
7£Æœ¬¡–– ˆ’˝»∑µƒ «(NA±Ì æ∞¢∑¸º”µ¬¬Þ≥£ ˝÷µ)°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °°°° A£Æ1 mol C60F60∑÷◊”÷–ú‘≠◊”÷ƺ‰π≤”√µÁ◊”∂‘ ˝Œ™90NA
°° °°°° B£Æ2.1 g DTO∑÷◊”÷–À˘∫¨÷–◊” ˝Œ™NA
°° °°°° C£Æµ»÷ ¡øµƒO2”ÎO3À˘’ºÃª˝÷Ʊ»“ª∂®Œ™3£∫2
°° °°°° D£Æƒ≥¥ø檌ÔMgÕÍ»´»ÐΩ‚‘⁄NgÀÆ÷–£¨À˘µ√»Ð“∫µƒ»Ð÷ ÷ ¡ø∑÷ ˝“ª∂®Œ™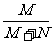
6£Æœ¬¡–—°œÓµƒ¡Ω∏ˆ¡ø÷–£¨«∞’þ“ª∂®¥Û”⁄∫Û’þµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°° °°°° A£ÆF2∫ÕBr2µƒ∑–µ„
°° °°°° B£ÆƒÕª≤ƒ¡œCaO∫ÕMgOµƒ»€µ„
°° °°°° C£Æ25°Ê ±£¨µ»Ãª˝°¢pHæ˘µ»”⁄3µƒ—ŒÀ·∫ÕA1C13»Ð“∫÷–£¨“—µÁ¿ÎµƒÀÆ∑÷◊” ˝
°° °°°° D£ÆH-∫ÕH+µƒ¿Î◊”∞Îæ∂
29£Æ(16∑÷)ƒ≥”–ª˙ªØ∫œŒÔAƒÐ∑¢…˙»Áœ¬ÕºÀ˘ æ◊™ªØ£∫
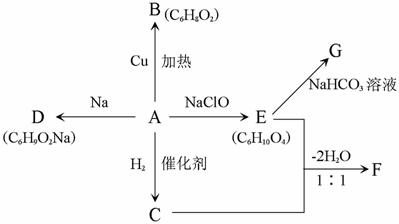
“—÷™£∫
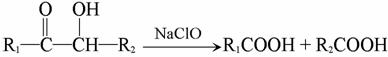
«“E∑÷◊”÷–√ª”–÷ß¡¥°£
«Îªÿ¥£∫
°° (1)Aµƒ∑÷◊” ΩŒ™£∫°°°°°°°°°°°° £ªC∫ÕE÷–∫¨”–µƒπŸƒÐÕ≈µƒ√˚≥∆∑÷±Œ™£∫°°°°°°°°°°°° °£
(2)FµƒΩ·ππºÚ ΩŒ™£∫°°°°°°°°°°°°°°°°°°°°°° £ª
(3)∑¥”¶E+C°˙Fµƒ∑¥”¶¿ý–ÕŒ™£∫°°°°°°°° £ª‘⁄A°˙Bµƒ∑¥”¶÷–£¨Cuµƒ◊˜”√Œ™£∫°°°°°°°° °£
(4)∑¥”¶A°˙Dµƒ∑Ω≥Ã ΩŒ™£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
∑¥”¶E°˙Gµƒ∑Ω≥Ã ΩŒ™£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
28£Æ(14∑÷)¡ÚÀ·—«Ã˙Ôß”÷√˚ƒ¶∂˚—Œ «“ª÷÷∏¥—Œ£¨≥£“‘ÀÆ∫œŒÔ[FeSO4°§(NH4)2SO4°§6H2O]–Œ Ω¥Ê‘⁄£¨Œ™«≥¿∂¬Ã…´æß㨑⁄ø’∆¯÷–±»“ª∞„—«Ã˙—ŒŒ»∂®£¨ «∑÷ŒˆªØ—ß÷–≥£”√µƒªπ‘≠º¡°£
µ—È “ø…”√»Áœ¬∑Ω∑®¿¥÷∆±∏¡ÚÀ·—«Ã˙Ôߣ∫
¢Ÿ≥∆»°12.4g(NH4)2SO4º”»ÎµΩFeSO4»Ð“∫÷–£¨º”»»’Ù∑¢≈®Àı£ª
¢⁄≥∆»°5.6g∑œÃ˙–ºÕ∂»ÎµΩ20mL5%µƒNa2CO3»Ð“∫÷–£¨÷Û∑–º∏∑÷÷”∫Ûπ˝¬À≤¢”√’Ù¡ÛÀÆœ¥æª£ª
¢€∞—œ¥æªµƒÃ˙∑€º”»ÎµΩ60mL 2mol/LµƒH2SO4»Ð“∫÷–£¨–°ªº”»»Œ¬∂»øÿ÷∆‘⁄50°Ê~60°Ê÷ƺ‰£¨≤¢≤ª∂œ≤π≥‰’Ù¡ÛÀÆ“‘±£≥÷‘≠ê˝£¨÷±÷¡≤ª‘Ÿ”–∆¯≈ð∑≈≥ˆ£ª
¢Ð≥√»»π˝¬À£¨¬À“∫◊™“∆µΩ’Ù∑¢√Û÷–£ª
¢ð¿‰»¥÷¡ “Œ¬π˝¬Àµ√≤˙∆∑£ª
“—÷™£∫FeSO4°§7H2O‘⁄¿‰ÀÆ÷–»ÐΩ‚∂»∫Ж°°£
‘ªÿ¥œ¬¡–Œ £∫
°° (1)’˝»∑µƒ µ—È≤Ω÷ËŒ™°°°°°°°°°°°°°°°°°°°°°° £ª
(2)≤Ω÷Ë¢⁄÷–”√Na2CO3»Ð“∫÷Û∑–º∏∑÷÷”µƒƒøµƒ «£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
≤Ω÷Ë¢€Œ™∫Œ≤ª¿˚”√¥Ûªº”»»¿¥Ã·∏þ∑¥”¶ÀŸ¬ £ø°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(3)≤Ω÷ˢЌ™ ≤√¥“™≥√»»π˝¬À£ø°°°°°°°°°°°°°°°°°°°°°°°°°° °£
(4)ƒ¶∂˚—Œ∆∑÷ µƒ∏þµÕ÷˜“™æˆ∂®”⁄Fe2+º∞Fe3+µƒ∫¨¡ø£¨”√…œ ˆ∑Ω∑®÷∆±∏µƒ¡ÚÀ·—«Ã˙Ôß÷–Õ˘Õ˘∫¨”–Fe3+£¨»Ù“™ºÏ—È∆‰÷– «∑Ò∫¨”–Fe3+£¨ø…“‘ π”√ƒƒ÷÷ ‘º¡£∫ °°°°°°°°°°°°°°°°°°
A£ÆNaOH»Ð“∫°°°°°° B£ÆKSCN»Ð“∫°°°°°° C£Æ±Ω∑”»Ð“∫°°°° D£Æ Ø»Ô ‘“∫
(5)»°3.92g¡ÚÀ·—«Ã˙ÔßæßÃÂ≈‰≥…100mL»Ð“∫£¨”√À· ΩµŒ∂®πл°20.00mL◊¢»Î◊∂–Œ∆ø÷–£¨»ª∫Û”√Œ¥÷™≈®∂»µƒÀ·–‘∏þ√ÃÀ·ºÿ»Ð“∫Ω¯––µŒ∂®£¨œ˚∫ƒ∏√»Ð“∫µƒÃª˝Œ™8.00mL°£
¢Ÿ≈‰∆Ωœ¬¡–∑¥”¶ Ω£∫
°°°° Fe2++°°°° MnO4£≠+°°°° H+ -°°°° Mn2++°°°° Fe3++°°°° H2O
¢⁄”√°°°°°°°°°°°°°°°° (À· ΩªÚºÓ Ω)µŒ∂®πÐ ¢◊∞∏þ√ÃÀ·ºÿ»Ð“∫
¢€∏þ√ÃÀ·ºÿ»Ð“∫µƒŒÔ÷ µƒ¡ø≈®∂» «°°°°°°°°°°°°°°°°°° °£
27£Æ(15∑÷)∏ı‘™Àÿº∞∆‰ªØ∫œŒÔ‘⁄œ÷¥˙𧓵÷–”√Õæ Æ∑÷π„∑∫°£ƒ≥ø∆—––°◊È‘⁄ÃΩæø∏ıº∞∆‰ªØ∫œŒÔ–‘÷ ±µ√µΩ»Áœ¬µƒ◊ ¡œ–≈œ¢£∫
¢Ò ∏ı‘™Àÿ‘⁄◊‘»ªΩÁ÷–÷˜“™“‘∏ıÃ˙øÛ(FeO•Cr2O3)–Œ Ω¥Ê‘⁄
¢Ú Crµƒ≥£º˚ªØ∫œº€£∫+2£¨+3£¨+6
¢Û ’‚÷÷‘™Àÿ“‘≤ªÕ¨ªØ∫œŒÔµƒ–Œ Ω¥Ê‘⁄ ±—’…´≤ªÕ¨(º˚œ¬±Ì)£¨π ±ª≥∆Œ™°∞∂ý≤ µƒ‘™Àÿ°±
|
Œ¢¡£ |
Cr(OH)3 |
CrO2- |
Na2CrO4 |
Cr3+ |
Ag2CrO4 |
Cr2O72- |
BaCrO4 |
|
—’…´ |
ª“¬Ã…´ |
¬Ã…´ |
ª∆…´ |
◊œ…´ |
◊©∫Ï…´ |
≥»…´ |
ƒ˚≥»ª∆…´ |
¢Ù 𧓵…œ“±¡∂∏ıµƒ¡˜≥ûÁœ¬£∫
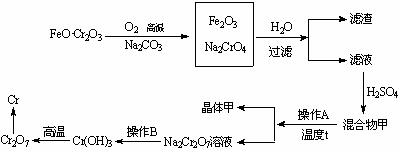
¢ı ∏ıÀ·ƒ∆º∞¡ÚÀ·ƒ∆µƒ»ÐΩ‚∂»«˙œþ»ÁÕº£∫
(I£∫Na2Cr2O7•2H2O II£∫Na2SO4•10H2O III£∫Na2SO4)
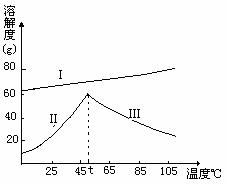
ÕÍ≥…œ¬¡–∏˜Ã‚£∫
°° (1)”…Cr2O3°˙Crø…”√¬¡»»∑®£¨∑¥”¶µƒ∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (2)œÚBaCrO4◊«“∫÷–µŒº”Ag+ ‘º¡£¨ªÏ∫œŒÔµƒ—’…´÷Ω•◊™ªØŒ™◊©∫Ï…´£¨Àµ√˜Ag2CrO4 µƒ»ÐΩ‚∂»°°°°°°°°°°°°°° ( ÃÓ°∞¥Û”⁄°±ªÚ°∞–°”⁄°±)BaCrO4µƒ»ÐΩ‚∂»°£
°° (3)“¿æð“‘…œ–≈œ¢∑÷Œˆ£¨œ¬¡–Àµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°° °£
A£Æ≤Ÿ◊˜Bπ˝≥Ã÷–“ª∂®º”»Îªπ‘≠º¡
B£Æ∏ıµƒªØ∫œŒÔø…“‘◊ˆƒ≥÷÷÷∏ 溡
C£Æ»Ùæßú◊Œ™Na2SO4£¨‘Ú≤Ÿ◊˜A «ºÃ–¯’Ù∑¢Ω·æߣ¨≥√»»π˝¬À
D£Æ»Ùæßú◊Œ™Na2SO4•10H2O£¨‘Ú≤Ÿ◊˜A «ºÃ–¯’Ù∑¢Ω·æߣ¨≥√»»π˝¬À
°° (4)Cr(OH)3µƒ–‘÷ ”ÎAl(OH)3µƒ–‘÷ œýÀ∆£¨ÕÍ≥…Cr(OH)3‘⁄ÀÆ÷–µƒµÁ¿Î∑Ω≥Ã Ω£∫
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°£
»ÙœÚCr(OH)3µƒ◊«“∫÷–÷µŒµŒº”NaOH»Ð“∫£¨π€≤ÏµΩµƒ µ—Èœ÷œÛ «£∫°°°°°°°° °£
»ÙºÃ–¯œÚÀ˘µ√µƒ»Ð“∫÷–µŒº”H2O2£¨»Ð“∫÷Ω•±‰≥…ª∆…´£¨∏√±‰ªØµƒ¿Î◊”∑¥”¶∑Ω≥Ã Ω£∫
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
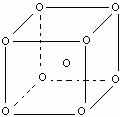
°° (5)∏ıæßê˘±æΩ·π𵕑™»ÁÕº(∏ı‘≠◊”∑÷≤º‘⁄¡¢∑Ωõƒ∂•µ„∫ÕÖƒ)£∫»ÙΩ Ù∏ıµƒ√Ð∂»Œ™¶—g/cm3£¨∏ıµƒœý∂‘‘≠◊”÷ ¡øŒ™M£¨NA¥˙±Ì∞¢∑¸º”µ¬¬Þ≥£ ˝£¨‘Úæß∞˚µƒ±þ≥§aŒ™£∫°°°°°°°° °£
26£Æ(15∑÷)
°° (1)”…µ⁄“ª°¢µ⁄∂˛÷Ð∆⁄‘™Àÿ◊È≥…µƒº∏÷÷ŒÔ÷ £¨∆‰◊È≥…∑÷±»Áœ¬£∫
A£∫H2O2°° °°°°°°°°°°°°°°°°B£∫NH2OH(Ù«∞∑)°° °°°°°°°°C£∫HO-CN(«ËÀ·)
D£∫H2N-NH2(ά) °°°°°°E£∫H2N-CN(«Ë∞∑)
°°°°°° ªÿ¥œ¬¡–Œ £∫
¢Ÿæþ”–18µÁ◊”µƒ∑÷◊””–£∫°° °°°°°°°°°°°°°°°°°°°°(”√◊÷ƒ∏±Ì æ)
¢⁄¥”Ω·ππ…œø¥£¨Ù«∞∑ «∞±∑÷◊”÷–µƒ“ª∏ˆ«‚‘≠◊”±ªÙ«ª˘»°¥˙µƒ≤˙ŒÔ£¨Ù«∞∑µƒµÁ◊” ΩŒ™£∫
°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
¢€H2‘⁄ø’∆¯÷–»º…’øÿ÷∆ µ±µƒÃıº˛ø…“‘…˙≥…H2O2£¨«“H2(g)+O2(g)=H2O2(l)£ª¶§H=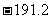 kJ/mol°£»ÙH2µƒ»º…’»» «285.8kJ/mol£¨ÕÍ≥…H2O(l)…˙≥…H2O2(l)µƒ»»ªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°£
kJ/mol°£»ÙH2µƒ»º…’»» «285.8kJ/mol£¨ÕÍ≥…H2O(l)…˙≥…H2O2(l)µƒ»»ªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°£
°° (2)Ω´8mol H2∫Õ2molN2≥‰»Î2L√б’»ð∆˜÷–£¨‘⁄“ª∂®Ãıº˛œ¬Ω¯––∫œ≥…∞±∑¥”¶£¨4min∫Û∑¥”¶¥ÔµΩ∆Ω∫‚£¨≤‚µ√»ð∆˜÷–ªπ”–5.6molH2°£‘Ú”√N2±Ì 浃∑¥”¶ÀŸ¬ Œ™°°°°°°°° °£
µ±∆‰À˚Ãıº˛≤ª±‰£¨Ω´»ð∆˜Ãª˝±‰Œ™1L¥ÔµΩ–¬∆Ω∫‚ ±£¨N2µƒ≈®∂»°° °°°°°°°°(ÃÓ°∞£æ°±°¢°∞=°±°¢°∞£º°±°∞£Ω°±‘≠∆Ω∫‚ ±N2µƒ≈®∂»°£
(3)”√¡Ω÷ß∂Ë–‘µÁº´≤»Î500mL pHŒ™6.0µƒAgNO3»Ð“∫÷–£¨Õ®µÁµÁΩ‚£¨µ±µÁº´…œŒˆ≥ˆπÃÃÂ÷ ¡ø¥Û‘ºŒ™54mg ±£¨µÁΩ‚“∫µƒpH‘ºŒ™°°°°°°°°°°°° (…˵ÁΩ‚ ±“ıº´√ª”–«‚∆¯Œˆ≥ˆ£¨«“µÁΩ‚“∫‘⁄µÁΩ‚«∞∫Ûê˝±‰ªØø…“‘∫ˆ¬‘)£¨—Ùº´µÁ∞Â∑¥”¶ ΩŒ™°° °°°°°°°°°°°£
13£Æ “Œ¬ ±£¨0.1 mol°§L£≠1µƒHA »Ð“∫µƒpH=3£¨œÚ∏√»Ð“∫÷–÷µŒº”»ÎNaOH»Ð“∫£¨‘⁄µŒº”π˝≥Ã÷–£¨”–πÿ– ˆ≤ª’˝»∑µƒ « °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
A£ÆŒ¥º”»ÎNaOH»Ð“∫ ±£¨‘≠HA»Ð“∫÷–£¨C(H+) = C(OH-) + C(A-)
°°°°°° B£ÆœÚ‘≠»Ð“∫÷–µŒ»Î…Ÿ¡øµƒ0.1 mol°§L£≠1µƒNaOH »Ð“∫£¨ø…¥ŸΩ¯HAµƒµÁ¿Î£¨«“‘≠»Ð“∫µƒpH…˝∏þ°£
C£Æµ±µŒ»ÎµƒNaOH”ÎHA«°∫√ÕÍ»´÷–∫Õ ±£¨»Ð“∫÷–C(Na+) = C(A-)£¨«“»Ð“∫≥ ÷––‘°£
D£Æµ±º”»Îπ˝¡øµƒNaOH»Ð“∫ ±£¨»Ð“∫÷–¿Î◊”≈®∂»ø…ƒÐŒ™£∫C(Na+)£æC(A-)£æC(OH-)£æC(H+)
µ⁄¢ÚæÌ(174∑÷)
12£Æ”…“ª∏ˆ—ı‘≠◊”£¨“ª∏ˆµ™‘≠◊”£¨7∏ˆ«‚‘≠◊”∫Õ»Ù∏…∏ˆÃº‘≠◊”◊È≥…µƒ”–ª˙ŒÔ∑÷◊”£¨∆‰Ãº‘≠◊”µƒ∏ˆ ˝◊Ó…ŸŒ™ °°°°°°°°°°°°°°°°°°°° °°°°°° (°°°° )
A£Æ1°°°°°°°°°°°°°°°°°°°°°°°° B£Æ2°°°°°°°°°°°°°°°°°°°°°°°° C£Æ3°°°°°°°°°°°°°°°°°°°°°°°° D£Æ4
11£Æœ¬¡–Àµ∑®’˝»∑µƒ « °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
A£Æ≥£º˚Ω ÙÃ˙∫Õ¬¡‘⁄𧓵…œ «”…»»ªπ‘≠∑®÷∆µ√µƒ
B£Æ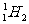 ∫Õ
∫Õ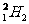 µƒŒÔ¿Ì–‘÷ ¬‘”–≤Ó“Ï£¨ªØ—ß–‘÷ º∏∫ıÕÍ»´œýÕ¨
µƒŒÔ¿Ì–‘÷ ¬‘”–≤Ó“Ï£¨ªØ—ß–‘÷ º∏∫ıÕÍ»´œýÕ¨
C£Æ µ—È “÷–”√◊ÿ…´µŒ∆ø¥Ê∑≈‰ÂÀÆ
D£ÆŒÌ°¢”–…´≤£¡ß°¢∆œÃ—ë»Ð“∫÷–∑÷…¢÷ µƒ¡£◊”÷±æ∂¥Û–°æ˘‘⁄1nm-100nm÷ƺ‰
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com