
27.(14分)有一包固体粉末由下列物质中若干种均匀混合而成:CaCO3、Fe2(SO4)3、BaCl2、K2S、Ba(NO3)2。有关实验过程及记录如下:
(1)将粉末溶于水,得到黄色溶液和白色沉淀,过滤后再将沉淀洗涤、烘干、称量,质量为a g。
(2)向滤出的沉淀中加足量稀HNO3,沉淀无变化。
(3)把(1)中所得滤液分成两等份,滴加试剂和实验结果如下图:
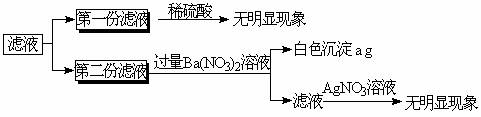
请回答下列问题:
(1)该固体粉末中一定不存在CaCO3,判断理由是 。
(2)写出将粉末溶于水后生成白色沉淀的离子方程式 。
(3)此固体粉末由 混合而成,它们的物质的量之比为 。
26.(16分)现有A、B、C、D四种原子序数依次增大的短周期元素,已知由A、B两元素组成的某化合物甲,其一分子中,原子总数与任意相邻化学键夹角度数之比为1/10。B元素和C元素能形成BC和BC2两种化合物,由C、 D两种元素所形成的化合物均能与水反应生成强碱。
(1)写出下列各元素的名称:A ,D 。
(2)一种仅由C、D两种元素组成的化合物乙,该物质晶体中存在两种化学键,请用电子式表示乙的形成过程 。
(3)在由A、B、C、D元素中的两种或三种或四种组成的所有化合物中,相互之间既可以发生化合反应和复分解反应,也可以发生氧化还原反应,有些物质还可以独立发生分解反应。
典型的盐分解反应的化学方程式为 ;
(当有多个时,只需写出一个即可,下同);
典型的中和反应生成正盐的离子方程式为 ;
典型的“三合一”的化合反应的离子方程式为 ;
典型的氧化还原反应的化学方程式为 。
(4)实验测得26 g甲物质完全燃烧时,放出的热量为384kJ,则表示甲物质燃烧热的热化学方程式为 。
(5)均由A、B、C、D四种元素中的三种组成的稳定化合物丙、丁,已知相对分子质量乙大于丙,一种物质抑制水的电离,一种物质促进水的电离。配得二者等物质的量浓度的溶液戊,在戊溶液中离子浓度由大到小的顺序为 。
13.在下图装置中能构成原电池,且在电流表中能形成指针偏转的是( )
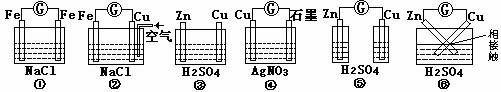
A.①④⑥ B.②④⑥ C.②④ D.④⑥
第Ⅱ卷(非选择题)
12.有一兴趣小组准备在实验室中制H2,装置如图所示。可是在实验室中发现酸液不足而又无其它酸液可加入。为达到实验目的,则可以从长颈漏斗中加入适量的试剂是( )
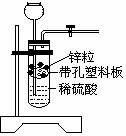
①NaNO3溶液 ②酒精 ③四氯化碳
④苯 ⑤Na2CO3溶液 ⑥KCl溶液
A.①②③ B.②④⑤ C.①②④⑥ D.②③⑥
11.如图:分别在两容器甲、乙中进行同一可逆反应:
2A(g)+2B(g) C(g)+3D(g);△H<0,现向体积为V的甲容器中充入2 mol A和2 mol B,再向乙容器中充入2 mol C和6 mol D,并使乙容器在反应开始前的体积为2 V,下列关于两容器中反应的说法正确的是 ( )
C(g)+3D(g);△H<0,现向体积为V的甲容器中充入2 mol A和2 mol B,再向乙容器中充入2 mol C和6 mol D,并使乙容器在反应开始前的体积为2 V,下列关于两容器中反应的说法正确的是 ( )
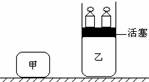
A.在恒温下,甲容器的反应先达到化学平衡状态
B.在恒温下,将乙容器中的砝码拿掉一只后再继续反应达平衡,所得平衡中各物质的质量分数、体积分数、物质的量浓度都与甲中相同
C.在恒温下两容器中达到平衡后,将甲、乙容器的温度升高,当达到一个相同的温度时,再达到平衡后两容器中C物质的物质的量浓度仍然相同
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
10.现有3 g CO和H2的混合气体,在一定量的氧气中燃烧,将燃烧后的混合物通过足量的过氧化钠固体,固体增重m g,并生成氧气1.6 g,则m值可能为 ( )
A.0<m<1.4 B.0.2<m<2.8 C.3 D.1.4<m<3
9.充有m mL NO和n mL NO2的一支试管,管口朝下插入水中,并向其中通入m mL的氧气,已知气体体积在相同状况下测定,且n>m,则充分反应后,剩余气体的体积与原气体的体积比为 ( )
A.(m-n)/[3(m+n)] B.n/[3(m+n)]
C.(n-m)/(m+n) D.(n-m)/[3(m+n)]
8.用惰性电极电解足量下列电解质稀溶液,电解一段时间后,恢复到室温,溶液的pH一定不发生变化的是 ( )
A.NaCl溶液 B.Na2SO4溶液 C.Na2CO3溶液 D.HCl溶液
7.某氧化物不溶于水,溶于熔化的NaOH中,生成易溶于水的化合物,向稀盐酸中滴加所生成化合物的水溶液,立即有白色沉淀产生,则原化合物可能是 ( )
A.CO2 B.SiO2 C.Al2O3 D.Fe2O3
6.对于所有的化学反应,当改变下列的某一条件时,化学反应速率一定发生变化的是( )
A.浓度 B.压强 C.体积 D.物质的量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com