
7.已知NA表示阿伏加德罗常数,下列说法不正确的是 ( )
A.0.1mol·L-1氯化钡溶液中含C1-数目是0.2NA
B.标准状况下,11.2L CO和O2的混合气体中,共含有NA个原子
C.78gNa2O2与足量水充分反应,共转移NA个电子
D.乙醇的燃烧热在数值上等于常温常压下NA个乙醇分子完全燃烧生成液态水和CO2气体时所放出的热量。
6.下列说法正确的是 ( )
①只由一种元素组成的物质,一定是纯净物;
②离子化合物中一定含离子键,可能含共价键,一定含金属元素;
③硝酸和盐酸既有氧化性,又有还原性;
④碱性氧化物一定是金属氧化物。
A.①② B.①④ C.②③ D.③④
22.150℃在一定容积的密闭容器中,使某气态烯烃和适量氧气点燃完全反应后,仍保持150℃时测定容器内压强为原来的1.2倍。
(1)求该烯烃的分子式。
(2)若该烯烃与氧气反应后的产物能生成两种一氯代物,写出该烯烃的结构简式。
(3)若(2)中烯烃的氢核磁共振谱中只在一个位置上出现特征峰,试写出该烯烃的名称。
21.(1)某离子晶体晶胞结构单元如图所示,X位于立方体的顶点,Y位于立方体的中心①晶体中每个Y同时吸引着 个X,每个X同时吸引着 个Y,该晶体的化学式是 。
②晶体中每个X周围与它最接近且距离相等的X共有 个。
③某气态分子也具有下图所示的空间结构,该分子的化学式是 。
(2)已知MEO的晶体结构属于NaC1型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误: .

20.下表中的实线表示元素周期表的部分边界。①一⑤分别表示元素周期表中对应位置的元素。
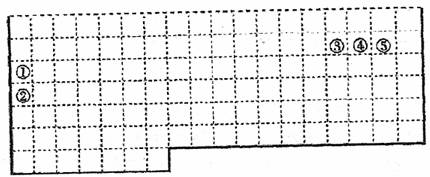
(1)请在上表中用实线补全元素周期表边界。
(2)元素③氢化物的电子式为 ,元素①的最高价氧化物对应水化物的电子式为 。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素中金属性较强的是 (填名称),可以验证该结论的实验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将除掉表面氧化膜的这两种元素的单质分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的热稳定性
(4)写出②的最高价氧化物对应的水化物与甲的最高价氧化物反应的离子方程式
19.某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。
|
产物 |
氢气 |
甲烷 |
乙烯 |
丙烯 |
苯 |
甲苯 |
碳 |
|
质量分数(%) |
12 |
24 |
12 |
16 |
20 |
10 |
6 |

加热聚丙烯废塑料得到的产物如上表:
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
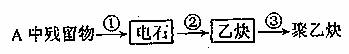
写出反应③的化学方程式 。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有 种。
(3)锥形瓶C中观察到的现象 。
经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为 。
(4)写出C中逸出的气体在工业上的两种用途 、 。
18.汽油不仅是最重要的燃制,而且是重要的化工原料,它既可裂解得到气态化工原料如乙烯等,还可以在催化剂催化下改变分子结构,由链烃变成芳香烃,如已烷变成苯,庚烷变成甲苯,这个变化叫异构化。请根据以汽油为原料的下列衍变关系,写出相应的化学方程式(有机物写结构简式),在括弧中填反应类型。
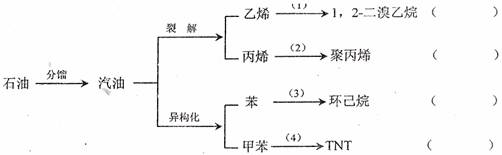
(1)
(2)
(4)
信息提示:苯环上原有取代基对新导入苯环上的取代基的位置有一定影响,其规律是:①苯环上新导入的取代基所占的位置决定于原取代基的性质;
②可以把原取代基分为二类:第一类是邻对位取代基,如-OH、-C1、-Br、-R、-OCOR…,可使新的取代基进入苯环的邻位或对位;第二类是间位取代基,如-NO2、-SO3H、-CHO、-COOH…,可使新的取代基进入苯环的间位,分析下列变化:

(1)C的结构简式为 ;
(2)D与E互为同分异构体,D的结构简式为 ;
(3)写出上图中②反应的化学方程式 。
17.(1)写出下列微粒的名称。
①一OH ②-CHO ③OH-
(2)下列各组中的两种有机物,可能是相同的物质、同系物或同分异构体等,请判断它们之间的关系。
①2一甲基丁烷和丁烷 ②异戊烷和2,2一二甲基丙烷
③间二甲苯和乙苯 ④1-己烯和环己烷
(3)下列物质①铁 ②干冰③金刚石④铜⑤水晶⑥氯化钠⑦碘⑧氢氧化钠中熔化或溶于水时克服离子键的是 ,(填写序号,下同)熔化时克服共价键的是 ,溶于水克服分子间作用力的是 。
(4)在烃的分子结构中,若每减少2个氢原子,则相当于碳碳间增加l对共用电子。试回答下列问题:
①分子式为CnH2n+2的烷烃中碳碳原子间共用电子对数为
②分子式为CnH2n-6的链烃分子中碳碳原子间共用电子对数为
③CX可看作是烃减氢后的产物,若某物质分子中碳碳原子间共用电子对数为140,则符合该条件的碳单质的化学式为 ;符合该条件的稀烃的分子式是 。
16.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是 ( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
15.含有2-5个碳原子的直链烷烃沸点和燃烧热的数据见下表
|
烷烃名称 |
乙烷 |
丙烷 |
丁烷 |
戊烷 |
|
沸点(℃) |
-88.6 |
-42.1 |
-0.5 |
36.1 |
|
*燃烧热(kJ/mo1) |
1560.7 |
2219.2 |
2877.6 |
3535.6 |
*燃烧热:1摩尔物质完全燃烧,生成二氧化碳、液态水时所放出的热量。
根据表中数据,下列判断错误的是 ( )
A.正庚烷在常温常压下肯定不是气体
B.烷烃燃烧热和其所含碳原子数成线性关系
C.随碳原子数增加,烷烃沸点逐渐升高
D.随碳原子数增加,烷烃沸点和燃烧热都成比例增加
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com