
9£®ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ ¡¡¡¡ A£®Àë×Ó¾§ÌåÖÐÿ¸öÀë×ÓÖÜΧ¾ùÎüÒý6¸ö´øÏà·´µçºÉµÄÀë×Ó
¡¡ ¡¡¡¡ B£®Ô×Ó¾§ÌåÖи÷ÏàÁÚµÄÔ×Ó¶¼ÒÔ¹²¼Û¼üÏà½áºÏ
¡¡ ¡¡¡¡ C£®·Ö×Ó¾§ÌåµÄÈ۷еã½ÏµÍ£¬³£ÎÂ϶¼ÒÔÒºÌåºÍÆøÌåÐÎʽ´æÔÚ
¡¡ ¡¡¡¡ D£®½ðÊô¾§ÌåÓɽðÊôÀë×ÓºÍÒõÀë×Ó¹¹³É
8£®ÉèNA±íʾ°¢·ü¼ÓµÂÂÞ³£ÊýµÄÊýÖµ£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ ¡¡¡¡ A£®¼ÓÈȺ¬0.2mol H2SO4µÄŨÁòËáÓë×ãÁ¿Í·´Ó¦£¬Éú³ÉµÄSO2µÄ·Ö×ÓÊýΪ0.1NA
¡¡ ¡¡¡¡ B£®1molCnH2n+2º¬ÓÐ(3n+1)NA¸ö¹²¼Û¼ü
¡¡ ¡¡¡¡ C£®2.24LµªÆøºÍÑõÆøµÄ»ìºÏÆøÌåÖÐËùº¬Ô×ÓÊýΪ0.2NA
¡¡ ¡¡¡¡ D£®1L 0.5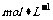 µÄCuCl2ÈÜÒºÖк¬ÓÐ0.5NA¸öCu2+
µÄCuCl2ÈÜÒºÖк¬ÓÐ0.5NA¸öCu2+
7£®½üÈÕÀ´£¬Éò³Ç¡°¾ÞÄܸơ±Ê¼þ·Ð·ÐÑïÑÔÒòÔÚÓÚ²¿·Ö¾ÞÄܸƱ»¼ì³öº¬ÓÐË«ÑõË®£¬¶øË«ÑõË®ÓÐÖ°©ÐÔ£¬¿É¼ÓËÙÈËÌåË¥ÀÏ¡£Òò´ËÎÀÉú²¿ÒÑ¿ªÊ¼¼Ó½ôµ÷²é¡°¾ÞÄܸơ±Ê¼þ¡£ÏÂÁÐÓйØ˵·¨´íÎóµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ ¡¡¡¡ A£®Ë«ÑõË®ÊÇÂÌÉ«Ñõ»¯¼Á£¬¿É×÷Ò½ÁÆÏû¶¾¼Á£¬ËµÃ÷H2O2¶ÔÈËÌåÎÞº¦
¡¡ ¡¡¡¡ B£®H2O2¡¢ Na2O2Öж¼´æÔڷǼ«ÐÔ¹²¼Û¼ü
¡¡ ¡¡¡¡ C£®H2O2¼ÈÓÐÑõ»¯ÐÔ£¬ÓÖÓл¹ÔÐÔ£¬ÓëKMnO4·´Ó¦Ê±±íÏÖH2O2µÄ»¹ÔÐÔ
¡¡ ¡¡¡¡ D£®H2O2×öƯ°×¼ÁÊÇÀûÓÃÆäÑõ»¯ÐÔ£¬Æ¯°×ÔÀíÓëHClOÀàËÆ£¬ºÍSO2²»Í¬
6£®»¯Ñ§ÓëÉú²ú¡¢Éú»î¡¢Éç»áÃÜÇÐÏà¹Ø¡£ÏÂÁÐÓйØ˵·¨Öв»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ ¡¡¡¡ A£®2008Äêŵ±´¶û»¯Ñ§½±±»ÊÚÓèÑо¿¡°ÂÌÉ«Ó«¹âµ°°×ÖÊ¡±µÄÃÀ¼®»ªÒá¿Æѧ¼ÒÇ®ÓÀ½¡µÈÈË¡£µ°°×Öʶ¼ÊÇÓÉ°±»ùËáÐγɵIJ»¿É½µ½âµÄ¸ß·Ö×Ó»¯ºÏÎÆäË®ÈÜÒºÓж¡´ï¶ûЧӦ
¡¡ ¡¡¡¡ B£®ÉñÆßÓԱËù´©º½Ìì·þÊÇÓÉÎÒ¹ú×ÔÐÐÑÐÖƵÄÐÂÐÍ¡°Á¬ÐøÏËάÔöÈÍ¡±º½¿Õ²ÄÁÏ×ö³ÉÖ÷Òª³É·ÖÊÇÓÉ̼»¯¹è¡¢ÌմɺÍ̼ÏËά¸´ºÏ¶ø³ÉµÄ£¬ËüÊÇÒ»ÖÖÐÂÐÍÎÞ»ú·Ç½ðÊô²ÄÁÏ
¡¡ ¡¡¡¡ C£®Í¬Ò»ÎïÖÊÈÜÓÚ²»Í¬µÄÎïÖÊʱ¿ÉÐγɲ»Í¬µÄ·Öɢϵ£¬È罫NaClÈÜÓÚË®¿ÉÐγÉÈÜÒº£¬ÈÜÓھƾ«Ôò¿ÉÐγɽºÌå
¡¡ ¡¡¡¡ D£®2008Äê±±¾©°ÂÔ˻ῪĻʽÉϵġ°½ÅÓ¡¡±µÈÑæ»ðÈÃÈ«ÊÀ½çΪ֮»¶ºô¡¢Çãµ¹£¬ÕâÖ÷ÒªÊÇÀûÓÃÁË»¯Ñ§ÖС°ÑæÉ«·´Ó¦¡±µÄÓйØ֪ʶ
29£®(11·Ö)º£ÄÏÊ¡ÊǺ£Ñó´óÊ¡£¬º£Ë®ÊÇÒ»ÖַḻµÄ×ÊÔ´£¬¹¤ÒµÉÏ´Óº£Ë®ÖпÉÌáÈ¡Ðí¶àÖÖÎïÖÊ£¬¹ã·ºÓ¦ÓÃÓÚÉú»î¡¢Éú²ú¡¢¿Æ¼¼µÈ·½Ãæ¡£ÏÂͼÊÇij¹¤³§¶Ôº£Ë®×ÊÔ´½øÐÐ×ÛºÏÀûÓõÄʾÒâͼ¡£
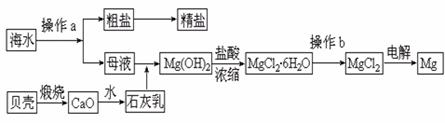
»Ø´ðÏÂÁÐÎÊÌ⣺
¡¡ (1)Á÷³ÌͼÖвÙ×÷aµÄÃû³ÆΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
¡¡ (2)¹¤ÒµÉÏ´Óº£Ë®ÖÐÌáÈ¡µÄNaCl£¬¿ÉÓÃÀ´ÖÆÈ¡´¿¼î£¬Æä¼òÒª¹ý³ÌÈçÏ£ºÏò±¥ºÍʳÑÎË®ÖÐÏÈͨÈëÆøÌåA£¬ºóͨÈëÆøÌåB£¬³ä·Ö·´Ó¦ºó¹ýÂ˵õ½¾§ÌåCºÍÂËÒºD£¬½«¾§ÌåC×ÆÉÕ¼´¿ÉÖƵô¿¼î¡£
¢ÙÔòÆøÌåAÓ¦ÊÇ¡¡¡¡ (Ìѧʽ)Æä¹ý³Ì·´Ó¦·½³ÌʽΪ_______________________¡£
¢ÚÂËÒºDÖÐÖ÷Òªº¬ÓÐNH4Cl¡¢NaHCO3µÈÎïÖÊ£¬¹¤ÒµÉÏÊÇÏòÂËÒºDÖÐͨÈëNH3£¬²¢¼ÓÈëϸСʳÑοÅÁ££¬ÀäÈ´Îö³ö²»º¬ÓÐNaHCO3µÄ¸±²úÆ·NH4Cl¾§Ì壬ÔòͨÈëNH3µÄ×÷ÓÃÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
¡¡ (3)þÊÇÒ»ÖÖÓÃ;ºÜ¹ãµÄ½ðÊô²ÄÁÏ£¬Ä¿Ç°ÊÀ½çÉÏ60%µÄþ´Óº£Ë®ÖÐÌáÈ¡¡£²Ù×÷bÊÇÔÚ¡¡¡¡¡¡¡¡¡¡¡¡ Æø·ÕÖнøÐУ¬ÈôÔÚ¿ÕÆøÖмÓÈÈ£¬Ôò»áË®½âÉú³ÉMg(OH)Cl£¬Ð´³öÓйط´Ó¦µÄ»¯Ñ§·½³Ìʽ_____________________________________________¡£
¡¡ (4)Ò»ÂȼÿÌìÏûºÄ234¶ÖNaCl£¬ÕâЩNaClÄÜÉú²úÖÊÁ¿·ÖÊýΪ32%µÄÉÕ¼îÈÜÒº________¶Ö£¬Í¬Ê±ÏûºÄ______________¿âµçÁ¿(1µç×ÓµçÁ¿1.60¡Á10-19C)
28£®¾Ý»·±£²¿ÃŲⶨ£¬ÎÒ¹úһЩ´ó³ÇÊеÄËáÓêpH£½3.5¡£ÔÚËáÓê¼¾½ÚÌúÖÆÆ·¼«Ò׸¯Ê´£¬ÔòÔÚÆ丯ʴÖÐÕý¼«·¢ÉúµÄ·´Ó¦ÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®Fe£2e-£½Fe2+¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®2H2O+O2+4e-£½4OH-
¡¡¡¡¡¡ C£®2H++2e-£½H2¡ü¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®4OH-£4e-£½2H2O+O2¡ü
27£®ÔÚÁòËáµÄ¹¤ÒµÖÆ·¨ÖУ¬ÏÂÁÐÉú²ú²Ù×÷¼°ËµÃ÷Éú²ú²Ù×÷µÄÖ÷ÒªÔÒò¶þÕ߶¼ÕýÈ·µÄÊÇ(¡¡¡¡ )
¡¡¡¡¡¡ A£®´Ó·ÐÌÚ¯³öÀ´µÄ¯ÆøÐè¾»»¯£¬ÒòΪ¯ÆøÖÐSO2»áÓëÔÓÖÊ·´Ó¦
¡¡¡¡¡¡ B£®ÁòÌú¿óȼÉÕÇ°ÐèÒª·ÛË飬ÒòΪ´ó¿éµÄ²»ÄÜȼÉÕ
¡¡¡¡¡¡ C£®SO3ÓÃ98.3%µÄŨÁòËáÎüÊÕ£¬Ä¿µÄÊÇ·ÀÖ¹ÐγÉËáÎí£¬ÓÐÀûÓÚSO3ÎüÊÕÍêÈ«
¡¡¡¡¡¡ D£®SO2Ñõ»¯ÎªSO3ʱÐèҪʹÓô߻¯¼Á£¬ÕâÑù¿ÉÒÔÌá¸ßSO2µÄת»¯ÂÊ
26£®ÏÂÁйØÓÚ¹¤ÒµÉú²úµÄ˵·¨ÖУ¬²»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®ÎÞË®ÂÈ»¯Ã¾µÄÖƱ¸£ºMgCl2¡¤6H2O MgCl2+6H2O
MgCl2+6H2O
¡¡¡¡¡¡ B£®Éú²úÆÕͨ²£Á§µÄÖ÷ÒªÔÁÏÓÐʯ»Òʯ¡¢Ê¯Ó¢ºÍ´¿¼î
¡¡¡¡¡¡ C£®¹¤ÒµÉϽ«´ÖͽøÐо«Á¶£¬Ó¦½«´ÖÍÁ¬½ÓÔÚµçÔ´µÄÕý¼«
¡¡¡¡¡¡ D£®Æ¯·Û¾«µÄÖƱ¸£º2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
25£®îÑÒÑ×÷Ϊ³£ÓýðÊôÌú¡¢ÂÁºóµÄµÚÈý½ðÊô£¬ÎÒ¹úîÑ¿ó´¢Á¿·á¸»£¬ËüµÄÓ¦ÓÃÑо¿ÊÇÄ¿Ç°¿ÆѧÑо¿µÄÇ°ÑØÖ®Ò»¡£ 2007Äêŵ±´¶ûÎïÀíѧ½±Îª·¨¹ú¿Æѧ¼Ò°¢¶û±´¡£·Ñ¶ûºÍµÂ¹ú¿Æѧ¼Ò±ËµÃ¡¤¸ñÁÖ±´¸ñ¶û¹²Í¬»ñµÃ£¬ÒÔ±íÕÃËûÃÇÔھ޴ŵç×èЧӦ(MRЧӦ)Ñо¿·½ÃæµÄ³É¾Í£¬Ä³¸ÆîÑÐ͸´ºÏÑõ»¯Îï(ÈçÏÂͼ)£¬ÒÔAÔ×ÓΪ¾§°û¶¥µã£¬Aλ¿ÉÒÔÊÇCa¡¢Sr¡¢Ba»òPb£¬µ±BλÊÇV¡¢Cr¡¢Ti¡¢Feʱ£¬ÕâÖÖ»¯ºÏÎï¾ßÓÐCMRЧӦ¡£
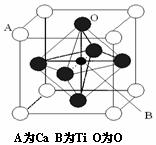
¡¡ (1)д³ö¸Ã¾§ÌåµÄ»¯Ñ§Ê½________________
¡¡ (2)TiµÄºËÍâµç×ÓÅŲ¼Ê½Îª_______ËüλÓÚÖÜÆÚ±íÖÐ______Çø£¬¼Ûµç×ÓÅŲ¼Îª________¡£
¡¡ (3)Ã̵ĵ縺ÐÔΪ1.99¡£CrµÄµç¸ºÐÔΪ1.66£¬ËµÃ÷Ã̵ĽðÊôÐԱȸõ_____(Ç¿¡¢Èõ)
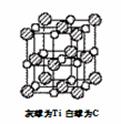
¡¡ (4)×î½ü·¢ÏÖîÑ(Ti)Ô×ÓºÍ̼Ô×Ó¹¹³ÉÆø̬ÍÅ´Ø·Ö×Ó£¬·Ö×ÓÄ£ÐÍÈçͼ¡£ÔòÆ仯ѧʽΪ______¡£ËüÊôÓÚ______¾§Ì壬ÆäÖ÷ÒªÎïÀíÐÔÖÊ____________¡¡ __________(д³ö2¸ö¼´¿É)
¡¶»¯Ñ§Óë¼¼Êõ¡·
26-28ΪѡÔñÌ⣬ÿСÌâÖ»ÓÐÒ»¸öÕýÈ·Ñ¡ÏÿСÌâ3·Ö
24£®Ä³ÓлúÎï(Ãû³ÆÒÒϩͪ)µÄ½á¹¹¼òʽΪ£ºCH2£½C£½O£¬ÏÂÁÐÃèÊöÕýÈ·µÄÊÇ(¡¡¡¡ )
¡¡¡¡¡¡ A£®¸Ã·Ö×ÓÖй²ÓÐ2¸ö¦Ð½¡¡¢2¸ö¦Ò½¡
¡¡¡¡¡¡ B£®¸Ã·Ö×ÓÊô·Ç¼«ÐÔ·Ö×Ó
¡¡¡¡¡¡ C£®¸Ã·Ö×ÓÊÇÖ±ÏßÐÍ·Ö×Ó
¡¡¡¡¡¡ D£®¸Ã·Ö×ÓÖÐ2¸ö̼Ô×ÓµÄÔÓ»¯·½Ê½ÊDz»Í¬µÄ
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com