
15.在298K时,将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1:100混合,反应后所得溶液pH=7。若 值为 ( )
值为 ( )
A.2 B.3 C.4 D.5
14.向某FeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br-)=3c(Cl-)=0.3mol/L。反应过程中溶液的体积变化不计,则下列说法中正确的是 ( )
A.原溶液的浓度为0.1mol/L B.反应后溶液中c(Fe3+)=0.1mol/L
C.反应后溶液中c(Fe3+)=c(Fe2+) D.原溶液中c(Br-)=0.4mol/L
13.有关键能数据如表:
|
化学键 |
Si-O |
O = O |
Si – Si |
|
键能/kJ·mol-1 |
X |
498.8 |
176 |
则晶体硅在氧气中燃烧的热化学方程式:Si(s)+O2(g)===SiO2(s)中,△H=-989.2kJ·mol-1,则X的值为 ( )
A.460 B.920 C.1165.2 D.423.3
12.有一玻璃球,将其抽成真空质量为m1g,解除密封后称量,其质量为m2g,充满H2和O2的混合物气体质量为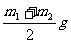 ,则混合物气体中H2所占体积分数为 ( )
,则混合物气体中H2所占体积分数为 ( )
A.58.3% B.41.7% C.10% D.90%
11.五个烧杯中均盛有相同物质的量浓度和相同体积的适量盐酸,分别加入相同物质的量为①Zn,②ZnO,③Zn(OH)2,④ZnCO3,⑤ZnS。恰好完全反应后,所得ZnCl2溶液的质量分数的值为 ( )
A.2种 B.3种 C.4种 D.5种
10.某含氧强酸HmXOn,相对分子质量为A,将它溶于水,测得溶液的氢离子浓度为2mol/L,溶液的质量分数为20%,密度为1.5g/cm3,则m值为 ( )
A. B.
B.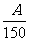 C.
C. D.
D.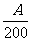
9.在25℃,101Kpa下由HCHO(g)、H2和CO组成的混合气体共6.72g,其相对氢气的密度为14。将该气体与2.24L氧气(标准状况下)充分反应后的产物通过足量的Na2O2粉末,Na2O2粉末增重的质量是 ( )
A.等于6.72g B.小于6.72g C.大于6.72g D.无法确定
8.用质量均为100g的铜片作电极,电解AgNO3溶液,电解一段时间后两极质量相差28g,此时阳极质量为 ( )
A.121,6g B.93.6g C.89.6g D.88.2g
7.将1.12L标准状况下由X、Y组成的混合气体用水全部吸收得到1L溶液,测得pH=1,则X、Y可能是( ),X与Y的体积比为 ( )
A.H2,Cl2;1:1 B.NO2,O2;4:1
C.Cl2,SO2;1:1 D.NO,O2;4:3
6.常温下,向20L真空容器中通入a mol硫化氢与b mol氯气(a,b均为正整数,且均≤5),反应后可生成硫固体和另一种气体,则容器内可能达到的最大密度是 ( )
A.35.5g/L B.17.85g/L C.18.25g/L D.19.45g/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com