
27.(11分每空1分)下图表示某些化工生产的流程(有的反应条件和产物已略去)
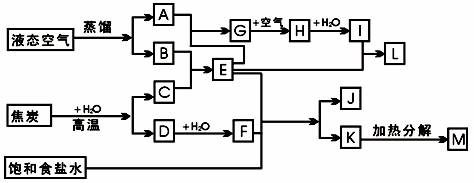
试回答:
(1)B与镁形成的化合物的化学式是 ,K的俗名是 。
(2)A+E→G的化学方程式是 (2分)。
(3)H与水的反应中,氧化剂与还原剂的物质的量之比为 。
(4)写出饱和食盐水+F+E→J+K(沉淀)的化学方程式是 (2分)
(5)写出由上述流程图中出现的两种铵盐的化学式 、
(6)写出M的两种用途: 、
选考题(每科选做1题,共做3题)
26.(18分每空2分)二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是氯气与硫合成二氯化硫的实验装置。

试回答下列问题:
(1)装置A中发生反应的化学方程式为 。
(2)装置B应盛放的药品是 ,C中是 。
(3)实验开始前先在D中放一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是 。
(4)实验时,D装置需加热至50-59℃.最好采用 方式加热。如何防止E中液体挥发 。
(5)二氯化硫分子中各原子均为8电子稳定结构,其电子式为 ,由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为 。
(6)在配制一定物质的量浓度的盐酸溶液时,下列操作所配溶液浓度偏低的是_____:
A.配制溶液时,容量瓶中有少量水。
B.使用容量瓶配制溶液时,俯视观察溶液凹液面与容量瓶刻度线相切
C.配制溶液的过程中,容量瓶未塞好,洒出一些溶液。
D.发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线
25.(14分每空3分)下图是工业生产硝酸铵的流程。

(1)吸收塔C中通入空气的目的是 (2分)。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H=-1266.8kJ/mol
N2(g)+O2(g)=2NO(g);△H=+180.5kJ/mol
写出氨高温催化氧化的热化学方程式:
(3)已知:N2(g)+3H2(g) 2NH3(g);△H=-92kJ/mol。为提高氢气的转化率,宜采取的措施有
。(填字母)
2NH3(g);△H=-92kJ/mol。为提高氢气的转化率,宜采取的措施有
。(填字母)
A.升高温度 B.使用催化剂 C.增大压强 D.循环利用和不断补充氮气 E.及时移出氨
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为25%,此时H2的转化率为
13.浓度为2mol·L-1的氢溴酸溶液VL,欲使其浓度变为4 mol·L-1,以下列出的方法中,可行的为 ( )
A.通入标况下的HBr气体44.8L
B.加入10 mol·L-1氢溴酸0.6VL,再将溶液稀释至2VL
C.蒸发掉0.5L水
D.将溶液加热蒸发浓缩至0.5V
第Ⅱ卷(必考题129分,选考题45分,共174分)
必考题(共8道题)
12.下列有关物质性质的比较正确的为 ( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高
②所有元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强
⑤还原性: S2->Cl->Br-
S2->Cl->Br-
⑥酸性:HClO4>H2SO4>H3PO4>H2SiO3
A.①③ B.②④ C.③⑥ D.⑤⑥
11.下列溶液中各微粒的浓度关系正确的是 ( )
A.1.0mol/LNa2CO3溶液:c(OH一)=c(H+)+c(H2CO3)+c(HCO3-)
B.物质的量浓度相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中c(NH4+):
c(NH4)2SO4>c(NH4HSO4)>c(NH4C1)
C.pH=6的纯水:c(H+)>c(OH一)
D.向醋酸钠溶液中加入适量醋酸,得到酸性混合溶液:
c(Na+)>c(CH3COO一)>c(H+)>c(OH一)
10.对下列装置,不添加其他仪器无法检查气密性的是 ( )
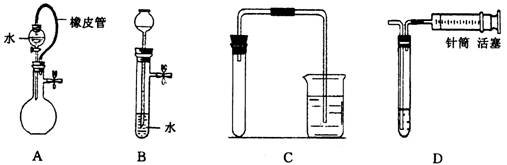
9.下列电离方程式中,正确的是 ( )
A.HClO4  H++ClO4-
H++ClO4-
B.H2CO3
 2H++CO32-
2H++CO32-
C.H2PO4-+H2O  HPO42-+H3O+
HPO42-+H3O+
D.NH3·H2O == NH4++OH-
8.用NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.2mol过氧化氢完全分解转移的电子数目为0.4NA
B.300mL 2 mol/L蔗糖溶液中所含分子总数为0.6NA
C.在常温常压下,17g硫化氢所含质子数目为8NA
D.在标准状况下,2.24L二氧化硫与氧气的混合气体中所含氧原子数为0.2NA
7.北京奥运会“水立方”游泳池中的水主要是通过砂滤、臭氧、活性炭来净化的,下列有关说法不正确的是 ( )
A.砂滤是利用过滤原理除去水中较大的固体颗粒
B.用臭氧杀菌消毒是因为臭氧具有强氧化性
C.游泳池中的臭氧浓度越高越好
D.活性炭可以吸附水中悬浮的杂质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com