
5.下列各种变化中,不属于化学变化的是 ( )
A.向鸡蛋白溶液中加入饱和硫酸铵溶液,析出蛋白质
B.向白色无水硫酸铜粉末中滴加少量水
C.纯碱晶体风化
D.向鸡蛋白溶液中滴加硝酸铅溶液,析出白色沉淀
4.下列物质是电解质的为 ( )
A.氨气 B.硫酸钡 C.二氧化碳 D.硝酸钾溶液
3.根据下列反应:(1)2Fe3++2I-=2Fe2++I2 (2)Br2+2Fe2+=2Br-+2Fe3+
判断离子的还原性由强到弱的顺序是 ( )
A.Br->Fe2+>I- B.I->Fe2+>Br-
C.Br->I->Fe2+ D.Fe2+>I->Br-
2.下列物质中属于纯净物的是 ( )
A.磷在氯气中燃烧后的生成物 B.盐酸
C.液氯 D.淀粉KI溶液
1.食用下列物质不会引起中毒的是 ( )
A.用碳酸钡作X射线透视的“钡餐” B.加碘食盐
C.用甲醇兑制的白酒 D.用于混凝土防冻的亚硝酸钠
29.(14分)某有机物A(只含C、H、O)是一种重要化工生产的中间体,其蒸气密度是相同状况下氢气密度的83倍。试根据下列信息回答相关问题:
①A分子中碳原子总数是氧原子总数的3倍,其苯环上只有一个取代基,且取代基中不含甲基;
②A可与NaHCO3溶液作用,产生无色气泡;
③A在一定条件下可与乙酸发生酯化反应。
请写出:
(1)A的分子式 ;A的一种可能的结构简式 ;
A中含氧官能团的名称为 。
若有机物A存在如下转化关系,请据此时A的结构回答(2)、(3)、(4)问:
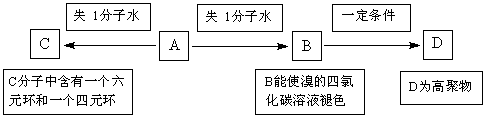
(2)请写出:A→C和B→D的化学反应方程式(注明反应条件),并注明反应类型:
A→C: ,反应类型: ;
B→D: ,反应类型: 。
(3)A的一种同分异构体F,其苯环上有两个相邻的取代基,且能与三氯化铁溶液发生显色反应。F在稀硫酸存在下水解生成G和H,其中H俗称“木精”,是饮用假酒过程中致人失明、甚至死亡的元凶。
请写出F的结构简式:____________________________________。
(4)已知H在一定条件下可被氧化成K,K的水溶液常用作防腐剂,请写出:
H→K的化学方程式:_________________________________________________。
28.(16分)某化学兴趣小组为探究铜跟浓硫酸的反应,用下图装置进行有关实验。请回答下列问题:
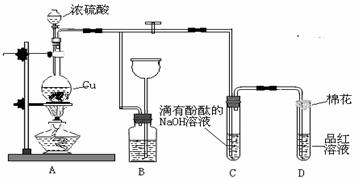
(1)装置A中发生的化学反应的化学方程式为________________________________。
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是______(填序号)
①水 ②酸性KMnO4 ③Na2CO3溶液 ④饱和NaHSO3 溶液
(3)装置C和D中产生的现象相同,但原因却不同。其中D中现象说明SO2具有_____________性。
(4)装置D中试管口塞一团棉花,棉花浸有一种液体,这种液体可以是________(填序号),①浓溴水 ②酸性KMnO4 溶液 ③NaOH溶液 ④饱和NaHSO3 溶液
其作用是 。
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其它离子无关,某同学设计了下列实验,其中不必要的是 (填序号)。
①观察稀H2SO4 溶液呈无色 ②观察CuSO4 粉末呈白色 ③稀释CuSO4溶液,溶液蓝色变浅 ④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色 ⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍显蓝色
(6)若实验中用7.2g铜片和12.5mL 18mol/L 的浓硫酸在加热条件下充分反应,最终铜片仍有剩余。根据所学的知识,某同学认为该溶液中一定会有硫酸剩余,其理由是
;假定反应前后溶液的体积不变,设剩余硫酸的浓度为a mol/L ,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾 mol。(用含a的代数式表示,要化简)
27.(12分)下图A-J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质,其中A和G为固体单质,已知A-E和F-J中分别含有同一种元素。反应E→A+O2的反应条件未标出。
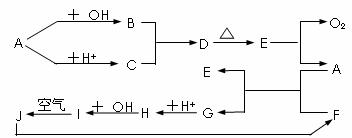
请填写下列空白:
(1)化合物H中的阳离子是_____________,D的化学式是______________。
(2)A生成B的离子方程式是 。
(3)向H的溶液中加入Na2O2后发生的现象是______________________________。
(4)I→J反应的化学方程式是 ,由H→J反应过程中发生的现象是 。
26.(18分)U、V、W、X、Y、Z是原子序数依次增大的六种短周期元素。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,其在W2中燃烧可生成淡黄色固体。Z的单质在W2中燃烧的产物可使品红溶液褪色。Y的单质也是一种金属,该金属在UW2中剧烈燃烧能生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为__________________;YW的电子式为______________;
X在周期表中的位置为_________________________。
(2)U元素形成的同素异形体的晶体类型可能是(填序号)_______。
① 原子晶体 ② 离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W分别与氢元素可形成10电子氢化物。U、V的氢化物中沸点较低的是(写化学式)____________;V、W的氢化物分子中结合H+能力较强的是(写化学式)____________,请用一个离子方程式加以证明________________________________。
(4)ZW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体VW,请用一个离子方程式表示有关反应________________________________________。
(5)已知通常状况下1g Z在W2中完全燃烧放出a kJ的热量,请写出表示Z燃烧热的热化学方程式________________________________________________________。
13.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60 mL B.45 mL C.30 mL D.15 mL
第Ⅱ卷(非选择题,共174分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com