
5.“白色污染”泛指塑料污染,常见的塑料有①聚乙烯②聚丙烯③聚氯乙烯④聚苯乙烯等,下列关于它们的叙述正确的是 ( )
A.都是烯烃 B.分子内部都含有双键
C.它们的单体都能发生加聚反应 D.它们的分子结构都是空间网状结构
4.金属的下列性质中,不能用金属晶体结构加以解释的是 ( )
A.易导电 B.易导热 C.有延展性 D.易锈蚀
3.下列叙述中不正确的是 ( )
A.油脂属于酯类 B.油脂的氢化又叫油脂的硬化
C.油脂是纯净物,不是混合物 D.某些油脂兼有醋和烯烃的一些化学性质
2.胶体区别于其他分散系的本质特征是 ( )
A.胶体粒子可以透过滤纸 B.胶体粒子大小在lnm-100nm之间
C.胶体粒子不能透过半透膜 D.光束穿过胶体时形成一条光亮的“通路”
1.下列物质一定不是天然高分子的是 ( )
A.尼龙 B.橡胶 C.蛋白质 D.纤维素
26.某石灰石样品中含有少量SiO2杂质。5.0g样品与50mL 2mol/L盐酸充分反应后,得到1064mL CO2(标准状况)。计算:
(1)石灰石样品中SiO2的质量分数;
(2)中和多余盐酸所需要1mol/L NaOH溶液的体积。
25.(11分)实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。

请回答下列问题:
(1)操作Ⅰ的名称为 ,通常操作Ⅱ所需要的玻璃仪器有 。
(2)若用硝酸钡来代替氯化钡,是否可行? (填“是”或“否”),请说明理由: 。
(3)若实验所得沉淀甲、固体乙的质量分别为Wg和Wg,则样品中K2SO4的质量分数计算式为 。
(4)某同学对该实验方案提出质疑,他认为加适量氯化钡溶液不容易控制,应该加入过量氯化钡溶液,并按照以下思路对氯化钾样品进行提纯。请填写试剂①和试剂②的名称。
试剂①: 、试剂②: 。

24.(4分)KA1Si3Ox是正长石的化学式,其中x= ,若以氧化物的形式表示其组成应写成 。
23.(9分)甲、乙、丙为常见单质,组成乙、丙的元素是周期表中同一主族的短周期元素, A、B、C、D、E、F均为常见化合物,A、B、F的焰色反应为黄色,各物质转化关系如下图所示:
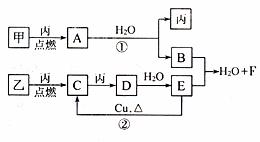
请按要求填空
(1)写出下列物质的化学式:甲 ,乙 ,丙 。
(2)指出A的一种用途 。
(3)C和空气中氮的氧化物随雨水降下就成为酸雨。酸雨的pH小于 。
(4)②的化学反应方程式为: 。
22.(9分)有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表。
|
元素特征信息 |
|
|
A |
其单质在F单质中燃烧,产生苍白色火焰 |
|
B |
最外层电子数是次外层电子数的三倍 |
|
C |
其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
|
D |
其氢氧化物和氧化物都有两性,与C同周期 |
|
E |
在地壳中,该元素的含量居第二位 |
|
F |
与C同周期,原子半径在该周期最小 |
回答下列问题:
(1)写出下列元素的元素符号:C ,D 。
(2)在A、B、E、F四种元素形成的化合物:A2B、A2B2、AF、EF4中各原子都满足最外层8电子结构的是 (填写化学式)。
(3)用电子式表示CF的形成过程: 。
(4)①写出EB2与A、B、C形成的化合物反应的化学方程式:
。
②F单质与A、B、C形成的化合物的水溶液在常温下反应的离子方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com