
3.下列关于物质性质变化的比较,不正确的是 ( )
A.酸性强弱:HIO4>HBrO4>HClO4 B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH D.金属性强弱:Na>Mg>Al
2.雷雨天闪电时空气中有臭氧(O3)生成,下列说法正确的是 ( )
A.O2和O3互为同位素
B.O2和O3的相互转化是物理变化
C.在相同的温度与压强下,等体积的O2和O3含有相同的分子数
D.等质量的O2和O3含有不同的原子数
1.某粒子含有10个电子,10个中子,带两个单位负电荷,则它的化学符号是 ( )
A.20Ar B.16O C.18O D.18O2-
29.(15分)一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质,不溶于水,也不溶于一般有机溶剂。能发生如下变化(A-F均分别代表一种物质,框图中的部分产物已略去)
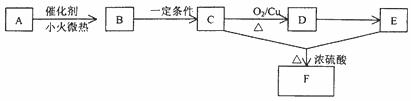
(1)由A生成B所使用的催化剂是 ,所得到的溶液的颜色是 ,化学方程式为 。
(2)B、D均含有的官能团是 ,设计实验,用弱氧化剂检验(1)所得到的溶液中的B分子结构中存在该官能团(要求:所需仪器和药品可以任选,如需采用实验室不能长期保存的试剂请写出它的制备过程;以下步骤可以填不满。)
①
②
③
④
⑤
(3)从A到F发生的反应类型有
A.氧化 B.酯化 C.消去 D.水解
(4)写出C到D所发生的化学反应的化学方程式
(5)F有多种同分异构体,请写出与它有相同官能团的所有同分异构体
28.(15分)
I.下列实验操作、试剂保存方法和实验室事故处理,一定正确的是 (填序号)。
A.实验室中,浓硝酸保存在带橡胶塞的棕色细口试剂并中;
B.制备氢氧化铁胶体时,应向20mL沸水中逐滴滴加1~2mL饱和的FeCl3溶液,并继续加热到液体呈透明的红褐色为止;
C.在石油的分馏实验中,温度计需插入液体中;
D.不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液;
E.用酸式滴定管量取20.00mL高锰酸钾酸性溶液;
F.在进行中和热测定时,为保证实验的准确性,我们可以采取以下具体措施:使用碎泡沫以起到隔热保温的作用、使用铜质搅拌棒进行搅拌、取用的碱溶液略过量、进行两到三次实验取平均值。
II.无水CuSO4在500℃以上按下式分解:CuSO4 CuO+SO3↑+SO2↑+O2↑(未配平),某同学为测定一定量的CuSO4受热分解所产生的SO3、SO2、O2的物质的量,从而通过计算来确定该条件下CuSO4分解方程式中各物质的化学计量数。实验的主要仪器如下:
CuO+SO3↑+SO2↑+O2↑(未配平),某同学为测定一定量的CuSO4受热分解所产生的SO3、SO2、O2的物质的量,从而通过计算来确定该条件下CuSO4分解方程式中各物质的化学计量数。实验的主要仪器如下:

实验所测得数据及有关事项如下:
a.准确称取6.4g无水CuSO4;
b.装置C在实验结束时增重2.88g;
c.实验结束后,测量量筒中水的体积后,折算成排出水的气体的体积(标准状况下)为224mL。
(1)按装置从左至右的方向,各仪器接口的连接次序为 (用圆圈数字表示)。
(2)500℃以上CuSO4分解的产物中,能被碱石灰吸收的气体有 (填分子式)。
(3)D装置中无水CaCl2的作用是: 。
(4)实验前,还需向盛满水的D装置中通入O2(所需的O2另用它法制取)使之达饱和,这样操作的目的是 。
(5)假设CuSO4完全分解且所有气体全被吸收或排出,通过题中所给的数据进行必要计算,CuSO4完全分解所得SO3的物质的量是 mol,该条件下无水CuSO4分解的化学方程式是 。
27.(15分)下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。

(1)在表中画出主族与非主族的交界线(不考虑零族元素),并分别用“△”将每个周期的第一个非金属所在的位置标同。
(2)字母H表示的元素符号为 该元素的名称是 。
(3)比较C和E气态氢化物水溶液的酸性强弱: > (填化学式)比较G和D单质的熔点高低: > (填化学式)
(4)工业制硝酸的基础是对元素 和 (填上表中的字母代号)形成的化合物 (填化学式)进行催化氧化,该反应的化学方程式为
(5)F单质在E单质中燃烧,产生 (描述实验现象)这是 (填物质名称)。加水振荡后,得到 溶液(描述颜色)。
26.(15分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水。向该盐的溶液中滴加足量的盐酸,随着盐酸的逐滴加入,所观察到的现象是 ,反应结束时,该反应的总反应离子方程式为 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为 。它的水溶液中存在多种离子,请根据电荷守恒写出一个用离子浓度表示的等式: 。
(3)若甲为W的最高价氧化物对应的水化物,乙为Y的氢化物。
现有①0.2mol/甲的溶液和②0.2mol/L乙的溶液,则①中由水电离出的c(OH-) ②中由水电离出的c(OH+)。(填“>”、“=”或“<”)
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
。
13.下列各项表述中正确的是 ( )
A.由 与
与 在溶液中可以共存,推测:
在溶液中可以共存,推测: 与
与 在溶液中可以共存
在溶液中可以共存
B.足量的氢氧化钙溶液中滴加少量的碳酸氢镁:

C.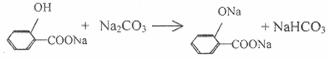
D.碘化亚铁溶液通入一定量的氯气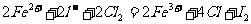
第II卷
12.在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的情况。下列反应中属于这种情况的是 ( )
①过量的锌与浓硫酸反应 ②过量的氢气与少量的N2在工业生产条件下
③过量的浓盐酸与碳酸钙反应 ④过量的乙酸和少量乙醇在浓硫酸、加热条件下
⑤过量二氧化锰与浓盐酸在加热条件下⑥过量的铜与浓硫酸在加热条件下
A.②③④⑥ B.②④⑤⑥ C.①②④⑤ D.③④⑤⑥
11.用Pt作电极,电解串联电路中分装在甲、乙两个烧杯中的200mL0.3mol/LNaCl溶液和现300mL0.15mol/L的AgNO3溶液,当甲中产生0.56L(标准状况)Cl2时停止电解,取出电极,将两杯溶液混合,混合液在室温下的pH为(设混合后总体积为500mL,且所产生的Cl2全部逸出) ( )
A.2 B.7 C.11.7 D.12
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com