
6.化学与生活、社会密切相关。下列叙述不正确的是 ( )
A.SO2、NO2或CO2都会导致酸雨的形成
B.银器久置后表面变暗,可能是发生了化学腐蚀
C.甲醛的含量属于食品安全检测的指标
D.食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质
29.(16分)已知:1,具有 结构(R1、R2、R3、R4可以是H,也可以是
结构(R1、R2、R3、R4可以是H,也可以是
其它原子或原子团)的物质不能稳定存在;
2,R-CH=CH-OH会自动转化为R-CH2-CHO;
3,甲醛中四个原子共平面。
某芳香族化合物A(分子式:C12H12O2)在一定条件下可以转变为B和C(分子式:C4H6O),相关转化关系如下图所示:

B能与NaHCO3反应产生CO2,且苯环上的一氯取代物有两种同分异构体;C能发生银镜反应,且分子中无支链。
请根据以上全部信息,回答下列问题:
(1)、C中官能团的名称是: ;
(2)、A的结构简式是: ;
(3)、①:E(分子式:C3H4O)是C的同系物,写出E与银氨溶液反应的化学方程式: ;
②:写出由C生成D的化学方程式: ;
(4)C有多种同分异构体,与C具有完全相同官能团的同分异构体(不含C)共有
种;
(5)B不具有的化学性质有: (填序号)
①遇FeCl3溶液显紫色;
②能使酸性高锰酸钾溶液褪色;
③能发生消去反应;
④一定条件下能发生取代反应。
(6)一个B分子中最多有 个原子共平面;
(7)1mol D与足量的Na反应,能生成标准状况下的气体的体积为 。
28.(I)(8分)某课外活动小组同学拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度,并除去尾气。(假设矿石中不含其他与CO反应的成分。与Fe2O3反应的CO需纯净、干燥。CO气体用H2C2O4  CO2↑+CO↑+H2O来制取。)
CO2↑+CO↑+H2O来制取。)
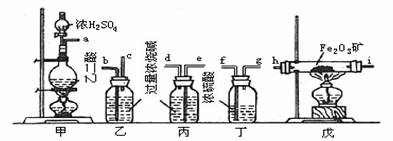
①若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a、b…表示)____接____,____接____,____接____,____接____,____。
②装置乙的作用是___ _。装置丙的目的是_ ___。
③实验结束后,先熄灭戊处的酒精灯,待戊冷却后再熄灭甲处的酒精灯,其主要原因是:
_ 。
(II)(8分)在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色稀溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;

当溶液中的原溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重1.6 g 。请回答下列问题:
①B电极的反应式_____________________。
②原溶液的物质的量浓度是_________________;电解后溶液的pH为________。(假设电解前后溶液的体积不变)
③请你设计实验确定原溶液中可能所含的酸根离子,要求:提出假设并
写出验证的操作步骤、实验现象和实验结论。
_____________________________________________________________________
_______________________________________________________________________。
27.(14分)氯碱工业中,通过电解饱和食盐水获得重要的化工原料,其产物中的氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、聚氯乙烯、氯苯等。
(1)电解食盐水的离子方程为 。
氯气用于生产半导体材料硅的流程如下:

①在制备粗硅时,焦炭的作用是 。
②粗硅与氯气反应后得到的液态四氯化硅中常混有一些杂质,必须进行分离提纯。其提纯方法为 。
③由四氯化硅得到高纯硅的化学方程式为: 。
(2)用于制造塑料薄膜、人造革、塑料管材和板材的聚氯乙烯(PVC塑料)就是以氯气和乙烯为主要原料通过加成、消去和 三步主要反应生产的,这三步的化学方程式分别为:CH2 =CH2 +Cl2→CH2Cl-CH2Cl、CH2Cl-CH2Cl→CH2 =CHCl +HCl、 。
(3)上述两种生产过程可得到同一种副产品,该副产品是 。
26.(14分)A、B、C、D、E、F均为短周期元素,其原子序数依次增大,A的最外层电子数等于其电子层数;B与A形成的某分子空间结构为正四面体;D是地壳中含量最高的元素;D与F易形成FD2、FD3型化合物,A和E同主族。请回答:
(1) B与D组成化合物BD2的电子式为: ,属 分子(填“极性”或“非极性”),所形成晶体的类型为: 晶体。
(2)均由A、D、E、F四种元素组成的两种盐,其摩尔质量相差16,写出它们在溶液中发生反应的离子方程式:__________________________________________;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)___________ __________ __。
(3) A与C组成的化合物C2A4可做火箭推进剂,若在空气中每燃烧1g该液态物质生成一种组成空气成分的气体和液态A2D时,放出QkJ的热量,写出该物质燃烧的热化学方程式:__________________________________________。
12.已知A(g)+B(g) C(g);ΔH=a。下图中的两条曲线分别表示200℃和300℃时,体系中B的百分含量和时间t的关系。下列说法中正确的是 ( )
C(g);ΔH=a。下图中的两条曲线分别表示200℃和300℃时,体系中B的百分含量和时间t的关系。下列说法中正确的是 ( )

① a>0 ;
② a<0;
③ R表示300℃的曲线 ;
④R表示200℃的曲线
⑤200℃时的平衡混合物相对分子质量大于300℃时的平衡混合物相对分子质量
A.②③⑤ B.②④ C.②③ D.①③
|
LaNi5H6
+ 6NiO(OH) LaNi5
+ 6Ni(OH)2 ,下列说法正确的是
LaNi5
+ 6Ni(OH)2 ,下列说法正确的是
A.放电时储氢合金作正极
B.放电时负极反应:LaNi5H6+6OH――6e-=LaNi5+6H2O
C.充电时储氢合金作阳极
D.充电时阳极周围c(OH-)增大
第Ⅱ卷
11.被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品。截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义。其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如下图所示。有关该化合物的叙述正确的是 ( )
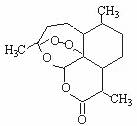
A.分子式为:C16H22O5
B.该化合物在一定条件下不能与NaOH溶液反应
C.该化合物中含有过氧键,一定条件下有氧化性
D.青蒿素与维生素一样是水溶性的
10.下列比较中,正确的是 ( )
A.0.1mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
B.pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原溶液的m倍和n倍,若稀释后两溶液的pH仍相同,则m=n
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) + c(CH3COOH)== 2c(Na+)
D.同浓度的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③NH3·H2O ④CH3COONH4,
其中c(NH4+) 由大到小的顺序是:①>④>②>③
9.下列反应的离子方程式中正确的是 ( )
A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应
CH3OH+H2O-6e-= CO2↑+6H+
B.在NaHSO4溶液中加Ba(OH)2溶液至中性
H++SO42-+Ba2++OH-= BaSO4↓+H2O
C.NaHSO3溶液与稀硝酸反应:HSO3-+H+=SO2↑+H2O
D.用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O = NaHCO3↓+NH4+
8.通过复习总结,你认为下列对化学知识概括合理的一组是 ( )
①能与酸反应的氧化物,一定是碱性氧化物
②一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
③原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
④原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
⑤在熔化状态和水溶液中均不能导电的物质称为非电解质
⑥NF3的沸点比NH3的沸点低是因为N-F键比N-H键的键能大
A.只有①② B.只有③④ C.只有⑤⑥ D.只有④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com