
17.(10分)下列B~G均可由有机物A通过不同的反应制得。试回答下列问题:
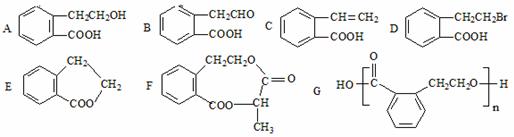
(1)A→C的反应的类型为:__________。A→E的反应的类型为:___________。
(2)在A-G七种物质中,互为同分异构体的是_________________(填代号,多选扣分,下同)。可看作酯类的是____________________。
(3)由A制取F时的另一反应物的结构简式为____________________________。
(4)请写出D的同分异构体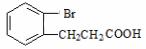 与足量NaOH溶液在一定条件下反应的化学方程式______________________________________________________。
与足量NaOH溶液在一定条件下反应的化学方程式______________________________________________________。
16.(8分)某研究性学习小组在实验室合成了一种物质A。
(1)经分析,A的相对分子质量不超过100,A中C、H的质量分数分别为:w(C)=69.76%,w(H)=11.63%,且完全燃烧后产物只有CO2和H2O。则A的摩尔质量为 _________ 。
(2)该兴趣小组同学对物质A结构进行了预测,其中不正确的是 (填序号)
A.可能含有一个碳环和一个醛基 B.可能含有一个碳碳双键和一个羟基
C.可能只含一个碳氧双键官能团 D.可能是环状的醚
(3)若A的核磁共振氢谱如下图所示,且A可以和金属钠反应生成H2,但不能在Cu作催化剂下被催化氧化。(提示:羟基与碳碳双键相连的结构不稳定)
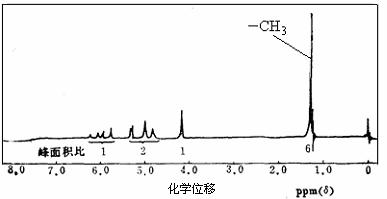
请根据以上信息写出A的结构简式 。
(4)A的某种同分异构体B分子中不含支链,能发生银镜反应。写出B发生银镜反应的化学方程式 。
15.(12分)环己酮(微溶于水,易溶于醇和醚,沸点155.7℃)是一种重要的有机化工原料,主要用于制造己内酰胺和己二酸。实验室可用环己醇氧化制取环己酮(已知该反应为放热反应):

实验步骤如下:
① 将重铬酸钠溶于适量水,边搅拌边慢慢加入浓H2SO4,将所得溶液冷至室温备用。
② 在一圆底烧瓶(乙)中加入适量环己醇,并将①中溶液分三次加入圆底烧瓶,每加一次都应振摇混匀。控制瓶内温度在55℃-60℃之间,充分反应0.5h。
③ 向②反应后的圆底烧瓶内加入少量水,并接入下图所示装置中,将T形管的活塞K打开,甲瓶中有适量水,加热甲,至有大量水蒸气冲出时关闭K,同时接通冷凝水。
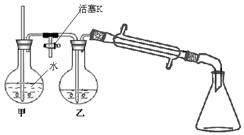
④ 将步骤③锥形瓶中收集到的液体分液,水层用乙醚(乙醚沸点34.6℃,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸)萃取,萃取液并入有机层。再向有机层中加入无水硫酸钠静置后转入干燥的圆底烧瓶中,进行蒸馏,除去乙醚后收集151℃-155℃馏分。
根据以上步骤回答下列问题:
(1)步骤①所得溶液分三次加入环己醇的原因是________________________________。
(2)步骤③利用图示装置进行实验的目的是_______________________,实验过程中要经常检查甲中玻管内的水位。若玻管内的水位升高过多,其可能原因是__________________,此时应立即采取的措施是_________________________。
(3)步骤④中加入无水硫酸钠的作用是_________,蒸馏除乙醚的过程中采用的加热方式为____________________。
(4)写出该实验中可能发生的一个副反应的化学方程式______________________
14.α-鸢尾酮香料的分子结构如下图,下列说法正确的是
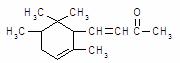
A.α-鸢尾酮的化学式为C14H24O
B.1molα-鸢尾酮最多可与3molH2加成
C.α-鸢尾酮能发生银镜反应
D.α-鸢尾酮既能发生氧化反应又能发生还原反应
|
13.下列说法正确的是
A.天然橡胶 和杜仲胶
和杜仲胶
属于同分异构体
B. 属于同系物
属于同系物
C.合成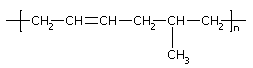 的单体为乙烯和2-丁烯
的单体为乙烯和2-丁烯
D.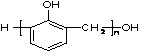 是由苯酚和甲醛发生加成反应后的产物脱水缩合而成
是由苯酚和甲醛发生加成反应后的产物脱水缩合而成
12.已知下列反应的热化学方程式:
(1)C(s)+O2(g)=CO2(g) ΔH 1=-393.5kJ/mol
(2)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
(3)H2(g)+ O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热(焓变)为
A.-488.3 kJ/mol B.+488.3 kJ/mol C.-244.15 kJ/mol D.+244.15 kJ/mol
11.下列实验设计、操作或实验现象均正确的是
A.检验甲酸中是否混有甲醛,可先向样品中加入足量NaOH溶液中和甲酸,再进行银镜反应实验
B.检验纤维素水解产物时,应将脱脂棉与18.4mol/L的硫酸一起充分搅拌,然后加入新制Cu(OH)2并加热至沸腾,观察现象
C.用新制碱性氢氧化铜悬浊液鉴别乙醇、乙醛、乙酸三种物质的水溶液。
D.通过向液态溴乙烷中滴加AgNO3溶液和稀HNO3观察有无淡黄色沉淀生成,以检验其中的溴元素
10.下列文字表述与反应方程式对应且正确的是
A.实验室用液溴和苯在催化剂作用下制溴苯:
B.向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
C.1 L0.5 mol/L稀硫酸与1 L1 mol/L氢氧化钠溶液反应放出57.3 kJ的热:
H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H=-114.6 kJ/mol
D.表示氢气燃烧热的热化学方程式: H2(g)+1/2O2(g)=H2O(g);△H=-241.8kJ/mol
9.NA为阿伏加德罗常数,下列叙述中正确的是
A.标准状况下,22.4L己烷中共价键数目为19NA
B.常温下,0.1mol甲烷与甲醛混合气体中所含碳原子数为0.1NA
C.在标准状况下,2.24L四氯甲烷中所含分子数大于0.1NA
D.1mol苯分子中含有碳碳双键数为3NA
8.两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如下图所示。下列有关混合气体的说法错误的是

A.该混合气体中一定含有乙烯
B.该混合气体中有且只有一种烷烃
C.组成该混合气体的烃分子所含氢原子数均为4
D.若混合气体由CH4和C2H4组成,则其体积比为2∶3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com